Перейти к:
Эффективность и безопасность профилактики венозных тромбоэмболических осложнений у беременных высокого риска: анализ результатов регистра беременных «БЕРЕГ»
https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.652
Аннотация
Введение. В последние годы наряду с увеличением возраста женщин, вступающих в беременность, и количества пациенток с экстрагенитальной патологией большую роль отводят прегравидарной подготовке и реализации профилактических мер, направленных на минимизацию развития тяжелых и нередко фатальных состояний, в частности, венозных тромбоэмболических осложнений (ВТЭО), которые являются одной из ведущих причин материнской и перинатальной смертности в развитых странах.
Цель: анализ эффективности и безопасности тромбопрофилактики у беременных с высоким риском развития ВТЭО в реальной клинической практике.
Материалы и методы. Анализ осуществлен на основании данных наблюдательного (когортного) исследования «Оценка клинического состояния беременных в течение гестации, в родах, раннем послеродовом периодах и через 12 месяцев после родов, а также анализ перинатальных исходов, состояние плода, новорожденного и качества лечения этих пациенток» – регистр «БЕРЕГ». Критерии включения в регистр: беременность на первом визите, получение письменного информированного согласия на участие в исследовании и постоянное проживание в Туле или Тульской области. Критерии невключения: нежелание подписать информированное согласие и проживание в других регионах. Данные брались из амбулаторной и стационарной карт и включали жалобы, анамнез, информацию о перенесенных и имеющих место заболеваниях, факторы риска ВТЭО, антропометрические показатели – рост, масса тела, индекс массы тела на момент вступления в беременность, препарат и доза антикоагулянта и антиагреганта. Особое внимание уделено акушерскому анамнезу – течению предыдущих и настоящей беременности, их перинатальным исходам, способам родоразрешения. Риск развития ВТЭО и тактику тромбопрофилактики оценивали по шкале «Антенатальная и постнатальная оценка факторов риска и тактика ведения беременности». Состояние новорожденного оценивали по росто-весовым показателям и по шкале Апгар на 1-й и 5-й минутах жизни.
Результаты. Всего в регистр вошли 3214 беременных в возрасте от 15 до 46 лет, из которых были выделены 330 (10,3 %) женщин, получавших антитромботическую терапию антикоагулянтами и/или дезагрегантами. Из них 217 (65,8 %) принимали комбинированную терапию надропарином кальция (Фраксипарин) в дозе 0,3 мл (2850 МЕ анти-Ха) подкожно однократно в сутки в сочетании с ацетилсалициловой кислотой (АСК) в дозе 150 мг/сут перорально (группа 1) и 113 (34,2 %) – монотерапию АСК 150 мг/сут однократно перорально (группа 2). По основным клинико-лабораторным характеристикам группы были сопоставимы. Случаев ВТЭО, материнской смертности, аллергических реакций, тромбоцитопении и гепарин-индуцированных тромбозов в обеих группах зарегистрировано не было. Однако только в группе пациенток на монотерапии АСК имели место такие осложнения как кровотечение в родах (n = 1) и гибель плода (n = 3), но четкой связи с приемом препарата установить не представлялось возможным вследствие небольшого числа наблюдений. Обращает внимание недостаточная информированность врачей в необходимости использования шкал по оценке риска развития ВТЭО с целью объективизации тактики медикаментозного лечения, что определялось отсутствием в медицинских картах указаний об их использовании.
Заключение. Проведенный анализ показал эффективность и безопасносность тромбопрофилактики препаратом Фраксипарин в фиксированной дозе 0,3 мл у беременных высокого риска в реальной клинической практике, что подтверждено отсутствием случаев ВТЭО, кровотечений, материнской смерти, аллергических реакций, тромбоцитопении и гепарин-индуцированных тромбозов. Возможно, ввиду недостаточной информированности врачей о необходимости использования шкал по оценке риска развития ВТЭО для объективизации последующей тактики медикаментозного лечения были произвольно выбраны схемы профилактического воздействия – комбинированная терапия низкомолекулярным гепарином в сочетании с АСК или монотерапия АСК.
Ключевые слова
Для цитирования:
Стрюк Р.И., Крикунова О.В., Локшина Э.Э., Гомова Т.А., Федотова Е.Е. Эффективность и безопасность профилактики венозных тромбоэмболических осложнений у беременных высокого риска: анализ результатов регистра беременных «БЕРЕГ». Акушерство, Гинекология и Репродукция. 2025;19(5):705-715. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.652
For citation:
Stryuk R.I., Krikunova O.V., Lokshina E.E., Gomova T.A., Fedotova E.E. Efficacy and safety for preventing of venous thromboembolic complications in high-risk pregnant women: results of the «BEREG» pregnant women registry. Obstetrics, Gynecology and Reproduction. 2025;19(5):705-715. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.652
Введение / Introduction
В последние годы наряду с увеличением возраста женщин, вступающих в беременность, возросло количество пациенток с экстрагенитальной патологией, предрасполагающей к развитию осложнений гестации и неблагоприятным перинатальным исходам, что ранее было отмечено нами при анализе результатов наблюдательного обсервационного исследования – регистра беременных «БЕРЕГ» [1]. В этой связи большую роль отводят прегравидарной подготовке и реализации профилактических мер, направленных на минимизацию развития тяжелых и нередко фатальных состояний, в частности, венозных тромбоэмболических осложнений (ВТЭО), которые являются одной из ведущих причин материнской и перинатальной смертности в развитых странах [2–4]. По данным Росстата, в Российской Федерации в последние 5 лет частота ВТЭО из числа заболеваний, осложнивших роды, также как и из числа женщин, закончивших беременность, не имеет тенденции к снижению и даже несколько возрастает [5]. Беременность можно рассматривать как модель физиологической гиперкоагуляции, для которой характерны все признаки триады Вирхова:
– изменение коагулирующих свойств крови – увеличение содержания прокоагулянтных факторов (F) FVIII, FVII, FV, FX, FXII, FVII, фибриногена; снижение активности антикоагулянтной системы за счет развития резистентности к активированному протеину С и снижения уровня протеина S; продукция плацентой ингибитора активатора плазминогена 2-го типа (англ. plasminogen activator inhibitor-2, PAI-2) и увеличение экспрессии ингибитора активатора плазминогена 1-го типа (англ. plasminogen activator inhibitor-1, PAI-1) на эндотелии, повышение уровня антиплазмина и ингибитора фибринолиза, активируемого тромбином (англ. thrombin activatable fibrinolysis inhibitor, TAFI);
– замедление скорости кровотока за счет уменьшения тонуса вен вследствие избытка гестагенов, компрессия вен таза беременной маткой, увеличение кровотока по маточной вене и внутренним подвздошным венам;
– повреждение тазовых вен вследствие компрессии их в родах; при оперативном родоразрешении создаются благоприятные условия для ВТЭО, особенно при наличии факторов риска их развития.
В группу высокого риска ВТЭО входят женщины с тромбофилией и ВТЭО в анамнезе, повторнорожавшие, с многоплодной беременностью, метаболическим синдромом, хронической артериальной гипертонией (ХАГ), хронической варикозной болезнью, курящие, забеременевшие в результате вспомогательных репродуктивных технологий, с наличием преэклампсии (ПЭ) в анамнезе и в текущей беременности, с другими осложнениями гестации и экстрагенитальными заболеваниями [6].
Венозные тромбозы магистральных вен приводят к тромбированию сосудов плаценты, ухудшают маточно-плацентарное кровообращение и внутриутробное состояние плода, предопределяя рост материнской и перинатальной смертности, приводя к тяжелым отдаленным осложнениям – посттромбофлебитическому синдрому, нередко его хронической форме с формированием трофических язв, хронической легочной гипертензии [6]. С учетом важности данной проблемы встают вопросы своевременной оценки факторов риска ВТЭО у беременной на всех этапах гестации с целью принятия решения о проведении тромбопрофилактики, что и явилось основанием для анализа ведения беременных с высоким риском развития ВТЭО в реальной клинической практике.
Цель: анализ эффективности и безопасности тромбопрофилактики у беременных с высоким риском развития ВТЭО в реальной клинической практике.
Материалы и методы / Materials and Methods
Дизайн исследования / Study design
В основу анализа положены данные наблюдательного (когортного) исследования «Оценка клинического состояния беременных в течение гестации, в родах, раннем послеродовом периодах и через 12 месяцев после родов, а также анализ перинатальных исходов, состояние плода, новорожденного и качества лечения этих пациенток» – регистр «БЕРЕГ», выполненного в рамках государственного задания «Маркеры рисков здоровья и триггеры патогенеза сердечно-сосудистых, аутоиммунных, онкологических заболеваний у женщин» – проект «Три возраста женщины». Регистр «БЕРЕГ» был проведен на базе ГУЗ «Тульский областной перинатальный центр» в период с 01.01.2014 по 31.12.2014, перед проведением регистра были получены все разрешительные документы Межвузовского комитета по этике и Министерства здравоохранения Тульской области. Протокол исследования включал сквозное включение беременных, соответствующих критериям включения/невключения, поступивших в ГУЗ «Тульский областной перинатальный центр имени В.С. Гумилевской» для родоразрешения в период с 01.01.2014 по 31.12.2014.
Критерии включения и невключения / Inclusion and non-inclusion criteria
Критерии включения в регистр: беременность с момента первого обращения; постоянное проживание пациентки в Туле или Тульской области; письменное информированное согласие.
Критерии невключения в регистр: проживание в других регионах; нежелание пациентки подписать информированное согласие на участие в исследовании.
Группы обследованных / Study groups
Всего в регистр БЕРЕГ вошли 3214 беременных в возрасте от 15 до 46 лет, среди которых были выделены 330 (10,3 %) женщин, получавших антитромботическую терапию антикоагулянтом и/или дезагрегантом; из них сформировали 2 группы: группу 1 составили пациентки, получавшие комбинированную терапию низкомолекулярным гепарином (НМГ) – надропарином кальция в сочетании с ацетилсалициловой кислотой (АСК), группу 2 – пациентки, получавшие только АСК.
Методы исследования / Study methods
Все данные по пациенткам были взяты из амбулаторной и стационарной карт и включали жалобы, анамнез, информацию о перенесенных заболеваниях, в том числе существующих на настоящий момент, факторы риска ВТЭО, антропометрические показатели – рост, масса тела, индекс массы тела (ИМТ), рассчитанный по формуле Кетле: ИМТ = вес (кг)/рост² (м²) на момент вступления в беременность, препарат и доза антикоагулянта и антиагреганта. Особое внимание уделено акушерскому анамнезу – течению предыдущих и настоящей беременности, их перинатальным исходам, способам родоразрешения. Риск развития ВТЭО и тактику тромбопрофилактики оценивали по шкале «Антенатальная и постнатальная оценка факторов риска и тактика ведения беременности» согласно действующим клиническим рекомендациям [7][8]. Состояние новорожденного оценивали по росто-весовым показателям и по шкале Апгар на 1‑й и 5‑й минутах жизни.
Терапия / Therapy
Из 330 пациенток 217 (65,8 %) женщин (группа 1) получали комбинированную терапию надропарином кальция; все женщины получали только оригинальный препарат Фраксипарин производства Аспен Нотр Дам де Бондевиль (Франция) в дозе 0,3 мл (2850 МЕ анти-Ха) подкожно однократно в сутки в сочетании с АСК в дозе 150 мг/сут перорально. Пациентки группы 2 – 113 (34,2%) женщин получали монотерапию АСК 150 мг/сут однократно перорально.
Статистические методы / Statistical analysis
Статистическую обработку полученных данных осуществляли с использованием пакета программ Statistica 10.0 (StatSoft Inc., США). Качественные показатели представлены в виде частот и процентов, количественные показатели – в виде среднего арифметического (M) и стандартного отклонения (SD). Для количественных показателей использовали t-критерий Стьюдента (Уэлча) в попарных сравнениях групп (так как дисперсии и численность в группах могут отличаться), для качественных (доля событий в процентах) – точный критерий Фишера в виде 2×2-таблиц также в попарном формате. Различия считали значимыми при уровне значимости р < 0,05.
Результаты / Results
Как видно из представленных в таблице 1 данных, группы пациенток были сопоставимы и не различались по основным клиническим параметрам.
Таблица 1. Клиническая характеристика пациенток, включенных в субанализ регистра «БЕРЕГ».
Table 1. Clinical characteristics of patients included in the register «BEREG» subanalysis.
|
Показатель Parameter |
Группа 1 Group 1 n = 217 |
2 группа Group 2 n = 113 |
p |
|
Средний возраст, лет, М ± SD Average age, years, M ± SD |
30,3 ± 5,8 |
31,3 ± 5,8 |
> 0,05 |
|
Возраст ≥ 35 лет, n (%) Age ≥ 35 years, n (%) |
53 (24,4) |
30 (26,5) |
> 0,05 |
|
Предстоящие роды по счету, М ± SD Upcoming birth, M ± SD |
2,9 ± 1,6 |
3,1 ± 1,7 |
> 0,05 |
|
Прибавка массы тела, кг, М ± SD Weight gain, kg, M ± SD |
12,4 ± 5,1 |
12,6 ± 10,4 |
> 0,05 |
|
Курение, n (%) Smoking, n (%) |
33 (15,2) |
13 (11,5) |
> 0,05 |
|
Хроническая артериальная гипертензия, n (%) Chronic arterial hypertension, n (%) |
11 (5,1) |
8 (7,1) |
> 0,05 |
|
Сахарный диабет, n (%) Diabetes mellitus, n (%) |
22 (10,1) |
9 (7,9) |
> 0,05 |
|
Хроническая варикозная болезнь, n (%) Varicose veins, n (%) |
2 (0,5) |
0 |
> 0,05 |
|
Экстракорпоральное оплодотворение, n (%) In vitro fertilization, n (%) |
2 (0,9) |
1 (0,9) |
> 0,05 |
|
Количество тромбоцитов, ×10⁹/л, М ± SD Platelets, ×10⁹/L, М ± SD |
202,2 ± 56,8 |
194,6 ± 62,6 |
> 0,05 |
|
Нормальный индекс массы тела, n (%) Normal body mass index (BMI), n (%) |
47 (21,7) |
22 (19,5) |
> 0,05 |
|
Избыточная масса тела (ИМТ = 25,0–29,9 кг/м²), n (%) Extra body weight (BMI = 25.0–29.9 kg/м2), n (%) |
67 (30,9) |
19 (16,8) |
> 0,05 |
|
Ожирение I степени (ИМТ = 30,0–34,9 кг/м²), n (%) Obesity grade I (BMI = 30.0–34.9 kg/м²), n (%) |
66 (30,4) |
31 (27,4) |
> 0,05 |
|
Ожирение II степени (ИМТ = 35,0–39,9 кг/м²), n (%) Obesity grade II (BMI = 35.0-39.9 kg/m²), n (%) |
31 (14,3) |
12 (10,6) |
> 0,05 |
|
Ожирение III степени (ИМТ > 40 кг/м²), n (%) Obesity grade III (BMI > 40 kg/m²), n (%) |
6 (2,8) |
3 (2,7) |
> 0,05 |
Примечание: ИМТ – индекс массы тела.
Note: BMI – body mass index.
Обращает внимание, что практически четверть пациенток обеих групп были старше 35 лет; у 71,6 % имело место нарушение жирового обмена – избыточная масса тела (26,1 %) или ожирение (45,5 %); курили 15,2 % женщин в группе 1 и 11,5 % в группе 2. Соматические заболевания – сахарный диабет и ХАГ выявлены примерно с одинаковой частотой в обеих группах наблюдения. Эти состояния, также как и возраст пациентки старше 35 лет, третьи и более роды, факт курения, вносят существенный вклад в суммарную балльную оценку риска развития ВТЭО [7][8]. На основании подсчета суммарного количества баллов по шкале риска развития ВТЭО, включающей, кроме предсуществующих факторов риска еще и акушерские – ПЭ во время текущей беременности, экстракорпоральное оплодотворение (ЭКО), кесарево сечение (КС), установлено, что в обеих группах наблюдения более 30 % женщин имели умеренный (2 и более баллов) и более 46 % высокий (3 и более баллов) риск развития ВТЭО и нуждались в тромбопрофилактике (рис. 1).
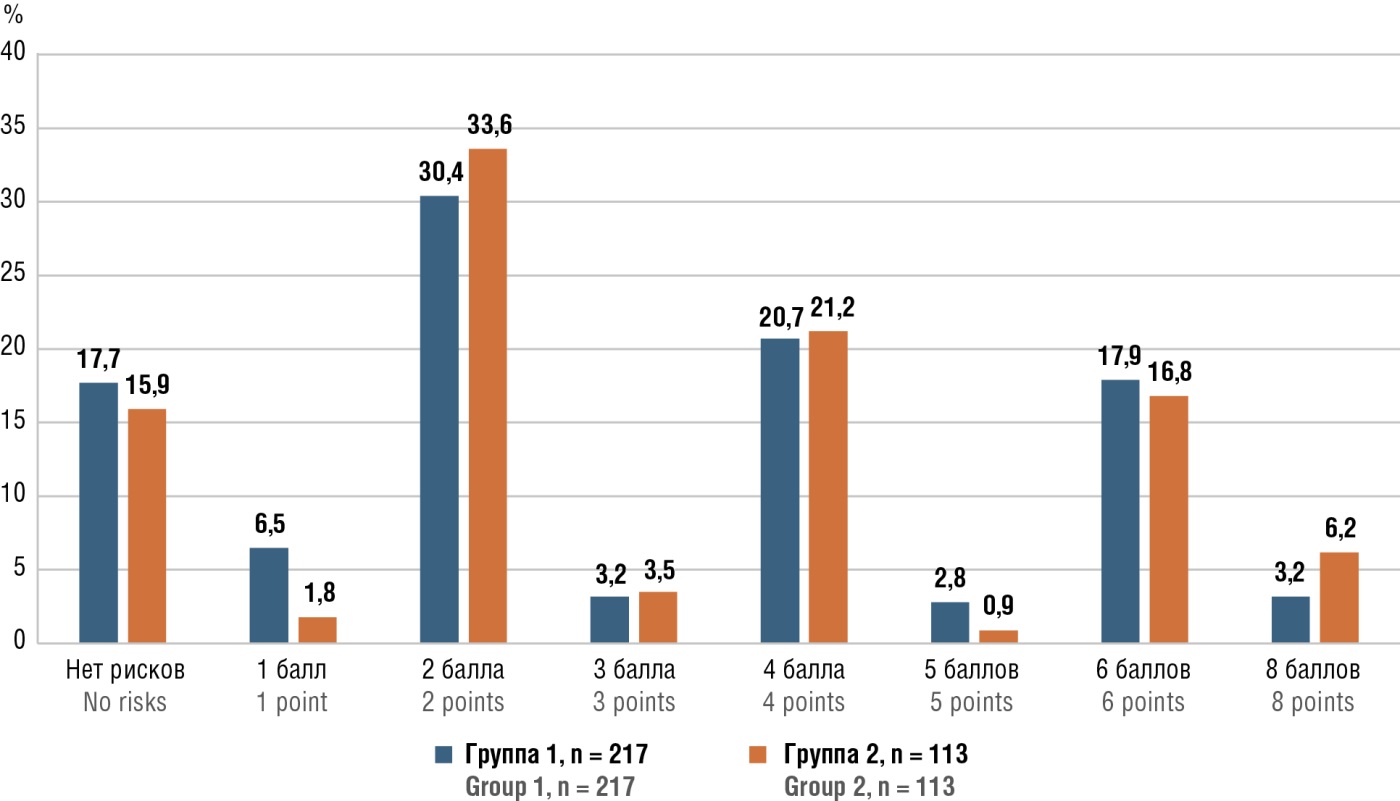
Рисунок 1. Распределение балльной оценки риска венозных тромбоэмболических осложнений.
Figure 1. Distribution of the risk score for venous thromboembolic events.
Анализ характера течения беременности, способа родоразрешения и перинатальных исходов продемонстрировал, что в обеих группах случаев ВТЭО и материнской смертности не было зарегистрировано; однако в группе 2 женщин, получавших АСК, в одном случае было зафиксировано тяжелое кровотечение в родах, а также достоверно чаще имели место гестационная артериальная гипертензия и риск реализации внутриутробной инфекции; у трех пациенток беременность закончилась гибелью плода (табл. 2). Анализ анамнеза, результатов клинико-лабораторных и инструментальных данных показал наличие у двух женщин ранней ПЭ на фоне тяжелой соматической патологиии; у одной пациентки с беременностью двойней, находящейся в программе ЭКО, на сроке 24–25 недель произошла внутриутробная гибель одного из плодов. Во всех трех случаях по данным патологоанатомического заключения у плодов были выявлены несовместимые с жизнью патологические состояния. Обращает внимание, что у одного из плодов была тяжелая форма геморрагической болезни новорожденных и у другого – кровоизлияние в боковые желудочки головного мозга.
Таблица 2. Осложнения беременности, способ родоразрешения и перинатальные исходы.
Table 2. Complications of pregnancy, route of delivery and perinatal outcomes.
|
Показатель Parameter |
Группа 1 Group 1 n = 217 |
2 группа Group 2 n = 113 |
p |
|
Гестационная артериальная гипертензия, n (%) Gestational arterial hypertension, n (%) |
8 (3,7) |
3 (2,7) |
≈ 1,0×10⁻⁴ |
|
Преэклампсия, n (%) Preeclampsia, n (%) |
23 (10,6) |
9 (7,9) |
> 0,05 |
|
Плацентарная недостаточность, n (%) lacental insufficiency, n (%) |
31 (14,3) |
16 (14,2) |
> 0,05 |
|
Риск реализации внутриутробной инфекции, n (%) Risk of intrauterine infection, n (%) |
26 (11,9%) |
7 (6,2) |
≈1,0×10⁻⁴ |
|
Микроальбуминурия, n (%) Microalbuminuria, n (%) |
64 (29,%) |
27 (23,9) |
≈1,0×10⁻⁴ |
|
Гестационный сахарный диабет, n (%) Gestational diabetes mellitus, n (%) |
20 (9,2) |
7 (6,2) |
> 0,05 |
|
Кровотечение в родах, n (%) Childbirth bleeding, n (%) |
0 |
1 (0,9) |
> 0,05 |
|
Гибельплода, n (%) Fetal death, n (%) |
0 |
3 (2,7) |
0,039 |
|
Кесарево сечение, n (%) Caesarean section, n (%): |
202 (93,1) |
107 (94,7) |
> 0,05 |
|
срочное кесарево сечение emergency caesarean section |
42 (20,8) |
23 (21,5) |
> 0,05 |
|
Недоношенность, n (%) Prematurity, n (%): |
37 (17,1) |
20 (17,7) |
> 0,05 |
|
недоношенность 1‑й степени / degree I |
25 (67,6) |
10 (50,0) |
> 0,05 |
|
недоношенность 2‑й степени / degree II |
6 (16,2) |
5 (25,0) |
> 0,05 |
|
недоношенность 3‑й степени / degree III |
4 (10,8) |
3 (15,0) |
> 0,05 |
|
недоношенность 4‑й степени / degree IV |
2 (5,4%) |
2 (10,0) |
> 0,05 |
|
Апгар на 1‑й минуте, балл, М ± SD Apgar at minute 1, score, M ± SD |
6,5 ± 1,0 |
6,2 ± 0,9 7,6 ± 1,0 |
> 0,05 |
|
Апгар на 5‑й минуте, балл, М ± SD Apgar at minute 5, score, M ± SD |
7,6 ± 0,8 |
7,6 ± 1,0 |
> 0,05 |
Подавляющее большинство женщин обеих групп были родоразрешены путем операции КС и более 20 % из них – экстренным КС (что еще больше увеличивало риски ВТЭО), но живым плодом с достаточно высокими показателями по шкале Апгар. В обеих группах количество недоношенных новорожденных было одинаковым, большинство из них с 1‑й и 2‑й степенью недоношенности. Все новорожденные были выписаны в удовлетворительном состоянии (табл. 2).
Обсуждение / Discussion
Беременность рассматривают в качестве модели физиологической гиперкоагуляции, основной целью которой является минимизация кровопотери в родах за счет объединения стремительно возрастающего кровотока матери и плода в плаценте. Однако целый ряд патологических состояний (перенесенные ранее ВТЭО, тромбофилии), метаболические нарушения и соматические заболевания (ожирение, сахарный диабет, гипертоническая болезнь, хроническая венозная болезнь), курение, длительная иммобилизация и другие факторы могут способствовать развитию ВТЭО, которые до настоящего времени остаются одной из ведущих причин материнской заболеваемости и смертности в развитых странах [2][9]. При ведении таких пациенток на этапе прегравидарной подготовки, также как и на всех этапах гестации, в родах и послеродовом периоде, перед врачом встают важные задачи: оценить риск развития ВТЭО с учетом степени риска, сроков беременности и в случае необходимости выбрать тактику тромбопрофилактики. Чтобы оценить риск ВТЭО у женщины в разные периоды (во время беременности, в родах и послеродовом периоде) используют целый ряд алгоритмов и шкал, позволяющих выявлять пациенток с повышенным риском; в России такая шкала представлена в текущих клинических рекомендациях [7][8]. Однако на момент сбора данных ни в одной медицинской карте пациенток, включенных в регистр «БЕРЕГ», мы не встретили балльного обоснования необходимости назначения лекарственных препаратов не только с целью тромбопрофилактики (пациентки группы 1), но и для профилактики акушерских осложнений беременности, которые с учетом особенностей патогенеза развития отдельных симптомов объединены в понятие «большие акушерские синдромы» (БАС), включающие преждевременные роды, преждевременный разрыв плодных оболочек, ПЭ, преждевременную отслойку нормально расположенной плаценты, задержку внутриутробного развития, маловесный плод, антенатальную гибель плода. Подход к объективизации тактики медикаментозной профилактики осложнений у пациенток с высоким риском их развития показал свою высокую информативность и применяется во всем мире [10].
Отмечено, что врожденная и приобретенная склонность к тромбозам может явиться причиной не только ВТЭО, но и материнской сосудистой мальперфузии плацентарного ложа из-за тромбоза спиральных сосудов – одного из механизмов развития БАС, что в свою очередь позволяет здесь рассматривать не только ассоциацию протромботического состояния гемостаза и развития БАС [11–13], но и обсудить у этих пациенток вопрос о необходимости тромбопрофилактики, в том числе медикаментозной. Показано, что наличие БАС повышает риск ВТЭО во время беременности и в послеродовом периоде, и факторами риска их развития, как считают исследователи, являются, кроме перечисленных в принятой шкале риска ВТЭО, отягощенный наследственный анамнез ранних тромбоэмболических событий, социальный статус, в частности, отсутствие работы у женщины, первая беременность и наличие ХАГ [14]. В свою очередь, сейчас в Российской Федерации экспертное сообщество по разработке клинических рекомендаций обосновало применение АСК в дозе 150 мг/сут в сроки от 16 до 36 недели беременности в целях профилактики развития БАС, в частности, ПЭ [15], но не для тромбопрофилактики [8][9].
Основными препаратами для тромбопрофилактики являются низкомолекулярные гепарины (НМГ) и нефракционированный гепарин (НФГ), которые не проникают через плаценту и имеют низкий риск воздействия на плод. Однако активно применяемый НФГ имеет некоторые минусы, в частности, для сохранения стабильной концентрации НФГ требуется постоянное внутривенное введение препарата в связи с коротким периодом полувыведения и плохой его всасываемостью из подкожно-жировой клетчатки. К тому же НФГ соединяется с белками плазмы крови, макрофагами и клетками эндотелия, что приводит к непредсказуемости ответа на введенную конкретную дозу лекарственного препарата. Также необходимо учитывать тот факт, что у различных серий НФГ может отличаться антитромботическая активность, что существенно как при использовании лечебных, так и профилактических доз. Степень гипокоагуляции под действием НФГ определяется величиной активированного частичного тромбопластинового времени в динамике и требует постоянного контроля [16–18].
Низкомолекулярные гепарины получают с помощью фракционирования или деполимеризации НФГ. Преимущественными характеристиками препаратов этой группы является то, что они обладают более выраженной анти-Ха активностью, сильнее угнетают выделение фактора фон Виллебранда и препятствуют его проагрегантной активности, способствуют выбросу ингибитора пути тканевого фактора, у которого есть антикоагулянтные свойства. Важным также является то, что НМГ имеют длительный период полувыведения и хорошо всасываются при подкожном введении, что дает возможность вводить их 1–2 раза в день. Необходимо подчеркнуть, что НМГ хуже соединяются с белками крови и клетками крови и меньше нейтрализуются тромбоцитарным фактором IV, который выделяется при агрегации тромбоцитов, вследствие чего крайне редко вызывают тромбоцитопению и гепарин-индуцированные тромбозы. При введении НМГ проводят оценку анти-Ха активности не для титрования дозы, а только для того, чтобы определить наличие препарата и его лечебное и профилактическое действие. В настоящее время рекомендуют проводить измерение анти-Ха активности с валидной тест-системой у пациентов с массой тела менее 50 кг или более 90 кг, с хронической болезнью почек при скорости клубочковой фильтрации менее 50 мл/мин, а также при клинической неэффективности НМГ и заданном уровне анти-Ха активности в профилактических дозах от 0,2 до 0,6 МЕ/мл [18]. Беременным с механическими протезами клапанов сердца может быть назначен варфарин, но вследствие его эмбриотоксичности необходимо учитывать дозу препарата (нужен контроль международного нормализованного отношения) и сроки беременности [19]. Другие пероральные антикоагулянты беременным противопоказаны, так как препараты могут проникать через плаценту, и их репродуктивные риски на данный момент неизвестны.
В нашем исследовании дозы надропарина кальция были профилактическими и соответствовали рекомендуемым. Полученные нами данные идентичны результатам мультицентрового исследования Highlow, в котором женщины, имеющие ВТЭО в анамнезе и получавшие НМГ в дозах, адаптированных по массе тела в дородовом и послеродовом периодах, статистически значимо имели более низкий риск повторных ВТЭО в сравнении с пациентками, получавшими низкие фиксированные дозы НГМ [20]. Это подтверждает вывод о том, что для профилактики ВТЭО у беременных высокого риска достаточно использования низких фиксированных доз НМГ и, в частности, у пациенток высокого риска при массе тела менее 100 кг достаточно применять 0,3 мл (2850 МЕ) надропарина кальция [20]. У женщин из регистра «БЕРЕГ» отсутствовали эпизоды ВТЭО, что подтвердило правомерность применения фиксированных дозировок НМГ, ранее продемонстрированных в исследовании Highlow.
На основании результатов метаанализа 15 исследований, в которые были включены 2795 беременных с высоким риском развития БАС и получавших лечение НМГ, было отмечено снижение развития ПЭ (отношение шансов (ОШ) = 0,62; 95 % доверительный интервал (ДИ) = 0,43–0,90; р = 0,010), малого гестационного возраста (ОШ = 0,61; 95 % ДИ = 0,44–0,85; р = 0,003) и перинатальной смерти (ОШ = 0,49; 95 % ДИ = 0,25–0,94; р = 0,030). Когда же из них были проанализированы данные 6 рандомизированных контролируемых исследований, в которых 920 женщин получали в дополнение к НМГ низкие дозы АСК, оказалось, что комбинированное лечение по сравнению с монотерапией низкими дозами АСК было более эффективным (ОШ = 0,62; 95% ДИ = 0,41–0,95; р = 0,030). В целом, нежелательные явления в группах наблюдения не были серьезными и существенно не различались [21].
В проведенном нами исследовании 113 пациенток получали монотерапию АСК в дозе 150 мг/сут, что на основе механизма действия препарата (через необратимое ингибирование циклооксигеназы 1 тромбоцитов, угнетение синтеза тромбоксана А2, обеспечивая, таким образом, длительный дезагрегантный эффект) обосновывает применение АСК с целью профилактики БАС [12][15]. В нашем исследовании случаев ВТЭО и материнской смертности ни в одной из групп наблюдения, несмотря на экстремально высокий риск их развития у большего числа пациенток, не было зарегистрировано. Однако, у 4 женщин, получавших монотерапию АСК, по сравнению с пациентками на комбинированной терапии надропарином с АСК, возникли такие серьезные осложнения как кровотечение в родах (n = 1) и гибель плода (n = 3). При этом у двух из плодов по результатам патологоанатомического вскрытия отмечались тяжелые геморрагические осложнения. Напрямую связать эти осложнения с приемом АСК мы не можем вследствие небольшого числа наблюдений, однако полученные данные дают основание для дальнейшего изучения влияния антикоагулянтов и дезагрегантов, используемых для тромбопрофилактики и при БАС у беременных высокого риска.
С результатами нашего исследования согласуются данные недавно опубликованного метаанализа, включающего 11 исследований (n = 1672), в которых оценивали влияние различных схем медикаментозной профилактики БАС и ВТЭО у женщин с персистирующими антифосфолипидными антителами. Результаты метаанализа продемонстрировали отсутствие случаев ВТЭО и артериальных тромбозов, тромбоцитопении, аллергических реакций и врожденных пороков развития у детей [22]. Вместе с тем было показано, что АСК по сравнению с плацебо с очень низкой степенью достоверности влияет на частоту живорождения, потерь беременности, преждевременных родов живым ребенком, внутриутробной задержки роста плода или неблагоприятных событий у ребенка, риск ПЭ (одно исследование, 40 женщин; ОШ = 0,94; 95 % ДИ = 0,71–1,2) и частоту кровотечения у матери (ОШ = 1,29; 95 % ДИ = 0,60–2,77). При анализе комбинированной терапии НМГ с АСК (5 исследований, 1295 женщин) с низкой степенью достоверности отмечено увеличение количества живорождений (ОШ = 1,27; 95 % ДИ = 1,09–1,49), но убедительных данных по влиянию такой терапии на риск ПЭ, преждевременных родов живым ребенком или внутриутробной задержки роста плода по сравнению с монотерапией АСК вследствие небольшого числа наблюдений и широкого 95 % ДИ, как считают исследователи, не получено. По этой же причине с уверенностью считать, что комбинированная терапия НМГ с АСК по сравнению с монотерапией АСК оказывает влияние на риск кровотечения у матери, не представляется возможным (ОШ = 1,65; 95 % ДИ = 0,19–14,03; одно исследование, 31 женщина) [22].
Заключение / Conclusion
Таким образом, результаты регистра «БЕРЕГ» по оценке эффективности и безопасности тромбопрофилактики препаратом Фраксипарин в фиксированной дозе 0,3 мл у беременных высокого риска в реальной клинической практике продемонстрировали эффективность и безопасность его использования, отсутствие случаев ВТЭО, кровотечений, материнской смерти, аллергических реакций, тромбоцитопении и гепарин-индуцированных тромбозов. Вместе с тем обращает внимание существовавшая ранее недостаточная информированность врачей о необходимости использования шкал по оценке риска развития ВТЭО для объективизации последующей тактики медикаментозного лечения, в связи с чем, на наш взгляд, были произвольно выбраны схемы профилактического воздействия – комбинированная терапия НМГ в сочетании с АСК и монотерапия АСК. При этом последняя, ввиду отсутствия доказанности, не может быть рекомендована в качестве профилактики ВТЭО. Несмотря на сопоставимость групп наблюдения по основным клинико-лабораторным характеристикам, только в группе пациенток, получавших монотерапию АСК, были зафиксированы такие осложнения как кровотечение в родах и гибель плода. Безусловно, это не дает оснований для связи развития этих осложнений с приемом АСК, но заставляет задуматься о корректности проводимой профилактики ВТЭО у беременных высокого риска и продолжить наблюдения в аспекте оценки ее эффективности, безопасности и согласованности с текущими одобренными клиническими рекомендациями.
Список литературы
1. Стрюк Р.И., Бернс С.А., Филиппова М.П. и др. Сердечно-сосудистые заболевания и ассоциированные с ними коморбидные состояния как факторы, определяющие неблагоприятные перинатальные исходы при беременности – анализ результатов регистра беременных «БЕРЕГ». Терапевтический архив. 2018;(1):9–16.
2. Saving Lives, Improving Mothers’ Care: Lessons learned to inform maternity care from the UK and Ireland Confidential Enquiries into Maternal Deaths and Morbidity 2014–16. Eds. K. Knight, K. Bunch, D. Tuffnell et al. National Perinatal Epidemiology Unit: University of Oxford, 2018. 104 p.
3. Petersen E.E., Davis N.L., Goodman D. et al. Vital signs: pregnancy-related deaths, United States, 2011–2015, and strategies for prevention, 13 States, 2013–2017. Morb Mortal Wkly Rep. 2019;68(18):423. https://doi.org/10.15585/mmwr.mm6818e1.
4. O'Shaughnessy F., O'Reilly D., Ní Áinle F. Current opinion and emerging trends on the treatment, diagnosis, and prevention of pregnancy-associated venous thromboembolic disease: a review. Transl Res. 2020;225:20–32. https://doi.org/10.1016/j.trsl.2020.06.004.
5. Здравоохранение в России: статистический сборник. Федеральная служба государственной статистики, 2023. 179 с. Режим доступа: https://youthlib.mirea.ru/ru/resource/6229. [Дата обращения: 21.05.2025].
6. McColl M.D., Ellison J., Greer I.A. et al. Prevalence of the post-thrombotic syndrome in young women with previous venous thromboembolism. Br J Haematol. 2000;108(2):272–4. https://doi.org/10.1046/j.1365-2141.2000.01877.x.
7. Клинические рекомендации – Венозные осложнения во время беременности и послеродовом периоде. Акушерская тромбоэмболия – 2022-2023-2024 (14.02.2022). М.: Министерство здравоохранения Российской Федерации, 2022. 66 с. Режим доступа: http://disuria.ru/_ld/11/1153_kr22O22MZ.pdf. [Дата обращения: 21.05.2025].
8. Клинические рекомендации – Нормальная беременность – 2023-2024-2025 (15.02.2024). М.: Министерство здравоохранения Российской Федерации, 2024. 58 с. Режим доступа: https://srb-48.gosuslugi.ru/netcat_files/44/136/KR_Normal_naya_beremennost_.pdf. [Дата обращения: 21.05.2025].
9. Say L., Chou D., Gemmill A., Tunçalp Ö. et al. Global causes of maternal death: a WHO systematic analysis. Lancet Glob Health. 2014;2(6):e323–33. https://doi.org/10.1016/S2214-109X(14)70227-X10.
10. Хизроева Д.Х., Бабаева Н.Н., Макацария Н.А. и др. Клиническое значение гемостазиологического скрининга на тромбофилию у беременных с тромбозами в анамнезе. Акушерство, Гинекология и Репродукция. 2022;16(5):528–40. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2022.361.
11. Ковалев В.В., Кудрявцева Е.В. Молекулярно-генетические девиации и акушерская патология. Акушерство и гинекология. 2020;(1):26–32.
12. Zur R.L., Kingdom J.C., Parks W.T., Hobson S.R. The placental basis of fetal growth restriction. Obstet Gynecol Clin North Am. 2020;47(1):81–98. https://doi.org/10.1016/j.ogc.2019.10.008.
13. Ходжаева З.С., Холин А.М., Чулков В.С., Муминова К.Т. Ацетилсалициловая кислота в профилактике преэклампсии и ассоциированных акушерских и перинатальных осложнений. Акушерство и гинекология. 2018;(8):12–8.
14. Долгушина В.Ф., Сюндюкова Е.Г., Чулков В.С., Униговская К.А. Риски венозных тромбоэмболических событий при больших акушерских синдромах. Доктор.Ру. 2023;22(1):33–9. https://doi.org/10.31550/1727-2378-2023-22-1-33-39.
15. Клинические рекомендации – Преэклампсия. Эклампсия. Отеки, протеинурия и гипертензивные расстройства во время беременности, в родах и послеродовом периоде – 2024-2025-2026 (05.09.2024). М.: Министерство здравоохранения Российской Федерации, 2024. 53 с. Режим доступа: http://disuria.ru/_ld/15/1564_kr24O10O16MZ.pdf. [Дата обращения: 21.05.2025].
16. Hirsh J., Anand S.S., Halperin J.L. et al. Guide to anticoagulant therapy: heparin. A Statement for healthcare professionals from the American Heart Association. Circulation. 2001;103(24):2994–3018. https://doi.org/10.1161/01.cir.103.24.2994.
17. Antman E.M., Handin R. Low-molecular-weight heparins. An intriguing new twist with profound implications. Circulation. 1998;98(4):287–9. https://doi.org/10.1161/01.cir.98.4.287.
18. Крикунова О.В., Стрюк Р.И. Эноксапарин в алгоритме ведения пациентов с острым коронарным синдромом. Рациональная фармакотерапия в кардиологии. 2018;14(1):131–6. https://doi.org/10.20996/1819-6446-2018-14-1-131-136.
19. Иртюга О.Б., Шмаков Р.Г., Вавилова Т.В. и др. Дискуссионные вопросы применения антикоагулянтов в профилактике венозных тромбоэмболических осложнений у беременных с сердечно-сосудистыми и системными заболеваниями. Резолюция Совета экспертов. Российский кардиологический журнал. 2023;28(4):5421. https://doi.org/10.15829/1560-4071-2023-5421.
20. Bistervels I.M., Buchmuller A., Wiegers H.M.G. et al. Intermediate-dose versus low-dose low-molecular-weight heparin in pregnant and post-partum women with a history of venous thromboembolism (Highlow study): an open label, multicentre, randomised, controlled trial. Lancet. 2022;400(10365):1777–87. https://doi.org/10.1016/S0140-6736(22)02128-6.
21. Cruz-Lemini M., Vazquez J.C., Ullmo J., Llurba E. Low-molecular-weight heparin for prevention of preeclampsia and other placenta-mediated complications: a systematic review and meta-analysis. Am J Obstet Gynecol. 2022;226(2S):S1126–S1144.e17. https://doi.org/10.1016/j.ajog.2020.11.006.
22. Hamulyák E.N., Scheres L.J., Marijnen M.C. et al. Aspirin or heparin or both for improving pregnancy outcomes in women with persistent antiphospholipid antibodies and recurrent pregnancy loss. Cochrane Database Syst Rev. 2020;5(5):CD012852. https://doi.org/10.1002/14651858.CD012852.pub2.
Об авторах
Р. И. СтрюкРоссия
Стрюк Раиса Ивановна - д.м.н., проф.
127006 Москва, Долгоруковская ул., д. 4
О. В. Крикунова
Россия
Крикунова Ольга Витальевна - к.м.н.
127006 Москва, Долгоруковская ул., д. 4
Э. Э. Локшина
Россия
Локшина Эвелина Эдуардовна - к.м.н., проф.
127006 Москва, Долгоруковская ул., д. 4
Т. А. Гомова
Россия
Гомова Татьяна Александровна - к.м.н.
300053 Тула, ул. Яблочкова, д. 1-а
Е. Е. Федотова
Россия
Федотова Елена Евгеньевна
300053 Тула, ул. Яблочкова, д. 1-а
Что уже известно об этой теме?
► Причины повышенного тромбообразования крайне разнообразны.
► Наступление беременности значительно повышает вероятность развития венозных тромбоэмболических осложнений (ВТЭО), особенно при наличии у женщин наследственных или приобретенных заболеваний, включая тромбофилические состояния.
► Для уменьшения частоты развития ВТЭО требуются настороженность и своевременная оценка существующих факторов риска у беременных.
Что нового дает статья?
► Данные регистра «БЕРЕГ» представляют картину реальной клинической практики по оценке риска ВТЭО у беременных.
Как это может повлиять на клиническую практику в обозримом будущем?
► Правильная оценка риска ВТЭО и своевременное начало тромбопрофилактики обеспечивают надежную профилактику осложнений во время беременности и послеродовом периоде.
► Выводы из исследования позволят лучше использовать актуальные клинические рекомендации «Венозные осложнения во время беременности и послеродовом периоде. Акушерская тромбоэмболия».
Рецензия
Для цитирования:
Стрюк Р.И., Крикунова О.В., Локшина Э.Э., Гомова Т.А., Федотова Е.Е. Эффективность и безопасность профилактики венозных тромбоэмболических осложнений у беременных высокого риска: анализ результатов регистра беременных «БЕРЕГ». Акушерство, Гинекология и Репродукция. 2025;19(5):705-715. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.652
For citation:
Stryuk R.I., Krikunova O.V., Lokshina E.E., Gomova T.A., Fedotova E.E. Efficacy and safety for preventing of venous thromboembolic complications in high-risk pregnant women: results of the «BEREG» pregnant women registry. Obstetrics, Gynecology and Reproduction. 2025;19(5):705-715. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.652

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.











































