"Акушерство, Гинекология и Репродукция" (АГР), является научно-практическим рецензируемым журналом для акушеров-гинекологов и специалистов в области женского здоровья. В числе приоритетов и целей издания - развитие научно-информационной поддержки и укрепление связей в «профессиональном сообществе», помощь в формировании новых и перспективных исследований в области акушерства и гинекологии. Также журнал «Акушерство, Гинекология и Репродукция» способствует непрерывному медицинскому образованию (НМО) (continue medical education, CME) практикующих специалистов в области женского здоровья - акушеров, гинекологов, специалистов, занимающихся проблемами экстракорпорального оплодотворения (ЭКО) и вспомогательными репродуктивными технологиями (ВРТ).
"Акушерство, Гинекология и Репродукция" основан в 2007 г.
Импакт-фактор Российского Индекса Научного Цитирования (РИНЦ) (Russian Science Citation Index, RSCI) в 2015 г. – один из самых высоких из журналов в сфере акушерства, гинекологии, перинатологии, репродукции человека и проблем женского здоровья. Двухлетний импакт-фактор РИНЦ в 2013 году составил 0,509; в 2014 – 0,810; в 2015 – 0,976.
В журнале публикуются научные статьи с результатами клинических и экспериментальных исследований, обзоры литературы по актуальным проблемам в сфере акушерства, гинекологии и репродукции человека. Часть публикаций посвящены непрерывному медицинскому образованию (НМО) и историческим аспектам акушерства и гинекологии. Научные статьи - результаты собственных исследований и обзоры литературы - публикуются после обязательного предварительного рецензирования..
Языки журнала: русский и английский.
Периодичность издания: 6 номеров в год.
Распространяется на условиях Creative Commons Attribution 4.0 License: полнотекстовые материалы доступны в открытом доступе.
Распространение печатной версии: Россия, страны ЕвРаЗэс (Беларусь, Казахстан, Кыргызстан, Таджикистан, Узбекистан, Армения, Молдова), Украина, Грузия.
В редакционную коллегию журнала «Акушерство, гинекология и репродукция» входят ведущие специалисты из России, Австрии, Великобритании, Израиля, США, Хорватии, Армении, Украины, Грузии и Узбекистана.
Редакционная коллегия АГР поддерживают политику, направленную на соблюдение всех принципов издательской этики. Этические правила и нормы соответствуют принятым ведущими международными научными издательствами.
Все поступившие материалы проходят обязательную процедуру двойного слепого рецензирования.
Свидетельство о регистрации СМИ: ПИ №ФС77-39270.
ISSN 2313-7347 (Print)
ISSN 2500-3194 (Online)
Журнал «Акушерство, Гинекология и Репродукция» включен в «Перечень ведущих рецензируемых научных журналов и изданий ВАК», в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученых степеней доктора и кандидата наук, присутствует в Российской универсальной научной электронной библиотеке (РУНЭБ) elibrary.ru и входит в базу данных Российского индекса научного цитирования (РИНЦ), реферируется Всероссийским институтом научной и технической информации Российской академии наук (ВИНИТИ РАН) и содержится в справочной системе по периодическим и продолжающимся изданиям “Ulrich’s Periodicals Directory”.
Текущий выпуск
РЕДАКЦИОННАЯ СТАТЬЯ
В этом номере основное внимание уделяется переходу от традиционных подходов к персонализированной, предиктивной и превентивной медицине, освещаются исследования, демонстрирующие высокую диагностическую и прогностическую ценность новых биомаркеров (таких как соотношение sFlt-1/PlGF, miRNA, VEGF) для раннего выявления преэклампсии, риска преждевременных родов и рецидива эндометриоза. Рассматриваются современные хирургические тактики, включая органосохраняющий гемостаз и инновационные методы периоперационной аналгезии, соответствующие принципам ускоренного восстановления после операции (ERAS). Анализируются актуальные данные по нутрициальной поддержке (омега-3 ПНЖК), профилактике тромбоэмболических осложнений, роли микронутриентов в фертильности и влиянию эндокринных дизрапторов на репродуктивное здоровье. Обзор также включает разбор клинических случаев и исторических аспектов, что в совокупности формирует целостное представление о современных решениях, трансформирующих рутинную практику врача.
ОРИГИНАЛЬНЫЕ СТАТЬИ
Что уже известно об этой теме?
► Во время беременности у пациенток с экстрагенитальными заболеваниями повышается риск развития преэклампсии (ПЭ).
► Плацентарный фактор роста (PlGF) и растворимая fms-подобная тирозинкиназа-1 (sFlt-1) играют важную роль в развитии ПЭ, так как гиперпродукция одного фактора блокирует действия другого фактора, что приводит к развитию клинической симптоматики.
Что нового дает статья?
► Впервые в мире показана высокая значимость биомаркеров в диагностике ранней ПЭ у беременных с наличием экстрагенитальных заболеваний: сахарного диабета 1-го и 2-го типа, хронической артериальной гипертензии, хронического пиелонефрита, хронического гломерулонефрита.
► Определена точка отсечения соотношения sFlt-1/PlGF – 11,8, т. е. при коэффициенте выше этого значения ПЭ развивалась у большинства пациенток с экстрагенитальными заболеваниями.
► Максимальная глубина прогноза риска возникновения ПЭ составляет 6 недель.
Как это может повлиять на клиническую практику в обозримом будущем?
► Включение в рутинную практику исследований биомаркеров sFlt-1 и PlGF и их соотношения позволит более точно прогнозировать наступление ПЭ, а также вовремя оказывать помощь беременным.
Введение. Преэклампсия (ПЭ) остается одной из наиболее актуальных проблем современного акушерства, являясь ведущей причиной материнской и перинатальной заболеваемости и смертности. Это мультисистемное расстройство, возникающее после 20 недель беременности и характеризующееся артериальной гипертензией в сочетании с протеинурией и/или полиорганной дисфункцией.
Цель: определить содержание биомаркеров – растворимой fms-подобной тирозинкиназы-1 (англ. soluble fms-like tyrosine kinase-1, sFlt-1), плацентарного фактора роста (англ. placental growth factor, PlGF) и их соотношение (sFlt-1/PlGF) у пациенток с экстрагенитальными заболеваниями для диагностики ранней и поздней ПЭ.
Материалы и методы. В проспективное исследование включены 439 пациенток с экстрагенитальными заболеваниями (сахарным диабетом 1-го и 2-го типа, хронической артериальной гипертензией, хроническим пиелонефритом, хроническим гломерулонефритом), среди которых были выделены подгруппы с ПЭ (n = 94) и без ПЭ (n = 345). Обследование пациенток проводили на всем протяжении беременности, начиная с 12 недель. Определение PlGF и sFlt-1 в сыворотке крови выполняли с помощью электрохемилюминесцентных диагностических тестов на автоматических анализаторах с последующим расчетом соотношения sFlt-1/PlGF для каждого образца сыворотки. С целью определения прогностической ценности соотношения sFlt1/PlGF для выявления ПЭ выполнялось построение ROC-кривых с последующей оценкой качества прогноза.
Результаты. Сроки манифестации ранней и поздней ПЭ имели различную динамику ангиогенных биомаркеров. При ранней ПЭ статистически значимое изменение уровня маркера sFlt-1 (р = 0,001) и коэффициента sFlt-1/PlGF (р = 0,003) фиксировали уже с 22–24 недель по сравнению с предыдущими периодами гестации. При поздней ПЭ изменения были менее выражены и статистически значимы лишь эпизодически на сроке гестации 25–27 недель (р = 0,027). В прогнозе развития ПЭ изменения биомаркеров являлись ранними предикторами, предшествуя родам за 6 недель. Для пациенток с экстрагенитальной патологией установлена пониженная точка отсечения соотношения sFlt-1/PlGF – 11,8.
Заключение. Проведенное исследование позволяет сделать вывод о высокой диагностической значимости определения ангиогенных биомаркеров у пациенток с экстрагенитальной патологией в сроки конца II – начала III триместра гестации (28–33 недели). Анализ диагностической ценности биомаркеров, основанный на построении ROC-кривых, выявил следующую иерархию по их прогностической эффективности: наивысшая прогностическая ценность характерна для соотношения sFlt-1/PlGF, которое превосходит по своим показателям изолированное определение sFlt-1 и PlGF. Ключевые показатели (чувствительность, специфичность и площадь под ROC-кривой – AUC) подтверждают, что соотношение sFlt-1/PlGF является наиболее эффективным предиктором по сравнению с изолированным измерением значений sFlt-1 и PlGF в диагностике ПЭ в данной когорте пациенток. Оптимальным пороговым значением для соотношения sFlt-1/PlGF является 11,8. Установлено, что максимальная глубина прогнозирования риска развития ПЭ с использованием данного критерия составляет 6 недель, что определяет его высокую клиническую ценность для своевременного формирования групп риска и назначения превентивных мероприятий.
Что уже известно об этой теме?
► Эндометриоз – хроническое прогрессирующее заболевание с рецидивирующим течением.
► Вероятность рецидива эндометриоза яичников после оперативного лечения остается высокой, достигая практически 50 % через 5 лет после операции.
► Существующие методы прогнозирования рецидива позволяют выявить больных с высоким риском рецидива эндометриоза в ближайшие несколько лет, но они не уточняют сроки его развития у конкретной женщины.
Что нового дает статья?
► Представлена количественная оценка значимости качественных предикторов развития рецидива эндометриоза яичников по величине относительного риска.
► Разработан индекс риска RI, учитывающий неблагоприятное воздействие «n» факторов риска на организм в течение «х» лет, который позволяет с надежностью до 80 % прогнозировать конкретные сроки рецидива эндометриоза после операции в течение ближайших 4 лет.
Как это может повлиять на клиническую практику в обозримом будущем?
► Представленный метод прогнозирования сроков рецидива эндометриоза позволяет синхронизировать повышение активности профилактических мер с периодом максимального риска развития заболевания.
Введение. Эндометриоз поражает около 10 % женщин репродуктивного возраста и характеризуется хроническим рецидивирующим течением. Вероятность рецидива эндометриоза после хирургического лечения заболевания остается очень высокой, что диктует необходимость разработки надежных персонализированных подходов к выбору оптимальных методов профилактики рецидивов, основанных на прогнозе риска их развития.
Цель: разработать персонализированный подход к оценке вероятности развития и меры профилактики рецидива эндометриоза яичников после хирургического лечения.
Материалы и методы. В проспективное исследование включены 148 пациенток с эндометриомой одного яичника после хирургического лечения; в последующем пациентки были разделены на 2 группы. Основная группа состояла из 59 пациенток с рецидивом эндометриоза, контрольная группа включала 89 пациенток без рецидива. Для построения модели прогнозирования рецидива эндометриоза использовались показатели, наличие которых с позиций доказательной медицины категории А, В и С увеличивают риск развития эндометриоза после операции. Приверженность лечению оценивалась с помощью опросника «КОП-25», уровень стресса – по методике Холмса-Раге. При построении модели использовался расчет относительного риска (англ. relative risk, RR).
Результаты. Проведена количественная оценка значимости качественных предикторов развития рецидива эндометриоза по величине RR. Его значение при наличии курения составило 2,4, стресса – 2,0, в молодом возрасте (менее 25 лет) – 2,4, при приверженности лечению – 3,2, неполном удаления очагов – 3,1, а также зависело от индекса массы тела (RR = 1,6). В течение первого года после операции рецидив произошел у 18 больных на фоне максимального числа факторов риска (8,4 ± 0,5). В течение последующего года было выявлено 13 новых случаев рецидива при наличии 5,3 ± 0,4 факторов риска. В ходе третьего года наблюдения число рецидивов увеличилось на 12 случаев, а количество факторов риска у больных не превысило 4,6 ± 0,2. На основании полученных данных для разработки количественного подхода к оценке конкретных сроков развития рецидива в течение 4 лет был введен индекс риска (англ. risk index, RI) = n×х (усл. ед.), учитывающий неблагоприятное воздействие «n» факторов риска на организм в течение «х» лет.
Заключение. При персонализированном подходе к оценке риска развития рецидива эндометриоза значимость качественных предикторов с позиций доказательной медицины требует количественного уточнения. Разработанный индекс RI позволяет с надежностью более 80 % прогнозировать конкретные сроки рецидива. Предложенный метод позволяет синхронизировать повышение активности профилактических мер с периодом максимального риска развития заболевания.
Что уже известно об этой теме?
► Частота акушерского кровотечения увеличивается при оперативном родоразрешении в 5 и более раз. Методы хирургического гемостаза включают перевязку трех пар маточных сосудов, наложение компрессионных швов и их комбинацию.
► Ближайшие последствия органосохраняющих операций включают субинволюцию матки, эндометрит, спаечный процесс и некроз матки. Отдаленные последствия включают развитие внутриматочных синехий, аменореи.
► Частота реканализации маточных артерий после двухсторонней перевязки не превышает 40 %. При перевязке внутренней подвздошной артерии отмечено снижение показателей овариального резерва.
Что нового дает статья?
► У пациенток, перенесших патологическую кровопотерю при кесаревом сечении и перевязку трех пар маточных сосудов, наблюдается изменение кровоснабжения в маточных артериях и внутрияичниковом кровотоке. Отмечено уменьшение диаметра маточных артерий у данной группы пациенток до 2,18 ± 0,02 мм и 2,09 ± 0,03 мм, в среднем на 10,3 %.
► Проведено изучение влияния органосохраняющих операций на состояние репродуктивной системы в дальнейшем. Расчет объемного кровотока в маточных артериях и индекса артериальной перфузии матки (ИАП) показал снижение васкуляризации матки. Объемный кровоток в маточных артериях в основной группе по сравнению с контрольной группой был ниже в правой маточной артерии на 18,2 %, в левой маточной артерии – на 22,6 %. ИАП матки в основной группе составил 0,90 ± 0,02 с–1, что значимо ниже (р < 0,001), чем в контрольной группе (1,29 ± 0,02 с–1).
► В маточных артериях и внутрияичниковом кровотоке выявлен высокорезистентный кровоток. Пульсационный индекс в правой маточной артерии был повышен до 3,67 ± 0,04, в левой маточной артерии – до 3,84 ± 0,04, показатели индекса резистентности были выше, чем в контроле и составили справа 0,92 ± 0,01 и слева 0,90 ± 0,02.
Как это может повлиять на клиническую практику в обозримом будущем?
► В дальнейшем у данной категории пациенток возможно развитие аномальных маточных кровотечений в виде нарушений менструальной функции от олигоменореи до аменореи.
► Высокорезистентный кровоток во внутрияичниковых артериях может привести к формированию гипергонадотропной яичниковой недостаточности, связанной со снижением выработки стероидных гормонов яичника, что в свою очередь приведет к компенсаторному повышению гонадотропных гормонов – фолликулостимулирующего гормона и лютеинизирующего гормона.
► При своевременном выявлении высокорезистентного кровотока в маточных артериях и внутрияичниковом кровотоке возможно проведение коррекции ановуляции и недостаточности лютеиновой фазы. Данные вмешательства, возможно, приведут к вынашиванию беременности.
Введение. Для остановки акушерских кровотечений применяются хирургические органосохраняющие методы, одним из которых является перевязка маточных сосудов на трех уровнях. Эффективность органосохраняющих методов составляет до 94 %. Функция любого органа зависит от адекватного кровоснабжения, в связи с чем состояние репродуктивной функции женщин, перенесших органосохраняющие операции, является объектом дальнейшего изучения.
Цель: изучение кровотока в матке и яичниках у женщин после перевязки трех пар маточных сосудов при патологической кровопотере в родах.
Материалы и методы. Проведено проспективное контролируемое исследование. Основную группу составили пациентки (n = 41), которым произведена перевязка трех пар маточных сосудов при патологической кровопотере во время проведения оперативного родоразрешения, контрольную – 25 женщин после кесарева сечения без патологической кровопотери и перевязки трех пар маточных сосудов. Проводилось доплерометрическое исследование маточных артерий и центрального кровотока яичника с изучением уголнезависимых параметров – пульсационного индекса (ПИ), индекса резистентности (ИР). Производился расчет объемного кровотока в маточных артериях и индекса артериальной перфузии матки.
Результаты. Средний возраст пациенток в основной группе составил 30,00 ± 0,84 лет, в контрольной – 25,96 ± 0,99 лет (р = 0,003). Объем кровопотери в основной группе был в 2,7 раз больше, чем контрольной (р < 0,001). Изучение ПИ и ИР в маточных артериях показало высокорезистентный кровоток, отмечено достоверное повышение ПИ в 1,6 и ИР 1,4 раза в сравнении с контрольной группой (р < 0,001). Расчет объемного кровотока в маточных артериях у пациенток основной группы показал снижение на 18,2–22,6 % в сравнении с контрольной. Данный факт привел к снижению индекса артериальной перфузии матки в группе пациенток, перенесших органосохраняющие операции при патологической кровопотере, на 30,2 %. Показатели ПИ и ИР во внутрияичниковом кровотоке показали повышение в 2,0 и 1,4 раза соответственно (р < 0,05).
Заключение. Выявленный высокорезистентный кровоток в матке и яичниках может приводить в дальнейшем к формированию ановуляторного цикла в связи с нарушением органной гемодинамики, что может привести к развитию яичниковой недостаточности.
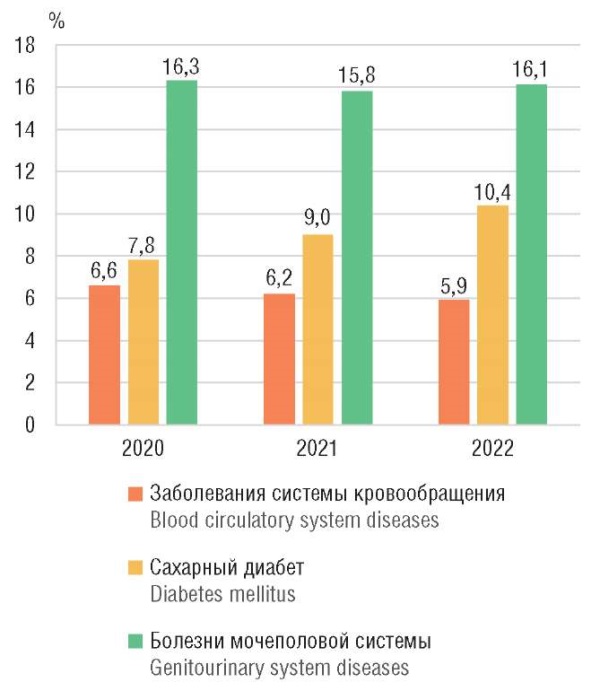
Что уже известно об этой теме?
► Длинноцепочечные омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК) абсолютно незаменимы для нормального функционирования репродукции, физиологического течения беременности, тормозят старение и фиброзирование тканей почек и печени, миокарда, зрения и мозга, кожи.
► Эйкозапентаеновая кислота (ЭПК) и докозагексаеновая кислота (ДГК) – ключевые формы ω3-ПНЖК, важные для физиологического окончания воспаления и для нейропротекции.
► ДГК способствуют синтезу антифибротических метаболитов, защищающих ткань почек при токсикозе беременных, препятствуя развитию послеродовой депрессии. ω3-ПНЖК являются тонкой модуляцией биосинтеза простагландинов (PG) и, в частности, простагландинов PGE2 и PGF2α. Избыточная активность простагандинов PGE2 и PGF2α, стимулируя приток нейтрофилов и продукцию цитокинов, экспрессию циклооксигеназы-2 (тем самым усиливая свою собственную продукцию), отрицательно сказывается на продолжительности вынашивания.
Что нового дает статья?
► Впервые проведено высокоточное хроматографическое определение жирнокислотного состава 10 препаратов, оценены 55 химических соединений – 55 метаболитов жирных кислот,
► Определено общее содержание ω3, ω6, ω7, ω9, ω11-ПНЖК, ЭПК, ДГК, ЭПК+ДГК.
Как это может повлиять на клиническую практику в обозримом будущем?
► Выявлены препараты с высокой степенью стандартизации по ω3-ПНЖК (Омакор, Фемибион Наталкер-2 и др.). Однако препарат Омакор фактически не рекомендуется для беременных; назначать Омакор беременным следует с осторожностью, только после тщательной оценки соотношения риска и пользы.
► Врачи не должны быть подвержены терминологической путанице, при которой все препараты ω3-ПНЖК называются «рыбий жир»: ω3-ПНЖК могут изготовляться вообще без использования экстрактов жира рыб, с использованием, например, экстрактов жира морских млекопитающих, экстрактов водорослей, льняного масла, синтетических форм ω3-ПНЖК.
► Поддержка беременных посредством стандартизированных препаратов ω3-ПНЖК способствует нормальной продолжительности беременности, профилактирует послеродовую депрессию и улучшает развитие зрения, мозга плода, снижает риск аллергических заболеваний новорожденого.
Введение. Омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК), модулируя сложным образом обмен эйкозаноидов (в том числе простагландинов, липоксинов и лейкотриенов) и докозаноидов (нейропротектинов, резолвинов, маресинов), являются важным фактором репродуктивного и соматического здоровья женщин.
Цель: сравнить образцы ω3-ПНЖК по степени стандартизации состава по эйкозапентаеновой (ЭПК) ω3-ПНЖК и докозагексаеновой (ДГК) ω3-ПНЖК, оценить степень очистки от жирнокислотных примесей.
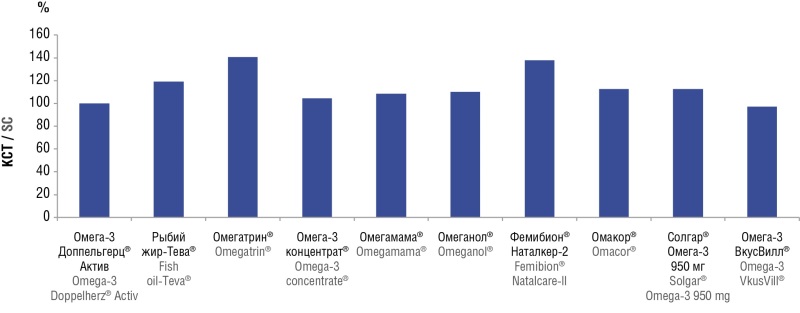
Материалы и методы. В работе представлены результаты хроматографического анализа 10 препаратов ω3-ПНЖК.
Результаты. Исследование позволило выявить показатели состава экстрактов ω3-ПНЖК, посредством которых возможно отличать фармацевтически стандартизированные препараты ω3-ПНЖК (Омакор, Фемибион Наталкер-2 и др.) от менее стандартизированных препаратов (Омеганол, Омегамама и др.).
Заключение. Более стандартизированный препарат Фемибион Наталкер-2 эффективен и безопасен для поддержки репродуктивной функции во время беременности и для улучшения неврологического развития детей. Омакор – высоко стандартизированный препарат, но не имеет официального разрешения к применению у беременных.
Что уже известно об этой теме?
► Становление «Биобанкирования», нового направления биомедицины, обуславливает смену парадигмы в подходах и методологиях проведения научных исследований, которые могут быть проведены на платформе биоколлекций. Биоколлекции представляют собой систематизированное собрание высококачественных образцов различного типа биоматериалов пациентов для долговременного хранения.
► Во всех областях медицинской науки подходы к созданию исследовательских биоколлекций только формируются, и их эффективность предстоит только оценить. В работе авторами оценивается возможность применения биоколлекции, созданной авторами согласно стратегии «лонгитюдное биобанкирование», в качестве платформы для раннего моделирования риска акушерских осложнений.
Что нового дает статья?
► Несмотря на сложность «лонгитюдного» подхода, коллекционирование биообразцов как на ранних сроках гестации, так и в контрольных «точках» на протяжении беременности позволяет оценивать динамику показателей, а также, что наиболее значимо, определять уровни предикторов на ранних сроках гестации до реализации осложнений.
► Включение в структуру коллекции различных типов высококачественных биообразцов позволяет оценивать различные биомаркеры в разных биологических средах с применением наиболее современных лабораторных методов, таких как секвенирование нового поколения. Сохранение широкого спектра клинических данных, ассоциированных с биообразцами, позволяет выявлять клинико-анамнестические предикторы осложнений.
► Разработка алгоритма раннего моделирования высокого риска преждевременных родов с учетом клинических, транскриптомных и протеомных данных на основе биоколлекции, созданной согласно стратегии «лонгитюдное биобанкирование», позволяет заключить об эффективности применения биоколлекции как платформы для поиска инструментов раннего прогнозирования риска акушерских осложнений.
Как это может повлиять на клиническую практику в обозримом будущем?
► Появление новых инструментов раннего прогнозирования риска акушерских осложнений позволит клиницистам при ведении беременности выбирать наилучшие стратегии риск-менеджмента и определять наиболее эффективные подходы к профилактике реализации тяжелых акушерских осложнений.
Цель: на платформе биоколлекции образцов беременных, созданной согласно стратегии «лонгитюдное биобанкирование», разработать алгоритм раннего моделирования высокого риска преждевременных родов (ПР) на основе клинических, протеомных и транскриптомных данных.
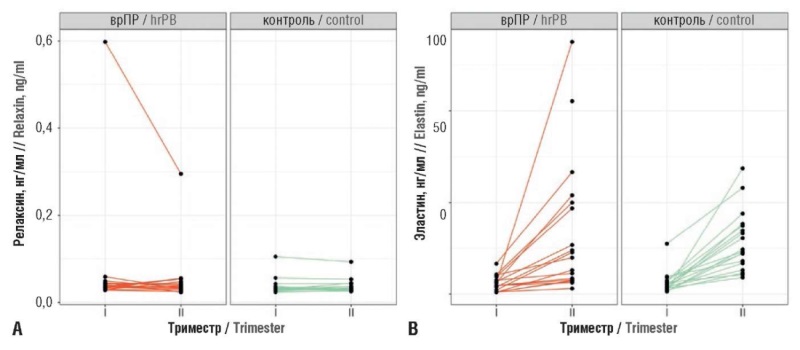
Материалы и методы. Проведено проспективное когортное исследование. Из биоколлекции были отобраны образцы сыворотки и плазмы крови, полученные в динамике в I и II триместрах гестации от 18 беременных с высоким риском ПР, реализовавших истмико-цервикальную недостаточность (ИЦН), и от 18 женщин с низким риском ПР, беременность которых не была осложнена ИЦН на любом сроке гестации. Проведен анализ клинико-анамнестических предикторов, определен уровень сывороточного релаксина и эластина, маркерных микроРНК (hsa-miR-432-5p, hsa-miR-134-5p, hsa-miR-431-5p, hsa-miR-122-5, hsa-miR-34a-5p).
Результаты. На основе наиболее значимых клинико-анамнестических предикторов, протеомного предиктора (уровень сывороточного релаксина), транскриптомных предикторов (экспрессия маркерных микроРНК) с использованием метода опорных векторов (англ. support vector machine, SVM) разработана прогностическая модель, высокая эффективность которой подтверждается ROC-кривыми (AUC = 0,83 при обучении и 0,67 в кросс-валидации), что позволяет использовать разработанный классификатор в качестве инструмента для оценки риска ПР.
Заключение. Биоколлекции образцов беременных, сформированные согласно стратегии «лонгитюдное биобанкирование», могут являться эффективной платформой для разработки технологий раннего прогнозирования риска акушерских осложнений.
Что уже известно об этой теме?
► Причины повышенного тромбообразования крайне разнообразны.
► Наступление беременности значительно повышает вероятность развития венозных тромбоэмболических осложнений (ВТЭО), особенно при наличии у женщин наследственных или приобретенных заболеваний, включая тромбофилические состояния.
► Для уменьшения частоты развития ВТЭО требуются настороженность и своевременная оценка существующих факторов риска у беременных.
Что нового дает статья?
► Данные регистра «БЕРЕГ» представляют картину реальной клинической практики по оценке риска ВТЭО у беременных.
Как это может повлиять на клиническую практику в обозримом будущем?
► Правильная оценка риска ВТЭО и своевременное начало тромбопрофилактики обеспечивают надежную профилактику осложнений во время беременности и послеродовом периоде.
► Выводы из исследования позволят лучше использовать актуальные клинические рекомендации «Венозные осложнения во время беременности и послеродовом периоде. Акушерская тромбоэмболия».
Введение. В последние годы наряду с увеличением возраста женщин, вступающих в беременность, и количества пациенток с экстрагенитальной патологией большую роль отводят прегравидарной подготовке и реализации профилактических мер, направленных на минимизацию развития тяжелых и нередко фатальных состояний, в частности, венозных тромбоэмболических осложнений (ВТЭО), которые являются одной из ведущих причин материнской и перинатальной смертности в развитых странах.
Цель: анализ эффективности и безопасности тромбопрофилактики у беременных с высоким риском развития ВТЭО в реальной клинической практике.
Материалы и методы. Анализ осуществлен на основании данных наблюдательного (когортного) исследования «Оценка клинического состояния беременных в течение гестации, в родах, раннем послеродовом периодах и через 12 месяцев после родов, а также анализ перинатальных исходов, состояние плода, новорожденного и качества лечения этих пациенток» – регистр «БЕРЕГ». Критерии включения в регистр: беременность на первом визите, получение письменного информированного согласия на участие в исследовании и постоянное проживание в Туле или Тульской области. Критерии невключения: нежелание подписать информированное согласие и проживание в других регионах. Данные брались из амбулаторной и стационарной карт и включали жалобы, анамнез, информацию о перенесенных и имеющих место заболеваниях, факторы риска ВТЭО, антропометрические показатели – рост, масса тела, индекс массы тела на момент вступления в беременность, препарат и доза антикоагулянта и антиагреганта. Особое внимание уделено акушерскому анамнезу – течению предыдущих и настоящей беременности, их перинатальным исходам, способам родоразрешения. Риск развития ВТЭО и тактику тромбопрофилактики оценивали по шкале «Антенатальная и постнатальная оценка факторов риска и тактика ведения беременности». Состояние новорожденного оценивали по росто-весовым показателям и по шкале Апгар на 1-й и 5-й минутах жизни.
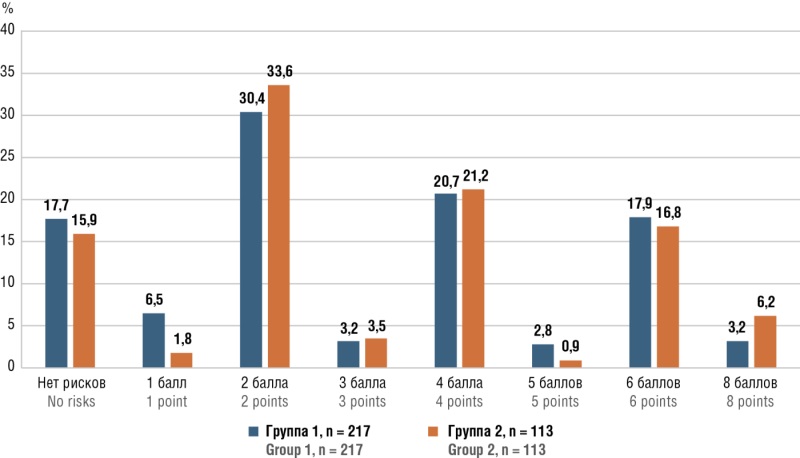
Результаты. Всего в регистр вошли 3214 беременных в возрасте от 15 до 46 лет, из которых были выделены 330 (10,3 %) женщин, получавших антитромботическую терапию антикоагулянтами и/или дезагрегантами. Из них 217 (65,8 %) принимали комбинированную терапию надропарином кальция (Фраксипарин) в дозе 0,3 мл (2850 МЕ анти-Ха) подкожно однократно в сутки в сочетании с ацетилсалициловой кислотой (АСК) в дозе 150 мг/сут перорально (группа 1) и 113 (34,2 %) – монотерапию АСК 150 мг/сут однократно перорально (группа 2). По основным клинико-лабораторным характеристикам группы были сопоставимы. Случаев ВТЭО, материнской смертности, аллергических реакций, тромбоцитопении и гепарин-индуцированных тромбозов в обеих группах зарегистрировано не было. Однако только в группе пациенток на монотерапии АСК имели место такие осложнения как кровотечение в родах (n = 1) и гибель плода (n = 3), но четкой связи с приемом препарата установить не представлялось возможным вследствие небольшого числа наблюдений. Обращает внимание недостаточная информированность врачей в необходимости использования шкал по оценке риска развития ВТЭО с целью объективизации тактики медикаментозного лечения, что определялось отсутствием в медицинских картах указаний об их использовании.
Заключение. Проведенный анализ показал эффективность и безопасносность тромбопрофилактики препаратом Фраксипарин в фиксированной дозе 0,3 мл у беременных высокого риска в реальной клинической практике, что подтверждено отсутствием случаев ВТЭО, кровотечений, материнской смерти, аллергических реакций, тромбоцитопении и гепарин-индуцированных тромбозов. Возможно, ввиду недостаточной информированности врачей о необходимости использования шкал по оценке риска развития ВТЭО для объективизации последующей тактики медикаментозного лечения были произвольно выбраны схемы профилактического воздействия – комбинированная терапия низкомолекулярным гепарином в сочетании с АСК или монотерапия АСК.
Что уже известно об этой теме?
► Послеоперационный болевой синдром остается актуальной клинической проблемой даже при минимально инвазивных вмешательствах. Лапароскопическая миомэктомия нередко сопровождается выраженной болью за счет висцерального компонента.
► Протокол ускоренного послеоперационного восстановления (ERAS) при лапароскопической миомэктомии предполагает применение мультимодальной анальгезии. Важным ее элементом считается превентивное использование местных анестетиков.
► Блокада гипогастрального сплетения ранее доказала эффективность при лечении хронической тазовой боли, что делает ее перспективной в хирургической гинекологии.
Что нового дает статья?
► Впервые описана методика комбинированного превентивного обезболивания при лапароскопической миомэктомии, включающая лапароскопическую блокаду верхнего гипогастрального сплетения и подкожную инфильтрацию области троакаров местным анестетиком.
► Использование данной методики снижает потребность в опиоидах и ускоряет мобилизацию пациенток в раннем послеоперационном периоде.
► Подтверждено, что послеоперационная боль при лапароскопической миомэктомии обусловлена преимущественно висцеральным компонентом, о чем свидетельствует преобладание глубокой тазовой боли у пациенток без блокады гипогастрального сплетения.
Как это может повлиять на клиническую практику в обозримом будущем?
► Применение комбинированной методики превентивного обезболивания позволяет снизить интенсивность боли в раннем послеоперационном периоде, уменьшить потребность в опиоидах и повысить безопасность анальгезии.
► Использование локальных методов анальгезии облегчает раннюю мобилизацию и способствует сокращению сроков госпитализации, что соответствует современным принципам ERAS протоколов.
► Включение лапароскопической блокады гипогастрального сплетения в рутинную практику может улучшить качество жизни пациенток и повысить удовлетворенность результатами хирургического лечения.
Цель: оценить влияние блокады верхнего гипогастрального сплетения в сочетании с превентивной инфильтрационной анестезией операционных ран на интенсивность болевого синдрома после лапароскопической миомэктомии.
Материалы и методы. В проспективное рандомизированное плацебо-контролируемое двойное слепое исследование включены 207 пациенток, которым была выполнена лапароскопическая миомэктомия. Пациентки, рандомизированные в 3 группы с целевым соотношением 1:1:1, включались в исследование постепенно, некоторые (n = 9) исключались из исследования интраоперационно. Таким образом, в исследование вошли 198 пациенток: группа 1 (n = 66) получала стандартную анальгезию в сочетании с инфильтрацией троакарных ран и блокадой верхнего гипогастрального сплетения, группа 2 (n = 65) – инфильтрацию троакарных ран без блокады сплетения, контрольная группа 3 (n = 67) получала только стандартную анальгезию. Первичной конечной точкой исследования была выраженность болевого синдрома по цифровой рейтинговой шкале (ЦРШ) через 4 часа после операции. Вторичными конечными точками являлись динамика болевого синдрома в другие контрольные точки (2, 6, 8, 12 и 24 часа после операции), сроки мобилизации, частота применения опиоидных анальгетиков, а также характер боли.
Результаты. Выраженность болевого синдрома была достоверно ниже в группе комбинированной анальгезии (группа 1) по сравнению с остальными группами в контрольных точках через 2, 4, 6, 8, 12 часов и на момент выписки (p < 0,05). Использование опиоидных анальгетиков в группе 1 составило 4,5 % против 32,8 % в группе 3 (p = 0,001). Время до первой мобилизации в группе 1 было достоверно короче по сравнению с группами 2 и 3 (медиана – 5 часов против 7 часов; p = 0,017). Висцеральный характер боли (ощущение глубокой тазовой боли) значительно чаще отмечался в группах 2 и 3, чем в группе 1 (p = 0,021).
Заключение. Комбинированная превентивная анальгезия с использованием инфильтрации операционных ран раствором анестетика и блокады гипогастрального нервного сплетения позволяет эффективно снижать выраженность послеоперационного болевого синдрома, минимизировать потребность в опиоидах и ускорять мобилизацию пациенток после лапароскопической миомэктомии.
Что уже известно об этой теме?
► Ангиогенез, или процесс формирования новых кровеносных сосудов, является естественным явлением, которое происходит как в нормальных, так и в патологических условиях. Например, заживление раны или восстановление эндометрия после менструации и подготовка эндометрия к имплантации подразумевают глубокие ангиогенные изменения. Ангиогенез также тесно связан с ростом опухолевых клеток.
► Эффекты ангиогенеза в организме человека представляют собой состояние баланса между ангиогенными стимуляторами (ангиогенными факторами) и ангиогенными ингибиторами (антиангиогенными факторами).
► Члены семейства фактора роста эндотелия сосудов (VEGF) являются главными регуляторами физиологического и патологического васкулогенеза, ангиогенеза и лимфангиогенеза.
Что нового дает статья?
► Впервые проведено исследование концентрации VEGF в крови у пациенток с вульвовагинальной атрофией (ВВА) и гормон-зависимыми злокачественными опухолями женской репродуктивной системы (рак эндометрия, рак цервикального канала, рак яичников, рак молочных желез).
► Впервые проведено определение концентрации VEGF в крови у женщин с ВВА и гормон-зависимыми доброкачественными опухолями женской репродуктивной системы.
► Впервые проведен сравнительный анализ уровня VEGF в плазме у женщин с ВВА со злокачественными новообразованиями и доброкачественными заболеваниями женских половых органов с группой здоровых женщин.
Как это может повлиять на клиническую практику в обозримом будущем?
► Правильная регуляция ангиогенеза и проницаемости сосудов имеет важное значение для физиологического функционирования женского репродуктивного тракта, а многие патологические состояния, такие как аномальные маточные кровотечения, эндометриоз, ВВА, связаны с сосудистым компонентом.
► Повышенная экспрессия VEGF у женщин с ВВА по сравнению с группой здоровых женщин может быть связана с нарушениями васкуляризации и регенерации тканей влагалища и вульвы, которые дополнительно усиливаются при злокачественных процессах.
► Полученные результаты указывают на важную роль VEGF в процессах ангиогенеза, ассоциированным со злокачественными заболеваниями.
Введение. Ангиогенез является важным процессом роста и развития сосудов в норме, при заживлении ран и решающим фактором прогрессирования опухолей. Одним из главных стимуляторов ангиогенеза является фактор роста эндотелия сосудов (англ. vascular endothelial growth factor, VEGF), в присутствии которого эндотелиальные клетки начинают активно пролиферировать и мигрировать; в злокачественных опухолях VEGF поддерживает развитие опухолевых сосудов, что, возможно, имеет корреляцию с прогнозом и диагностикой рака.
Цель: оценить концентрацию VEGF в крови у пациенток с вульвовагинальной атрофией (ВВА) и гормон-зависимыми злокачественными опухолями репродуктивной системы женщин (молочных желез, цервикального канала, яичников и эндометрия), гормон-зависимыми доброкачественными опухолями женской репродуктивной системы и у здоровых женщин.
Материалы и методы. Проведено поперечное исследование, которое включало 68 диагностированных случаев ВВА и рака женских репродуктивных органов (группа 1) – рак молочной железы (РМЖ), рак цервикального канала (РЦК), рак эндометрия (РЭ), рак яичников (РЯ); 53 женщины с ВВА и доброкачественными заболеваниями женских половых органов (группа 2) и 80 здоровых женщин перименопаузального периода без гинекологической патологии (контрольная группа). Гистопатологическим типом злокачественных новообразований (ЗНО) являлась аденокарцинома, стадия 1А. Оценка концентраций VEGF в плазме крови проводилась с помощью иммуноферментного анализа. Образцы крови получали путем пункции периферической вены перед хирургическим вмешательством. Статистическая обработка полученных данных проводилась с использованием программы StatTech v. 4.8.5 (ООО «СтатТех», Россия).
Результаты. Медианный уровень VEGF в плазме 80 здоровых женщин (контрольная группа) составил 190 (диапазон 40,00–661,50) пг/мл, в группе 1 – 452,0 (диапазон 69,98–2808,44) пг/мл и в группе 2 – 323,0 (диапазон 95,7–1100,0) пг/мл. Медианный уровень и межквартильный размах VEGF у 30 больных c ВВА и РМЖ, 10 больных с ВВА и РЦК, 10 больных с ВВА и РЭ и 9 больных с ВВА и РЯ составили 632,0 [360,0–1110,5] пг/мл, 228,0 [209,5–238,5] пг/мл, 448,0 [422,0–499,5] пг/мл и 503,0 [211,0–1337,0] пг/мл, соответственно. Концентрации VEGF у больных с ВВА и РМЖ, РЯ и РЭ были значимо выше, чем у здоровых женщин (U-критерий Манна-Уитни, р = 0,001, р = 0,021 и р < 0,0001, соответственно). Но у больных с ВВА и РЦК уровень VEGF не имел статистически значимых различий по сравнению со здоровыми женщинами. Медианный уровень VEGF в плазме у пациенток с ВВА и доброкачественными заболеваниями женских половых органов составил 323,0 (диапазон 95,7–1100,0) пг/мл, что демонстрирует статистически значимые различия по сравнению с контрольной группой (р = 0,007).
Заключение. Выявлены существенные различия между концентрацией VEGF у женщин с ВВА и злокачественными опухолями репродуктивной системы и у женщин с ВВА и доброкачественными новообразованиями женских половых органов по сравнению с контрольной группой здоровых женщин. Полученные результаты указывают на важную роль VEGF в процессах ангиогенеза, ассоциированным со злокачественными заболеваниями. Повышенная экспрессия VEGF у женщин с ВВА по сравнению с группой здоровых женщин может быть связана с нарушениями васкуляризации и регенерации тканей влагалища и вульвы, которые дополнительно усиливаются при злокачественных процессах.
НАУЧНЫЕ ОБЗОРЫ
Что уже известно об этой теме?
► Бесплодие – глобальная проблема здравоохранения, в половине случаев обусловленная состоянием мужского репродуктивного здоровья.
► Микронутриенты-антиоксиданты улучшают качество спермы.
► Миоинозитол (МИ) и D-хироинозитол (ДХИ) являются «сырьем» для биосинтеза фосфатидилинозитол фосфатов – важной разновидности сигнальных молекул, играющих важнейшие роли в цитогенезе, морфогенезе и росте ооцитов.
Что нового дает статья?
► МИ/ДХИ, их биологически активные производные, марганец и фолаты играют ключевые роли в функционировании сперматозоидов, начиная с вызревания сперматозоидов и заканчивая оплодотворением ооцитов.
► МИ и ДХИ принципиально необходимы для оплодотворения ооцитов; ионы марганца важны для функции гамет посредством влияния на концентрацию тестостерона, повышение активности антиоксидантных ферментов и митохондриального потенциала; фолаты, снижая уровни гаметотоксичного гомоцистеина, способствуют сохранению целостности ДНК сперматозоидов.
► Результаты экспериментальных и клинических исследований моделей глубокого дефицита инозитолов указывают на воздействия МИ/ДХИ и их синергистов на подвижность сперматозоидов, в том числе через модуляцию электрических полей.
Как это может повлиять на клиническую практику в обозримом будущем?
► Перспективно назначение МИ/ДХИ в сочетании с органическими солями марганца и фолатами пациентам с идиопатической патоспермией, инсулинорезистентностью, ожирением и в условиях оксидативного стресса.
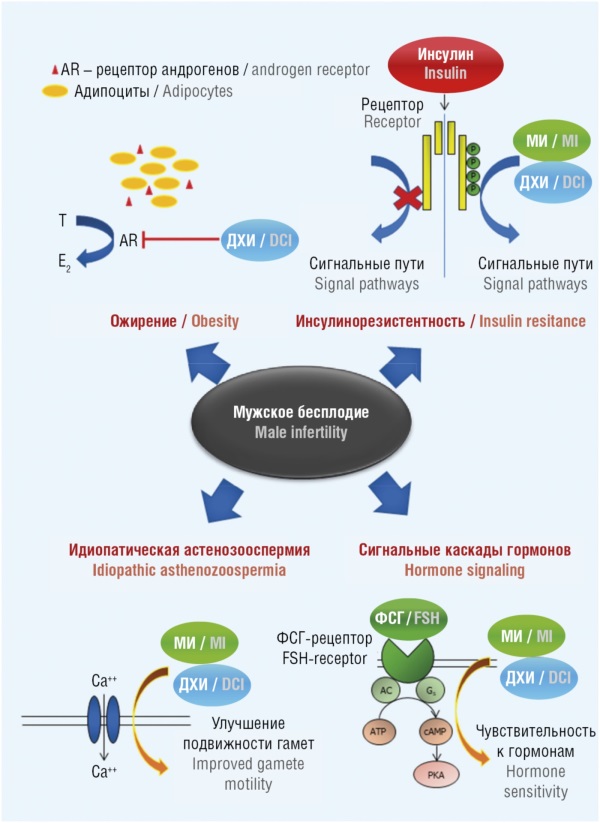
Важным фактором вторичного мужского бесплодия является дефицит витаминов и микроэлементов. В настоящей работе систематизирован комплекс исследований миоинозитола (МИ), D-хироинозитола (ДХИ), их синергистов (фолаты, ионы марганца) в поддержании структуры и функционирования гамет. МИ и ДХИ улучшают общее количество подвижных и прогрессивно подвижных сперматозоидов посредством участия в сигнальных каскадах рецепторов репродуктивных гормонов (что нормализует обмен андрогенов и способствует профилактике инсулинорезистентности) и улучшения функции митохондрий. МИ и ДХИ оказывают воздействие на созревание/функционирование сперматозоидов, их подвижность и процесс оплодотворения ооцитов, в том числе с участием инозитол-зависимого сигнального белка фосфолипазы C-дзета (англ. phospholipase C-zeta, PLCz) и посредством модуляции электрических полей гамет. Клинические данные по использованию МИ и ДХИ при мужском бесплодии указывают на улучшение состояния zona pellucida, плазматической мембраны, цитоплазмы и рецепции сперматозоидов. Ионы марганца способствуют улучшению функционирования гаметоцитов посредством влияния на концентрацию тестостерона, повышения активности антиоксидантных ферментов и мембранного потенциала митохондрий. Фолаты, снижая уровни гаметотоксичного гомоцистеина, способствуют сохранению целостности ДНК сперматозоидов. Перспективно назначение МИ/ДХИ в сочетании с органическими солями марганца и фолатами пациентам с идиопатической патоспермией, особенно на фоне нарушений обмена углеводов (инсулинорезистентность) и сниженной антиоксидантной защиты.
Что уже известно об этой теме?
► Химические вещества, разрушающие эндокринную систему (EDC), представляют собой широкий класс ксенобиотиков, способных нарушать гормональную регуляцию и оказывать негативное воздействие на репродуктивное здоровье женщин.
► Ранее установлено, что EDC, включая бисфенол А, фталаты и диоксины, могут вызывать окислительный стресс, гормональные нарушения и ускоренное истощение овариального резерва.
► Ряд исследований продемонстрировал способность EDC индуцировать эпигенетические изменения, которые потенциально передаются следующему поколению, усиливая межпоколенческое воздействие этих веществ.
Что нового дает статья?
► EDC вызывают апоптоз клеток гранулезы, нарушают митохондриальные функции и провоцируют эпигенетические изменения, приводящие к истощению овариального резерва и преждевременной недостаточности яичников.
► Воздействие EDC изменяет экспрессию микроРНК и длинных некодирующих РНК, что влияет на регуляцию фолликулогенеза, овуляторные процессы и гормональный баланс.
► Некоторые природные соединения и антиоксиданты ослабляют токсические эффекты EDC, снижая окислительный стресс, нормализуя передачу сигнала и восстанавливая экспрессию ключевых генов в клетках яичников.
Как это может повлиять на клиническую практику в обозримом будущем?
► Использование антиоксидантов, сигнальных модуляторов и эпигенетических регуляторов может быть интегрировано в схемы терапии для снижения репродуктивной токсичности у женщин, подвергшихся воздействию EDC.
► Учет вклада EDC в патогенез дисфункции яичников способен изменить подходы к ведению пациенток с идиопатическим бесплодием, синдромом поликистозных яичников и преждевременной овариальной недостаточностью.
Химические вещества, разрушающие эндокринную систему (англ. endocrine-disrupting chemicals, EDC), представляют собой широкий спектр экзогенных веществ, способных нарушать нормальное функционирование гормональной системы и вызывать серьезные последствия для женского репродуктивного здоровья. Одной из наиболее уязвимых мишеней для действия EDC являются яичники, в которых они запускают ряд патофизиологических процессов. В настоящей статье систематизированы современные данные о ключевых механизмах овариальной токсичности, индуцированной EDC, включая нарушение гормональной регуляции, окислительный стресс, апоптоз, эпигенетические модификации и нарушение межклеточной сигнализации. Показано, что хроническое воздействие таких соединений, как бисфенол А, фталаты, полициклические ароматические углеводороды и диоксины, приводит к нарушению фолликулогенеза, истощению овариального резерва и преждевременной недостаточности яичников. Кроме того, обсуждаются механизмы эпигенетического наследования, через которые EDC могут оказывать долговременное влияние на репродуктивную функцию нескольких поколений. Особое внимание уделено терапевтическим стратегиям, включая использование антиоксидантов, модуляторов сигнальных путей и эпигенетических регуляторов, направленных на смягчение токсических эффектов EDC. Приведены тематические исследования, демонстрирующие глобальное распространение загрязнения окружающей среды EDC и их биоаккумуляцию в биологических объектах. Полученные данные подчеркивают необходимость междисциплинарного подхода к оценке рисков и разработки профилактических и лечебных мер, направленных на снижение влияния EDC на репродуктивное здоровье женщин и охрану репродуктивного потенциала будущих поколений.
Что уже известно об этой теме?
► Полного понимания патогенеза развития доброкачественной гиперплазии предстательной железы (ДГПЖ) и рака предстательной железы (РПЖ) на данный момент нет.
► Как ДГПЖ, так и РПЖ прогрессируют, и применяемые средства достаточно эффективны, но способствуют развитию побочных эффектов, ухудшающих качество жизни, таких как ухудшение сексуальной функции, вплоть до полного ее отсутствия.
► ДГПЖ и РПЖ имеют выраженную возрастную взаимосвязь, развиваясь крайне редко в молодом и среднем возрасте и стремительно увеличиваясь в своей частоте у возрастных мужчин, возникая в подавляющем количестве случаев.
Что нового дает статья?
► Данная статья освещает влияние прогестерона на механизм развития заболеваний предстательной железы и демонстрирует важность системного подхода не только к физиологии и патофизиологии, но и к профилактике и лечению.
► Натуральные и синтетические формы гормонов оказывают существенно различный эффект, что должно учитываться при использовании препаратов в практической медицине.
► Представлены результаты влияния эстрогенов на фермент 5α-редуктазу, что также подчеркивает многофакторность развития таких сложных заболеваний, как ДГПЖ и РПЖ.
Как это может повлиять на клиническую практику в обозримом будущем?
► Привлекая внимание ученых и клиницистов, можно инициировать проведение клинических исследований, которые дадут возможность ответить на вопрос: эффективно и безопасно ли использование прогестерона в клинической практике для профилактики и лечения ДГПЖ и РПЖ.
► Также важно оценить, будет ли использование прогестерона более эффективным, чем применение широко используемых сейчас препаратов из класса блокаторов 5α-редуктазы.
► Можно ли избежать таких побочных явлений, как нарушение эректильной функции и снижение либидо, которые возникают при использовании препаратов из класса блокаторов 5α-редуктазы, если будет применяться прогестерон.
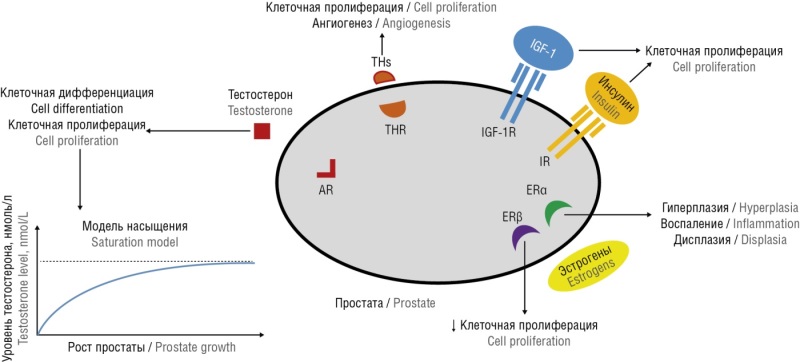
Распространенность заболеваний предстательной железы, прежде всего доброкачественной гиперплазии (ДГПЖ) и рака предстательной железы (РПЖ), прогрессивно увеличивается с возрастом, когда баланс гормонов существенно меняется. Ученые и клиницисты придерживаются традиционных позиций в аспекте патогенеза развития ДГПЖ, и существенных достижений в профилактике и лечении этого заболевания нет. Продолжающиеся поиски в понимании механизмов развития данных патологий не затрагивают один из ключевых гормонов, играющих важную роль в функционировании предстательной железы – прогестерон, который никоим образом не исследовался долгие годы в этой взаимосвязи. До сих пор бытует мнение, что прогестерон – это исключительно «женский гормон», несмотря на то, что первой линией терапии при ДГПЖ являются препараты, снижающие активность фермента 5α-редуктазы, трансформирующих тестостерон в дигидротестостерон, а в условиях нормальной работы организма эту функцию в мужском организме как раз выполняет прогестерон. И указанные препараты, по сути, являются химическими аналогами прогестерона с небольшими изменениями в структуре молекулы. Иначе говоря, чтобы исправить патофизиологические аспекты, нужно исходить из физиологических аспектов. Учитывая эти предпосылки, проведен анализ имеющихся в мировой научной литературе данных, посвященных патогенезу ДГПЖ и РПЖ и эффективности различных патогномоничных терапевтических подходов в профилактике данных заболеваний.
КЛИНИЧЕСКИЕ СЛУЧАИ
Что уже известно об этой теме?
► Генитоуринарный синдром (ГУМС) в менопаузе ассоциирован с дефицитом эстрогена и сопровождается не только атрофией слизистых вульвы и влагалища, но и недержанием мочи, гиперактивным мочевым пузырем, пролапсом гениталий.
► Локальная терапия эстриолом в постменопаузе позволяет эффективно устранять симптомы вульвовагинальной атрофии в менопаузе, а также уменьшать проявления недержания мочи. Также применение локального эстриола необходимо при использовании урогинекологического пессария в менопаузе.
► Использование фракционного СО2-лазера на коже вульвы дает видимый эстетический эффект и улучшает качество кожи на вульве в менопаузе. Но воздействие лазером в этой зоне болезненно, поэтому возможно использование локального анестетика в форме крема ЭМЛА.
Что нового дает статья?
► Статья дает четкие практические алгоритмы по комбинации различных методов лечения проявлений ГУМС в менопаузе для устранения не только атрофических изменений на слизистой влагалища и вульвы, но и купирования симптомов недержания мочи, гиперактивного мочевого пузыря, пролапса гениталий.
Как это может повлиять на клиническую практику в обозримом будущем?
► Статья открывает перспективы для комбинированного или комплексного лечения различных проявлений ГУМС с использованием современных доказательных данных.
Генитоуринарный менопаузальный синдром (ГУМС) проявляется множеством клинических симптомов, таких как диспареуния, сухость слизистой оболочки влагалища и вульвы, а также может быть связан с недержанием мочи и опущением тазовых органов. Эти состояния значительно влияют на качество жизни женщин в постменопаузе и способствуют их социальной изоляции и психоэмоциональным расстройствам. Современные подходы к лечению ГУМС включают применение локальных гормональных препаратов (преимущественно в стандартной дозе 0,5 мг эстриола), таких как, например, оригинальный препарат Овестин в комбинации с хирургическим лечением, малоинвазивными лазерами, урогинекологическими пессариями. Крем ЭМЛА (комбинация лидокаина и прилокаина), обладая местноанестезирующими свойствами, может быть использован в качестве безопасного анестетика перед инвазивными процедурами. Статья рассматривает клинические случаи, иллюстрирующие варианты лечебных подходов у пациенток с различными проявлениями ГУМС, включая пролапс тазовых органов и стрессовое недержание мочи. В первом случае проведена слинговая уретропексия с предварительной терапией эстриолом, что позволило предотвратить послеоперационные осложнения и улучшить реабилитацию. Во втором случае комбинация местной и системной гормональной терапии, а также использование селективного β3-агониста привели к значительному улучшению состояния пациентки с гиперактивным мочевым пузырем, снизив частоту позывов к мочеиспусканию. Отдельно обсуждается пациентка с диспареунией, у которой фракционный фототермолиз в сочетании с локальной гормональной терапией привел к значительному улучшению состоянии слизистой влагалища и снижению болевого синдрома при половой жизни. Таким образом, необходимо придерживаться индивидуализированного подхода к лечению ГУМС, акцентируя внимание на мультидисциплинарной стратегии, которая сочетает хирургическую и медикаментозную терапию с физической реабилитацией. Локальная гормональная терапия, использование фракционного СО2-лазера и другие методы позволяют значительно повысить качество жизни женщин в постменопаузе, и важность этих вопросов в клинической практике требует дальнейшего обсуждения и исследования. Предоставление пациенткам четкой информации о доступных методах лечения создает возможности для активного их участия в управлении своим здоровьем, что в конечном итоге способствует улучшению качества жизни.
Что уже известно об этой теме?
► Вирус герпеса человека 6-го типа (ВГЧ-6) способен интегрироваться в хромосомный аппарат человека и передаваться по наследству, в том числе вертикально, что делает его особым среди герпесвирусов и потенциально значимым для перинатальной медицины.
► У детей раннего возраста ВГЧ-6 проявляется внезапной экзантемой, фебрильными судорогами и мононуклеозоподобным синдромом, однако такие проявления обычно возникают после 6 месяцев и редко встречаются у новорожденных.
► Врожденная ВГЧ-6 инфекция описана в литературе крайне ограниченно, что затрудняет клиническую настороженность и затягивает своевременную диагностику в неонатальном периоде.
Что нового дает статья?
► Впервые в отечественной практике представлен документированный случай врожденной инфекции ВГЧ-6 у доношенного новорожденного с подтверждением диагноза на основании положительных результатов ПЦР-диагностики в крови и слюне в первые дни жизни.
► Проведен системный анализ клинических, лабораторных и инструментальных данных, который позволил сопоставить индивидуальный случай с современными представлениями о герпесвирусных инфекциях у новорожденных и расширить знания об их неонатальных формах.
► Впервые акцентирована диагностическая ценность одновременного обследования матери и новорожденного в первые часы жизни, включая молекулярные методы, для выявления возможной перинатальной передачи ВГЧ-6.
Как это может повлиять на клиническую практику в обозримом будущем?
► Рутинное включение ВГЧ-6 в диагностическую панель у новорожденных с неясной лихорадкой может способствовать более ранней постановке диагноза, сокращению необоснованной эмпирической антибактериальной терапии и улучшению качества неонатальной помощи в раннем постнатальном периоде.
► Формируется новая клиническая настороженность у неонатологов и инфекционистов в отношении возможной вертикальной передачи герпесвирусов, не входящих в классическую TORCH-группу, что может изменить подходы к обследованию новорожденных.
► Расширяется область применения ПЦР-диагностики в рутинной неонатальной практике при наличии клинических признаков внутриутробной инфекции неясной этиологии, включая использование образцов слюны и пуповинной крови для ранней верификации диагноза.
Инфекция, вызванная вирусом герпеса человека 6-го типа (ВГЧ-6) у новорожденных детей, встречается крайне редко. Уникальность ВГЧ-6 заключается в том, что это единственный вирус, который интегрируется в хромосомы человека и передается от родителей к потомству. ВГЧ-6 у человека может быть связан с широким спектром заболеваний, а у детей нередко протекает с развитием внезапной экзантемы, фебрильных приступов, афтозного стоматита, мононуклеозоподобного синдрома или лихорадки без очага инфекции. Предлагаем описание редкого клинического наблюдения врожденной инфекции ВГЧ-6 у новорожденного ребенка, поскольку описаний таких случаев как в отечественной, так и в зарубежной литературе крайне мало, что отражает, по нашему мнению, значительные пробелы в знаниях врачей-неонатологов в данном вопросе. Обсуждаются формы течения заболевания, редкие клинические наблюдения, а также методы диагностики и терапии ВГЧ-6.
ИЗ ИСТОРИИ
При физиологических (нормальных) родах наиболее ответственным для роженицы является третий (последовый) период родов. Происходит силами природы (сокращения матки) отделение плаценты и потугой роженицы выделение (рождение) последа. При неэффективности потуживания роженицы послед удаляется из матки искусственно, специальными способами. Длительность последового периода определена в пределах 15–30 минут. В это время тщательно наблюдают за признаками отделения плаценты и при их появлении способствуют удалению последа из родовых путей. Среди общеизвестных таких признаков один носит название фамилий авторов – Кюстнера–Чукалова. В процессе занятий со студентами обращало на себя внимание различное написание названия признака как в учебниках по акушерству, так и в специальных публикациях. В данной статье проведено исследование первоисточников с целью унификации названия признака отделения плаценты «Кюстнера–Чукалова».
СОБЫТИЯ

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.
ISSN 2500-3194 (Online)