Перейти к:
Комплексный биохимический анализ состава препаратов и биологически активных добавок омега-3 полиненасыщенных жирных кислот для нутрициальной поддержки беременности
https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.669
Аннотация
Введение. Омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК), модулируя сложным образом обмен эйкозаноидов (в том числе простагландинов, липоксинов и лейкотриенов) и докозаноидов (нейропротектинов, резолвинов, маресинов), являются важным фактором репродуктивного и соматического здоровья женщин.
Цель: сравнить образцы ω3-ПНЖК по степени стандартизации состава по эйкозапентаеновой (ЭПК) ω3-ПНЖК и докозагексаеновой (ДГК) ω3-ПНЖК, оценить степень очистки от жирнокислотных примесей.
Материалы и методы. В работе представлены результаты хроматографического анализа 10 препаратов ω3-ПНЖК.
Результаты. Исследование позволило выявить показатели состава экстрактов ω3-ПНЖК, посредством которых возможно отличать фармацевтически стандартизированные препараты ω3-ПНЖК (Омакор, Фемибион Наталкер-2 и др.) от менее стандартизированных препаратов (Омеганол, Омегамама и др.).
Заключение. Более стандартизированный препарат Фемибион Наталкер-2 эффективен и безопасен для поддержки репродуктивной функции во время беременности и для улучшения неврологического развития детей. Омакор – высоко стандартизированный препарат, но не имеет официального разрешения к применению у беременных.
Ключевые слова
Для цитирования:
Громова О.А., Торшин И.Ю., Иловайская И.А., Громов А.Н. Комплексный биохимический анализ состава препаратов и биологически активных добавок омега-3 полиненасыщенных жирных кислот для нутрициальной поддержки беременности. Акушерство, Гинекология и Репродукция. 2025;19(5):675-689. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.669
For citation:
Gromova O.A., Torshin I.Yu., Ilovaiskaia I.A., Gromov A.N. Comprehensive biochemical analysis of the omega-3 polyunsaturated fatty acid-based drug and biologically active additive composition for nutritional support of pregnancy. Obstetrics, Gynecology and Reproduction. 2025;19(5):675-689. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.669
Введение / Introduction
Длинноцепочечные омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК) абсолютно незаменимы для нормального функционирования репродукции, физиологического течения беременности, развития зрения, мозга плода, формирования иммунного ответа [1][2]. Омега-3 ПНЖК тормозят старение и фиброзирование тканей почек и печени [3], миокарда [4], зрения и мозга [5], кожи [6]. Важность обеспеченности организма ω3-ПНЖК следует из фундаментальной биохимии, детально описанной в многочисленных оригинальных исследованиях, обзорных статьях, доказательных исследованиях и экспертных консенсусах [7][8].
В частности, из таких ключевых форм ω3-ПНЖК, как эйкозапентаеновая кислота (ЭПК) и докозагексаеновая кислота (ДГК), образуются важнейшие медиаторы воспаления – эйкозаноиды и докозаноиды, приниципально важные для физиологического окончания воспаления (англ. resolution of inflammation), для нейропротекции и для нормофизиологического роста тканей плода, для нутрициальной поддержки беременности и профилактики послеродовой депрессии [1].
ЭПК и ДГК, активируя рецептор, активируемый пролифератором пероксисом альфа (англ. рeroxisome proliferator-activated receptor alpha, PPARα) и другие сигнальные пути, способствуют улучшению энергетического метаболизма в печени, увеличивая β-окисление жирных кислот и продукцию АТФ [3], ингибируют синтез провоспалительных медиаторов, обеспечивают поддержку барьерной функции и гидратации кожи [6][9], способствуют синтезу антифибротических метаболитов, защищающих ткань почек при токсикозе, препятствуя формированию хронической болезни почек [10].
Благотворное влияние ω3-ПНЖК на репродуктивные процессы у женщин основано не только на поддержке соматического здоровья, но и прямой поддержке репродуктивной системы. Достаточная обеспеченность ЭПК и ДГК способствует формированию и предотвращает старение ооцитов, тормозя ферроптоз [11], поддерживая уровень лютеинизирующего гормона и соотношение прогестерон/эстрадиол [12].
Важным аспектом действия ω3-ПНЖК является тонкая модуляция биосинтеза простагландинов (англ. prostaglandin, PG) и, в частности, PGE2 и PGF2α. Эти 2 простагландина регулируют синтез прогестерона, состояние желтого тела и лютеолиз, сократительную функцию матки при родовой деятельности, участвующих в созревании шейки матки, разрыве плодных оболочек, сокращении миометрия и воспалении. Поскольку существует множество подтипов рецепторов для PGE2 и PGF2α, связанных с различными сигнальными путями, эффекты PGE2 и PGF2α в значительной степени зависят от пространственной и временной экспрессии этих рецепторов во внутриматочных тканях. PGE2, вероятно, более важен для начала родов, в то время как PGF2α может играть более важную роль в их завершении, что может быть связано с дифференциальным действием PGE2 и PGF2α в тканях матки [13].
Однако избыточная активность PGE2 и PGF2α, стимулируя приток нейтрофилов и продукцию цитокинов, экспрессию циклооксигеназы-2 (тем самым усиливая свою собственную продукцию), отрицательно сказывается на продолжительности вынашивания. Соотношение с ω3:ω6 ПНЖК в диете влияет на синтез PGE2 и PGF2α. Например, в эксперименте у мышей, получавших ω3-ПНЖК, все показатели фертильности были в норме, лютеолиз и роды также прошли нормально, а уровни синтеза PGF2α и PGE2 в матке составляли 50 % по сравнению с группой ω6-ПНЖК мышей, получавших соевое масло, что способствовало поддержке нормальной продолжительности вынашивания [14]. Употребление в пищу ω3-ПНЖК может продлевать беременность за счет снижения внутриматочной выработки PGE2 и PGF2α [15], что подтверждено в доказательных исследованиях [1][8].
Принимая во внимание крайне низкую обеспеченность россиянок ω3-ПНЖК [1], необходимо использование препаратов ω3-ПНЖК для компенсации этого микронутриентного дефицита. Очевидно, что пользу от применения препаратов ω3-ПНЖК можно ожидать только при условии применения качественных ω3-ПНЖК, действительно содержащих надлежащее количество ω3-ПНЖК и не содержащих примесей с прооксидантным и атерогенным действием [16].
Содержание в составе экстрактов ω3-ПНЖК, с одной стороны, ЭПК и ДГК, и, с другой стороны, других жирных кислот (как ненасыщенных, так и насыщенных) оказывает существенное влияние на фармакологические свойства соответствующих препаратов и биологически активных добавок (БАД). Например, насыщенные пальмитиновая, миристиновая, лауриновая кислоты стимулируют атерогенез как через повышение содержания общего холестерина и липопротеинов низкой плотности, так и через активацию провоспалительных толл-подобных рецепторов (англ. toll-like receptors, TLR) TLR4 и цитокинов – интерлейкина (англ. interleukin, IL) IL-6 и фактора некроза опухоли альфа (англ. tumor necrosis factor-alpha, TNF-α) [17][18]. Стеариновая и пальмитиновая кислоты способствуют развитию инсулинорезистентности [1]. Ненасыщенные ω-6 и ω-11 жирные кислоты также могут провоцировать развитие провоспалительных реакций. Поэтому стандартизация состава экстрактов ω3-ПНЖК по различным видам жирных кислот – фундаментальная основа эффективности и безопасности соответствующих препаратов и БАД на основе ω3-ПНЖК [16].
В настоящей работе мы представляем результаты количественного хроматографического анализа 10 препаратов ω-3 ПНЖК. Собранные биохимические данные анализировались с использованием современного комплекса информационных технологий, развиваемых в рамках топологического подхода к анализу данных [19–21].
Цель: сравнить образцы ω3-ПНЖК по степени стандартизации состава по эйкозапентаеновой ω3-ПНЖК и докозагексаеновой ω3-ПНЖК, оценить степень очистки от жирнокислотных примесей.
Материалы и методы / Materials and Methods
Препараты, исследованные в настоящей работе, перечислены в таблице 1. Большинство исследованных препаратов изготовлялись на основе сырья, включающего жир тех или иных сортов рыбы.
Таблица 1. Заявленное производителем содержание жирных кислот в исследованных препаратах омега-3 полиненасыщенных жирных кислот (ω3-ПНЖК).
Table 1. Manufacturer-declared fatty acids content of fatty acids in the studied omega-3 polyunsaturated fatty acids (ω3-PUFA) preparations.
|
N |
Препарат / Preparation |
Экстракт ПНЖК, мг PUFA extract, mg |
ω3, мг ω3, mg |
ЭПК, мг EPA, mg |
ДГК, мг DНА, mg |
Другие ω3 Other ω3 |
|
1 |
Омега-3 Доппельгерц® Актив / Omega-3 Doppelherz® Activ |
950 |
300 |
144 |
96 |
60 |
|
2 |
Рыбий жир-Тева® / Fish oil-Teva® |
500 |
165 |
НЗ / UK |
НЗ / UK |
165 |
|
3 |
Омегатрин® / Omegatrin® |
780 |
397,8 |
НЗ / UK |
НЗ / UK |
397,8 |
|
4 |
Омега-3 концентрат® / Omega-3 concentrate® |
1000 |
600 |
330 |
220 |
50 |
|
5 |
Омегамама® / Omegamama® |
500 |
150 |
15 |
105 |
30 |
|
6 |
Омеганол® / Omeganol® |
400 |
32 |
НЗ / UK |
НЗ / UK |
32 |
|
7 |
Фемибион® Наталкер-2 / Femibion® Natalcare II |
500 |
200 |
0 |
200 |
0 |
|
8 |
Омакор® / Omacor® |
1000 |
900 |
460 |
380 |
60 |
|
9 |
Солгар® Oмега-3 950 мг / Solgar® Omega-3 950 mg |
1350 |
950 |
504 |
378 |
68 |
|
10 |
Омега-3 ВкусВилл® / Omega-3 VkusVill® |
1000 |
900 |
500 |
200 |
200 |
Примечание: ЭПК – эйкозапентаеновая кислота; ДГК – докозагексаеновая кислота; НЗ – неизвестно.
Note: EPA – eicosapentaenoic acid; DHA – docosahexaenoic acid; UK – unknown.
Хроматографическое определение жирнокислотного состава / Chromatographically determined fatty acid composition
Образцы препаратов из таблицы 1 растворяли в гексане и подвергали солянокислому гидролизу в присутствии метанола (Methanolic-HCl (3N) Supelco) в плотно укупоренных виалах при 90 °С в течение 1 часа. Полученные таким образом метиловые эфиры жирных кислот анализировали на хроматографе GCMS-QP2010 Ultra (Shimadsu, Япония) при следующих условиях: газ-носитель – гелий, линейная скорость 35,6 см/сек (0,9 мл/мин), деление потока 4:1. Колонка капиллярная MDN-5 (Supelco), длина 30 метров, внутренний диметр 0,25 мм. Параметры хроматографа: в режиме градиента температур, детектор 200 °С, интерфейс 205 °С, режим измерения – от 45 до 450 m/z. Качественный состав полученных смесей определяли с использованием библиотеки масс-спектров NIST 11 (National Institute of Standards and Technology 11), количественный – конкретными соединениями из перечисленных в таблице 2. В результате проведения настоящей серии экспериментов каждый препарат описывался вектором из 55 позиций, в каждой из которых представлена площадь пика, соответствующая тому или иному соединению из таблицы 2.
Таблица 2. Соединения, найденные в исследованных образцах в результате проведения хроматографического анализа.
Table 2. Compounds chromatographically determined in the studied samples.
|
Cоединение / Compound |
Тип / Type |
|
11-эйкозеновая кислота / 11-eicosenic acid |
ω9 |
|
11-эйкозеновая кислота, пропиловый эфир / 11-eicosenoic acid, propyl ester |
ω9 |
|
13-докозеновая кислота / 13-docosenoic acid |
ω9 |
|
13-докозеновая кислота, пропиловый эфир / 13-docosenoic acid, propyl ester |
ω9 |
|
13-метилтетрадеканоевая кислота / 13-methyltetradecanoic acid |
НЖК / SFA |
|
4,7,10,13,16,19-докозагексаеновая кислота, бутиловый эфир / 4,7,10,13,16,19-docosahexaenoic acid, butyl ether |
ДГК / DНА |
|
4,7,10,13,16,19-докозагексаеновая кислота / 4,7,10,13,16,19-docosahexaenoic acid |
ДГК / DНА |
|
5,11,14,17-эйкозатетраеновая кислота / 5,11,14,17-eicosatetraenoic acid |
ЭТК / ETА |
|
5,8,11,14,17-эйкозапентаеновая кислота, этиловый эфир / 5,8,11,14,17-eicosapentaenoic acid, ethyl ester |
ЭПК / EPA |
|
5,8,11,14,17-эйкозапентаеновая кислота / 5,8,11,14,17-eicosapentaenoic acid |
ЭПК / EPA |
|
5,8,11,14,17-эйкозапентаеновая кислота, пропиловый эфир / 5,8,11,14,17-eicosapentaenoic acid, propyl ester |
ЭПК / EPA |
|
6,9,12,15-гексадекатетраеновая кислота / 6,9,12,15-hexadecatetraenoic acid |
ω3 |
|
6,9,12,15-октадекатетраеновая кислота, бутиловый эфир / 6,9,12,15-octadecatetraenoic acid a, butyl ester |
ω3 |
|
6,9,12,15-октадекатетраеновая кислота, этиловый эфир / 6,9,12,15-octadecatetraenoic acid, ethyl ester |
ω3 |
|
6,9,12,15-октадекатетраеновая кислота / 6,9,12,15-octadecatetraenoic acid |
ω3 |
|
6,9,12-гексадекатриеновая кислота / 6,9,12-hexadecatrienoic acid |
ω3 |
|
6-октадеценовая кислота, этиловый эфир / 6-octadecenoic acid, ethyl ester |
ω11 |
|
6-октадеценовая кислота / 6-octadecenoic acid |
ω11 |
|
7,10,13,16,19-докозагексаеновая кислота, бутиловый эфир / 7,10,13,16,19-docosahexaenoic acid, butyl ester |
ДГК / DНА |
|
7,10,13,16,19-докозапентаеновая кислота метиловый эфир / 7,10,13,16,19-docosapentaenoic acid methyl ester |
ДПК / DPА |
|
7-метил-6-гексадеценовая кислота / 7-methyl-6-hexadecenoic acid |
ω9 |
|
Линолевая кислота, этиловый эфир / Linoleic acid, ethyl ester |
ω6 |
|
Линолевая кислота / Linoleic acid |
ω6 |
|
Пальмитолеиновая кислота, этиловый эфир / Palmitoleic acid, ethyl ester |
ω7 |
|
Пальмитолеиновая кислота / Palmitoleic acid |
ω7 |
|
Олеиновая кислота, этиловый эфир / Oleic acid, ethyl ester |
ω9 |
|
Олеиновая кислота / Oleic acid |
ω9 |
|
Деканоевая кислота / Decanoic acid |
НЖК / SFA |
|
Додеканоевая кислота / Dodecanoic acid |
НЖК / SFA |
|
Эйкозановая кислота / Eicosanoic acid |
НЖК / SFA |
|
Эйкозановая кислота, пропиловый эфир / Eicosanoic acid, propyl ester |
НЖК / SFA |
|
Маргариновая кислота / Margaric acid |
НЖК / SFA |
|
Маргариновая кислота, этиловый эфир / Margaric acid, ethyl ester |
НЖК / SFA |
|
Пальмитиновая кислота / Palmitic acid |
НЖК / SFA |
|
Метилникотинат / Methyl nicotinate |
– |
|
Стеариновая кислота, этиловый эфир / Stearic acid, ethyl ester |
НЖК / SFA |
|
Стеариновая кислота / Stearic acid |
НЖК / SFA |
|
Каприловая кислота / Caprylic acid |
НЖК / SFA |
|
Пантолактон / Pantolactone |
– |
|
Пентадеканоевая кислота / Pentadecanoic acid |
НЖК / SFA |
|
Миристиновая кислота, этиловый эфир / Myristic acid, ethyl ester |
НЖК / SFA |
|
Миристиновая кислота / Myristic acid |
НЖК / SFA |
|
12-метил-тридеканоевая кислота / 12-methyl-tridecanoic acid |
НЖК / SFA |
|
Тридеканоевая кислота / Tridecanoic acid |
НЖК / SFA |
|
9,12,15-октадекатриеновая кислота (α-линоленовая) / 9,12,15-octadecatrienoic acid (α-linolenic) |
ω3 |
|
5,8,11,14-эйкозатетраеновая кислота (арахидоновая) / 5,8,11,14-eicosatetraenoic acid (arachidonic) |
ω6 |
|
8,11,14,17-эйкозатетраеновая кислота / 8,11,14,17-eicosatetraenoic acid |
ω3 |
|
5,8,11,14,17-эйкозапентаеновая кислота, изопропиловый эфир / 5,8,11,14,17-eicosapentaenoic acid, isopropyl ester |
ЭПК / ЕРА |
|
15-тетракозеновая кислота кислота / 15-tetracosenoic acid acid |
ω9 |
|
9-транс-12-транс-октадекадиеновая кислота / 9-trans-12-trans-octadecadienoic acid |
ω6 |
|
5,8,11,14,17-эйкозапентаеновая кислота, бутиловый эфир / 5,8,11,14,17-eicosapentaenoic acid, butyl ester |
ЭПК / ЕРА |
|
9-цис, 11-транс-октадекадиеновая кислота, этиловый эфир / 9-cis,11-trans-octadecadienoic acid, ethyl ester |
ω6 |
|
5,8,11,14-эйкозатетраеновая кислота (арахидоновая), этиловый эфир / 5,8,11,14-eicosatetraenoic acid (arachidonic), ethyl ester |
ω6 |
|
7,10,13,16,19-докозапентаеновая кислота, изопропиловый эфир / 7,10,13,16,19-docosapentaenoic acid, isopropyl ester |
ω3 |
|
13-докозеновая кислота, этиловый эфир / 13-docosenoic acid, ethyl ester |
ω9 |
Примечание: НЖК – насыщенные жирные кислоты; ДГК – докозагексаеновая кислота; ЭТК – эйкозатетраеновая кислота; ЭПК – эйкозапентаеновая кислота; ДПК – докозапентаеновая кислота.
Note: SFA – saturated fatty acids; DHA – docosahexaenoic acid; ETA – eicosatetraenoic acid; EPA – eicosapentaenoic acid; DPA – docosapentaenoic acid.
Для характеристики состава каждого из исследованных препаратов ω3-ПНЖК использовался профиль, включающий все 55 соединений, перечисленных в таблице 2. Помимо отдельных соединений, на основе уровней отдельных соединений и их химических типов (перечислены в крайней правой колонке таблицы 2) для характеризации каждого из исследованных образцов были рассчитаны суммарные характеристики жирнокислотного состава: общее содержание ω3, ω6, ω7, ω9, ω11-ПНЖК, ЭПК, ДГК, ЭПК+ДГК, других ω3 (Др.ω3), насыщенных жирных кислот (НЖК).
Как и в работе [15], мы также использовали «коэффициент стандартизации» (КСТ), оценивающий соответствие реально измеренных уровней ω3-ПНЖК содержанию ω3-ПНЖК, заявляемому производителем. КСТ рассчитывается как композиция 4 компонентов:
КСТ (%) = 1 – ω3соотв – ЭПКсоотв – ДГКсоотв – Др.ω3соотв, где
- ω3соотв = ω3заявл (%) – ω3изм (%) – соответствие заявленного общего содержания ω3-ПНЖК измеренному; если препарат содержит больше ω3, чем заявлено, то это увеличивает ω3соотв;
- ЭПКсоотв = ЭПКзаявл (%) – ЭПКизм (%), если заявлено содержание ЭПК; если нет, то назначается «штрафной процент» (мы использовали величину в 15 %, которая отражает среднее содержание ЭПК в слабо стандартизированных препаратах);
- ДГКсоотв = ДГКзаявл (%) – ДГКизм (%), если заявлено содержание ДГК, в противном случае – «штрафной процент» (10 %);
- Др.ω3соотв = |Др.ω3заявл – Др.ω3изм| – абсолютное значение разности между заявленным измеренным содержанием других ω3-ПНЖК, которое определяется как разница между общим содержанием ω3 и суммарным содержанием ЭПК+ДГК.
Статистический анализ / Statistical analysis
Для стандартной обработки результатов исследования использовались методы математической статистики, включающие расчет числовых характеристик случайных величин, проверки статистических гипотез с использованием параметрических и непараметрических критериев, корреляционного и дисперсионного анализа. Сравнение прогнозируемых и наблюдаемых частот встречаемости исследуемых признаков проводилось с помощью критерия χ², T-критерий Вилкоксона–Манна–Уитни и тест Стьюдента в электронных таблицах Microsoft Excel. Помимо стандартных методов статистики, в ходе анализа данных скрининга были использованы новые математические подходы к интеллектуальному анализу данных, основанные на методе метрических сгущений [15].
Результаты / Results
В результате проведения экспериментов были получены хроматограммы для каждого из 10 препаратов. Пики идентифицировались по библиотеке масс спектров NIST 11; пример расшифровки приведен на рисунке 1 (образец препарата с высокой степенью стандартизации Фемибион Наталкер-2 – № 7 в таблице 1).
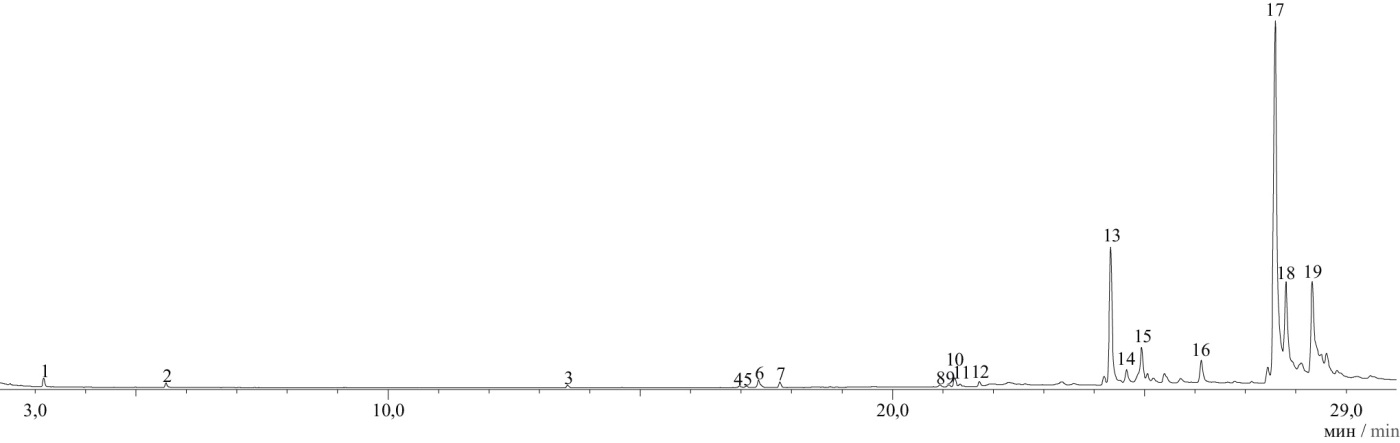
Рисунок 1. Расшифровка хроматограммы препарата омега-3 полиненасыщенных жирных кислот (на примере образца № 7 Фемибион Наталкер-2).
Примечание: пики: 1 – каприловая кислота (насыщенная), 2 – деканоевая кислота (насыщенная), 3 – миристиновая кислота (насыщенная), 4 – 6,9,12,15-гексадекатетраеновая кислота (ω3), 5 – 6,9,12-гексадекатриеновая кислота (ω3), 6 – пальмитолеиновая кислота (ω7), 7 – пальмитиновая кислота (насыщенная), 8 – 6,9,12,15-октадекатетраеновая кислота (ω3), 9 – линолевая кислота (ω6), 10 – олеиновая кислота (ω9), 11 – 6-октадеценовая кислота (ω11), 12 – стеариновая кислота (насыщенная), 13 – 5,8,11,14,17-эйкозапентаеновая кислота (ЭПК), 14 – 5,11,14,17-эйкозатетраеновая кислота (ЭТК), 15 – 11-эйкозеновая к-та (ω9), 16 – 11-эйкозеновая кислота, пропиловый эфир (ω9), 17 – 4,7,10,13,16,19-докозагексаеновая кислота (ДГК), 18 – 7,10,13,16,19-докозапентаеновая кислота, метиловый эфир (ДПК), 19 – 13-докозеновая кислота (ω9).
Figure 1. Decoding the chromatogram of the omega-3 polyunsaturated fatty acids preparation (representative sample No. 7 of Femibion Natalcare-II).
Note: peaks: 1 – сaprylic acid (saturated), 2 – decanoic acid (saturated), 3 – myristic acid (saturated), 4 – 6,9,12,15-hexadecatetraenoic acid (ω3), 5 – 6,9,12-hexadecatrienoic acid (ω3), 6 – palmitoleic acid (ω7), 7 – palmitic acid (saturated), 8 – 6,9,12,15-octadecatetraenoic acid (ω3), 9 – linoleic acid (ω6), 10 – oleic acid (ω9), 11 – 6-octadecenoic acid (ω11), 12 – stearic acid (saturated), 13 – 5,8,11,14,17-eicosapentaenoic acid (EPA), 14 – 5,11,14,17-eicosatetraenoic acid (ETK), 15 – 11-eicosene acid (ω9), 16 – 11-eicosene acid, propyl ether (ω9), 17 – 4,7,10,13,16,19-docosahexaenoic acid (DHA), 18 – 7,10,13,16,19-docosapentaenoic acid methyl ester (DPA), 19 – 13-docosenoic acid (ω9).
В таблице 3 приведены результаты – суммарные характеристики жирнокислотного состава (общее содержание ω3, ω6, ПНЖК, НЖК и др.), вычисленные на основе 55-компонентных профилей жирнокислотного состава. Визуальный анализ данных в таблице 3 указывает на существование экстрактов с очень высоким суммарным содержанием ω3-ПНЖК в форме ЭПК и/или ДГК. Например, содержание ω3-ПНЖК в среднем по всем исследованным препаратам составило 58,2 ± 27,2 % (ЭПК+ДГК = 50,1 ± 26,5 %). Если расположить строки таблицы 3 по возрастанию общего содержания ω3-ПНЖК, то становится очевидным наличие экстрактов с более низким общим содержанием ω3-ПНЖК (Омеганол – 12,59 %, Омегамама – 34,26 % и др.) и экстрактов с весьма высоким содержанием ω3-ПНЖК: Омакор – 97 % ω3-ПНЖК (ЭПК+ДГК = 91,3 %), Фемибион Наталкер-2 – 75 % ω3-ПНЖК (ЭПК+ДГК = 60 %) и др.
Таблица 3. Измеренные содержания жирных кислот (в процентах от массы образца).
Table 3. Measured fatty acid levels (presented as sample weight percentage).
|
N |
Препарат Preparation |
ЭПК EPA |
ДГК DHA |
ЭПК+ ДГК EPA + DHA |
Другие ω3 Other ω 3 |
Всего ω3 Total ω3 |
ω6 |
ω7 + ω9 + ω11 |
НЖК SFA |
КСТ SС % |
|
1 |
Омега-3 Доппельгерц® Актив / Omega-3 Doppelherz® Activ |
15,48 |
10,82 |
26,3 |
11,46 |
37,76 |
2,35 |
32,76 |
27,13 |
100,0 |
|
2 |
Рыбий жир-Тева® / Fish oil-Teva® |
16,19 |
10,29 |
26,48 |
13,01 |
39,49 |
1,94 |
31,53 |
27,04 |
119,0 |
|
3 |
Омегатрин® / Omegatrin® |
24,71 |
21,68 |
46,39 |
5,74 |
52,13 |
10,57 |
27,82 |
9,48 |
141,0 |
|
4 |
Омега-3 концентрат® / Omega-3 concentrate® |
32,1 |
26,18 |
58,28 |
8,37 |
66,65 |
1,56 |
21,86 |
9,93 |
105,0 |
|
5 |
Омегамама® / Omegamama® |
7,78 |
22,31 |
30,09 |
4,17 |
34,26 |
1,6 |
28,3 |
35,84 |
109,0 |
|
6 |
Омеганол® / Omeganol® |
0 |
10,72 |
10,72 |
1,87 |
12,59 |
15,44 |
46,33 |
25,64 |
110,0 |
|
7 |
Фемибион® Наталкер-2 / Femibion® Natalcare II |
13,43 |
46,03 |
59,46 |
16,03 |
75,49 |
0,18 |
22,27 |
2,06 |
138,0 |
|
8 |
Омакор® / Omacor® |
46,49 |
44,76 |
91,25 |
5,76 |
97,01 |
0,55 |
1,61 |
0,83 |
113,0 |
|
9 |
Солгар® Oмега-3 950 мг / Solgar® Omega-3 950 mg |
36,5 |
36,08 |
72,58 |
5,37 |
77,95 |
3,32 |
12,83 |
5,9 |
112,0 |
|
10 |
Омега-3 ВкусВилл® / Omega-3 VkusVill® |
55,4 |
23,99 |
79,39 |
9,16 |
88,55 |
4,98 |
5,11 |
1,27 |
97,0 |
Примечание: ЭПК – эйкозапентаеновая кислота; ДГК – докозагексаеновая кислота; НЖК – насыщенная жирная кислота; КСТ – коэффициент стандартизации (отличие состава от заявляемого состава).
Note: ЕРА – eicosapentaenoic acid; DHA – docosahexaenoic acid; SFA – saturated fatty acid; SС – standardization coefficient (difference in the determined vs. declared composition).
Изученные суммарные характеристики жирнокислотного состава в существенной степени коррелируют друг с другом. Корреляционный анализ между заявленными и измеренными показателями жирнокислотного состава (рис. 2) показал высоко достоверные и выраженные прямые корреляции (положительные значения коэффициента корреляции r) между заявленным и измеренным процентным содержанием ЭПК (r = 0,91), ДГК (r = 0,87), ЭПК+ДГК (r = 0,87) и общим количеством ω3-ПНЖК (r = 0,90). Таким образом, в целом по выборке заявляемые производителями показатели содержания ω3-ПНЖК соответствуют полученным результатам.
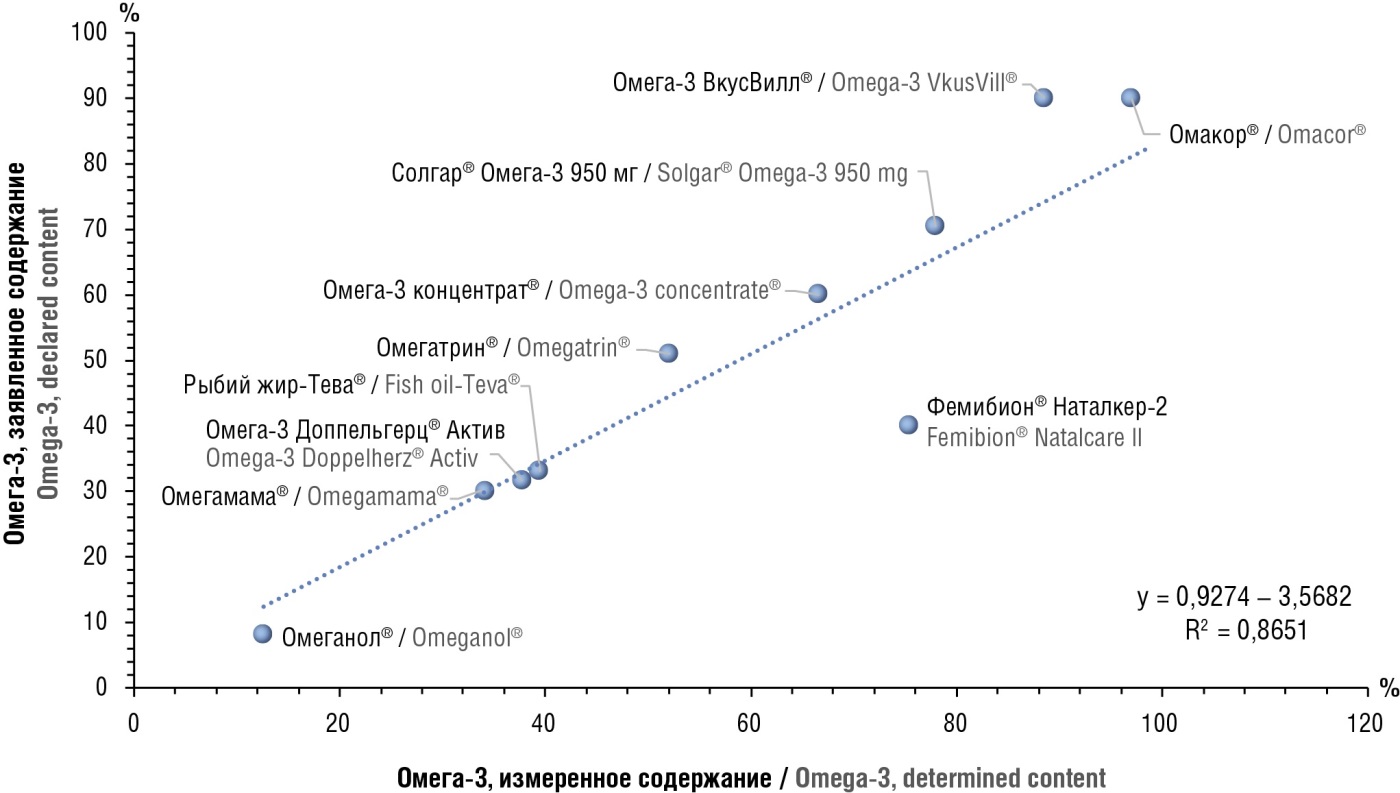
Рисунок 2. Примеры корреляций между заявленными и измеренными значениями различных суммарных показателей жирнокислотного состава.
Figure 2. Representative correlations between the declared and determined values of various total fatty acid composition parameters.
При оценке препаратов ω3-ПНЖК с точки зрения нутрициальной поддержки той или иной группы пациентов важно оценить относительное содержание ЭПК и ДГК. Например, для кардиопротекции наибольший интерес представляет именно ЭПК и ее производные (этиловые, бутиловые эфиры). В то же время для нутрициальной поддержки беременности и для нормофизиологического развития центральной нервной системы плода (и, впоследствии, ребенка) важно относительное содержание в препарате ДГК (так как именно депо ДГК истощается в мембранах эритроцитов, которые усиленно переносят ДГК к плоду) [22]. Среди исследованных препаратов наиболее высоким относительным содержанием ДГК отличались именно препараты ω3-ПНЖК, предназначенные для беременных (Фемибион Наталкер-2 и др., рис. 3).
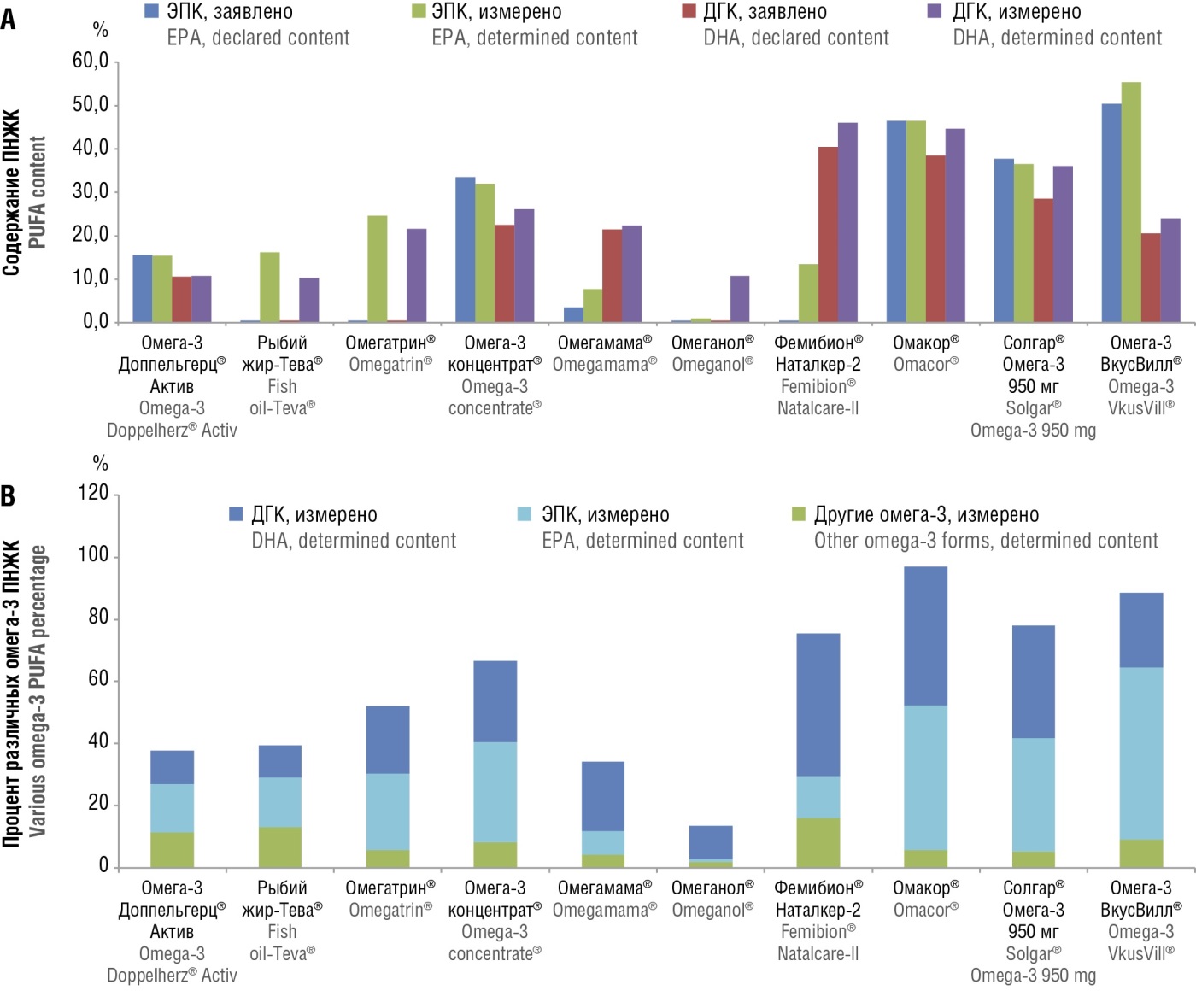
Рисунок 3. Относительное содержание эйкозапентаеновой кислоты (ЭПК) и докозагексаеновой (ДГК) кислоты в исследованных препаратах: А – процентное содержание полиненасыщенных жирных кислот (ПНЖК); В – процент различных омега-3 полиненасыщенных жирных кислот (ω3-ПНЖК).
Figure 3. Relative content of eicosapentaenoic acid (EPA) and docosahexaenoic (DHA) acid in the studied preparations: A – polyunsaturated fatty acid (PUFA) percentage; B – percentage of various оmega-3 polyunsaturated fatty acids (ω3-PUFA).
Для оценки качества препаратов ω3-ПНЖК в целом и для нахождения сходств и отличий между исследованными образцами препаратов необходимо использовать все показатели профиля жирнокислотного состава. В результате проведения хроматографического анализа каждый препарат был представлен вектором из 55 позиций, соответствующих веществам в таблице 2. В рамках фармакоинформационного профилирования данные по составу исследуемых препаратов были спроецированы на плоскую диаграмму, отражающую расстояния между всеми исследованными парами препаратов. С использованием метрики Колмогорова–Смирнова в приложении к этим 55-мерным векторам мы рассчитали «расстояния» между препаратами, исследовали наличие кластеров и представили полученные результаты на метрической карте (рис. 4). Диаграмма получена посредством проецирования 55-мерных векторов для каждого соединения на плоскость. Чем больше расстояние между точками, тем больше различия в фармакоинформационных профилях соответствующих соединений. Оси X и Y отражают (в у.е.) некоторые «главные компоненты» состава, которые расшифровываются далее в тексте настоящей статьи. Методом анализа метрических сгущений установлено наличие двух кластеров.
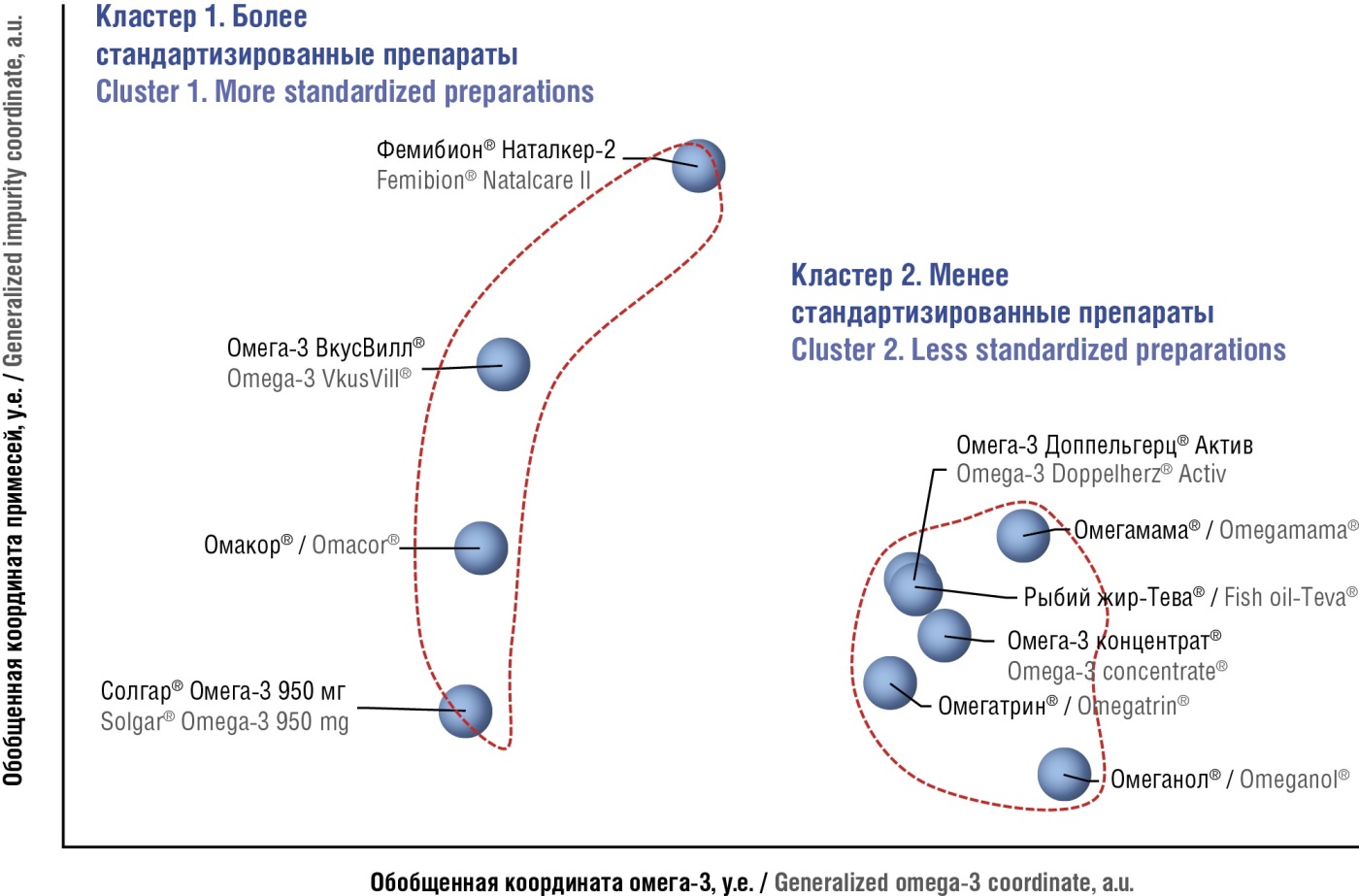
Рисунок 4. Метрическая диаграмма расстояний между жирнокислотными профилями изученных препаратов омега-3 полиненасыщенных жирных кислот.
Figure 4. Metric diagram depicting distances between fatty acid profiles of the studied оmega-3 polyunsaturated fatty acids preparations.
На полученной метрической диаграмме (рис. 4) каждому препарату соответствует одна точка. Горизонтальная ось координат соответствует оценке примесного состава препаратов, вертикальная – содержанию ω3-ПНЖК. Из рисунка 4 очевидно существование двух четко отделяемых кластеров более стандартизированных и менее стандартизированных препаратов ω3-ПНЖК.
Полученные при построении метрической карты на рисунке 4 «условные оси» X и Y должны быть расшифрованы, т. е. сопоставлены содержанию каких-то конкретных веществ. Для установления конкретных показателей биохимического качества стандартизации мы сравнили содержание всех 55 веществ в кластере более стандартизированных препаратов с содержанием этих веществ в кластере менее стандартизированных препаратов. Выявленные достоверные различия приведены в таблице 4.
Таблица 4. Различия жирнокислотного состава препаратов омега-3 полиненасыщенных жирных кислот (площади пиков хроматограмм, %) и маркеры, позволяющие отличать более стандартизированные препараты от менее стандартизированных.
Table 4. Differences in the fatty acid composition of omega-3 polyunsaturated fatty acids preparations (chromatogram peak areas, %) and markers allowing to distinguish more vs. less standardized preparations.
|
N |
Соединение Сompound |
Тип ЖК FA type |
Стандартизированная Standardized |
SD |
Нестандартизированная Not standardized |
SD |
р |
+/– |
|
3 |
13-докозеновая кислота / 13-docosenoic acid |
ω9 |
0,00 |
0,00 |
1,29 |
1,24 |
0,0164 |
– |
|
5 |
13-метилтетрадеканоевая кислота / 13-methyltetradecanoic acid |
НЖК / SFA |
0,00 |
0,00 |
0,12 |
0,09 |
0,0062 |
– |
|
7 |
4,7,10,13,16,19-докозагексаеновая кислота / 4,7,10,13,16,19-docosahexaenoic acid |
ДГК / DHA |
25,68 |
17,03 |
11,32 |
5,29 |
0,0348 |
+ |
|
10 |
5,8,11,14,17-эйкозапентаеновая кислота / 5,8,11,14,17-eicosapentaenoic acid |
ЭПК / EPA |
22,11 |
8,32 |
10,21 |
6,12 |
0,0055 |
+ |
|
11 |
5,8,11,14,17-эйкозапентаеновая кислота, пропиловый эфир / 5,8,11,14,17-eicosapentaenoic acid, propyl ester |
ЭПК / EPA |
8,15 |
9,94 |
0,77 |
0,84 |
0,0487 |
+ |
|
12 |
6,9,12,15-гексадекатетраеновая к кислота / 6,9,12,15-hexadecatetraenoic acid |
ω3 |
0,03 |
0,07 |
1,03 |
1,30 |
0,0449 |
– |
|
15 |
6,9,12,15-октадекатетраеновая кислота / 6,9,12,15-octadecatetraenoic acid |
ω3 |
0,51 |
0,97 |
2,32 |
1,68 |
0,0171 |
– |
|
16 |
6,9,12-гексадекатриеновая кислота / 6,9,12-hexadecatrienoic acid |
ω3 |
0,02 |
0,05 |
0,81 |
0,95 |
0,0348 |
– |
|
18 |
6-октадеценовая кислота / 6-octadecenoic acid |
ω11 |
0,78 |
1,11 |
3,37 |
1,55 |
0,0022 |
– |
|
21 |
7-метил-6-гексадеценовая кислота / 7-methyl-6-hexadecenoic acid |
ω9 |
0,00 |
0,00 |
0,52 |
0,49 |
0,0154 |
– |
|
23 |
Линолевая кислота / Linoleic acid |
ω6 |
0,44 |
0,52 |
3,65 |
3,43 |
0,0240 |
– |
|
25 |
Пальмитолеиновая кислота / Palmitoleic acid |
ω7 |
0,23 |
0,30 |
5,75 |
4,21 |
0,0066 |
– |
|
27 |
Олеиновая кислота / Oleic acid |
ω9 |
2,30 |
2,84 |
13,63 |
10,95 |
0,0169 |
– |
|
29 |
Додеканоевая кислота / Dodecanoic acid |
НЖК / SFA |
0,00 |
0,00 |
0,06 |
0,06 |
0,0112 |
– |
|
30 |
Эйкозановая кислота / Eicosanoic acid |
НЖК / SFA |
0,00 |
0,00 |
0,49 |
0,62 |
0,0392 |
– |
|
32 |
Маргариновая кислота / Margaric acid |
НЖК / SFA |
0,03 |
0,07 |
0,62 |
0,53 |
0,0125 |
– |
|
33 |
Маргариновая кислота, этиловый эфир / Margaric acid, ethyl ester |
НЖК / SFA |
0,09 |
0,16 |
0,62 |
0,79 |
0,0659 |
– |
|
34 |
Пальмитиновая кислота / Palmitic acid |
НЖК / SFA |
0,51 |
0,63 |
11,25 |
7,19 |
0,0037 |
– |
|
37 |
Стеариновая кислота / Stearic acid |
НЖК / SFA |
1,21 |
1,44 |
4,18 |
1,81 |
0,0028 |
– |
|
40 |
Пентадеканоевая кислота / Pentadecanoic acid |
НЖК / SFA |
0,00 |
0,00 |
0,46 |
0,37 |
0,0077 |
– |
|
42 |
Миристиновая кислота / Myristic acid |
НЖК / SFA |
0,16 |
0,17 |
3,53 |
2,68 |
0,0079 |
– |
|
45 |
9,12,15-октадекатриеновая кислота (α-линоленовая) / 9,12,15-octadecatrienic acid (α-linolenic) |
ω3 |
0,41 |
0,49 |
0,00 |
0,00 |
0,0334 |
+ |
|
46 |
5,8,11,14-эйкозатетраеновая кислота (арахидоновая) / 5,8,11,14-eicosatetraenoic acid (arachidonic) |
ω6 |
0,26 |
0,36 |
0,00 |
0,00 |
0,0517 |
+ |
|
47 |
8,11,14,17-эйкозатетраеновая кислота / 8,11,14,17-eicosatetraenoic acid |
ω3 |
0,80 |
0,84 |
0,00 |
0,00 |
0,0231 |
+ |
|
48 |
5,8,11,14,17-эйкозапентаеновая кислота, изопропиловый эфир / 5,8,11,14,17-eicosapentaenoic acid, isopropyl ester |
ЭПК / EPA |
4,60 |
4,80 |
0,00 |
0,00 |
0,0222 |
+ |
|
sum+ |
– |
8,86 |
5,97 |
3,18 |
1,75 |
0,03 |
||
|
sum– |
– |
0,35 |
0,46 |
2,98 |
2,22 |
0,02 |
Примечание: ЖК – жирная кислота; НЖК – насыщенная жирная кислота; ЭПК – эйкозапентаеновая кислота; ДГК – докозагексаеновая кислота; SD – стандартное отклонение; колонка «+/–» обозначает более высокое среднее содержание соответствующего соединения в кластере стандартизированных препаратов, «–» в противном случае; маркер «sum+» – сумма площадей пиков c “+” в колонке «+/–», маркер «sum–» – сумма площадей пиков с “–” в колонке «+/–».
Note: FA – fatty acid; SFA – saturated fatty acid; EPA – eicosapentaenoic acid; DHA – docosahexaenoic acid; SD – standard deviation; the column “+/–” denotes a higher average content of the corresponding compound in the standardized preparations cluster, “–” otherwise; marker “sum+” denotes the sum of the peak areas with “+” in the column “+/–”; marker “sum–” denotes the sum of the peak areas with “–” in the column “+/–”.
В результате проведенного анализа данных было получено несколько вариантов расшифровки осей X, Y диаграммы на рисунке 4. Эти варианты расшифровки представляют собой различные наиболее информативные маркеры жирнокислотного состава, позволяющие максимально точно отличать более стандартизированные препараты ω3-ПНЖК от менее стандартизированных (рис. 5).
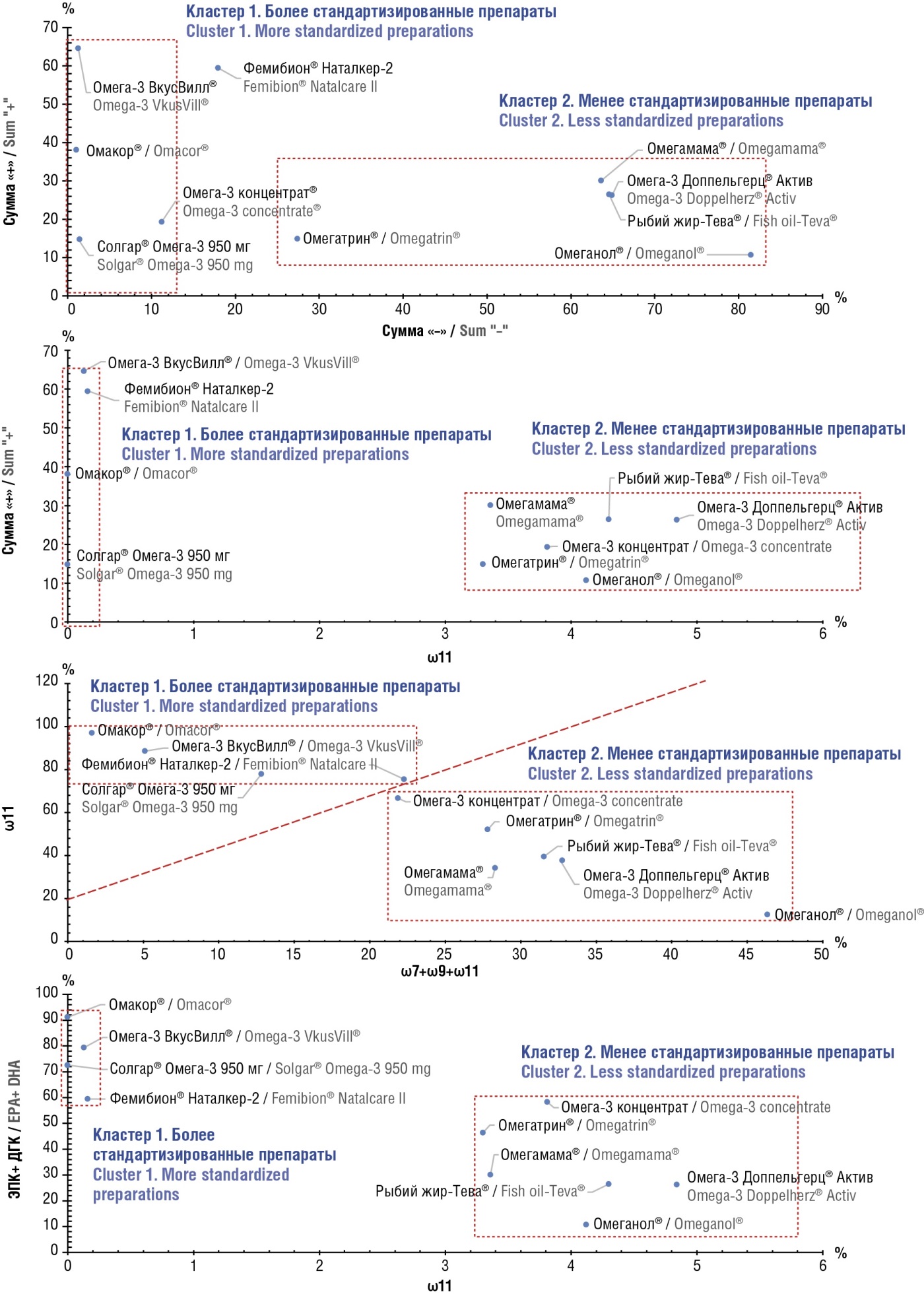
Рисунок 5. Диаграммы состава исследованных препаратов в осях, соответствующих разработанным маркерам жирнокислотного состава.
Примечание: ЭПК – эйкозапентаеновая кислота; ДГК – докозагексаеновая кислота; штрих-пунктирные линии отделяют кластер более стандартизированных препаратов от кластера менее стандартизированных.
Figure 5. Diagrams for the studied preparations composition in the axes corresponding to the developed fatty acid composition markers.
Note: EPA – eicosapentaenoic acid; DHA – docosahexaenoic acid; dash-and-dot lines separate the cluster of more vs. less standardized preparations.
В качестве наиболее информативных маркеров жирнокислотного состава были выбраны 1) маркеры "sum+", "sum–" («sum+» – сумма площадей пиков c “+” в колонке «+/–» таблицы 4, маркер «sum–» – сумма площадей пиков с “–” в колонке «+/–» таблицы 4); 2) общие содержания ω11 или ω7+ω9+ω11; 3) ЭПК+ДГК и общее содержание ω3-ПНЖК.
Приведенные на рисунке 5 диаграммы состава исследованных препаратов в этих координатах наглядно иллюстрируют перечисленные варианты выбора маркеров. При использовании пары маркеров "sum–" и "sum+" кластер стандартизированных препаратов отделяется от кластера нестандартизированных критериями «sum+ > 15 %», «sum– < 12 %». При использовании координат «ω11», «sum+» критерии «ω11 < 0,2 %», «sum+ > 15 %», а при «ω7+ω9+ω11», «ω3» кластеры разделяются критериями «ω7+ω9+ω11 < 22 %», «ω3 > 70 %» (хотя расстояние между кластерами достаточно мало). Хорошее разделение кластеров по обеим координатам очевидно при использовании пары координат («ω11», «ЭПК+ДГК»). В данном случае кластеры разделимы вертикальными линиям и находятся на существенном расстоянии друг от друга, что позволяет сформулировать критерии разделения кластеров: «ω11 < 0,2 %», «ЭПК+ДГК > 57 %».
Следует отметить, что в кластере более стандартизированных препаратов присутствуют не только лекарственный препарат Омакор, но и микронутриентные комплексы, зарегистрированные как «нутриентные биологически активные добавки» (Фемибион Наталкер-2, Солгар омега-3 950 мг и др.). Несмотря на указанное формальное различие в регистрации препарата, содержание ЭПК+ДГК достаточно высоко (более 75 %), а содержание самых нежелательных примесей (НЖК) не превышает 4 %.
В дополнение к маркерам «ЭПК+ДГК» и «ω11», позволяющим классифицировать препараты ω3-ПНЖК как более стандартизированные и менее стандартизированные, мы использовали коэффициент стандартизации (КСТ, %); примеры расчета КСТ (%) были приведены в таблице 4. Значение КСТ (%) позволяет однозначно выделить препараты, в которых содержится больше полезной фракции ПНЖК, чем заявлено производителем. Наибольшими значениям КСТ отличались Фемибион Наталкер-2 и Омегатрин (рис. 6).
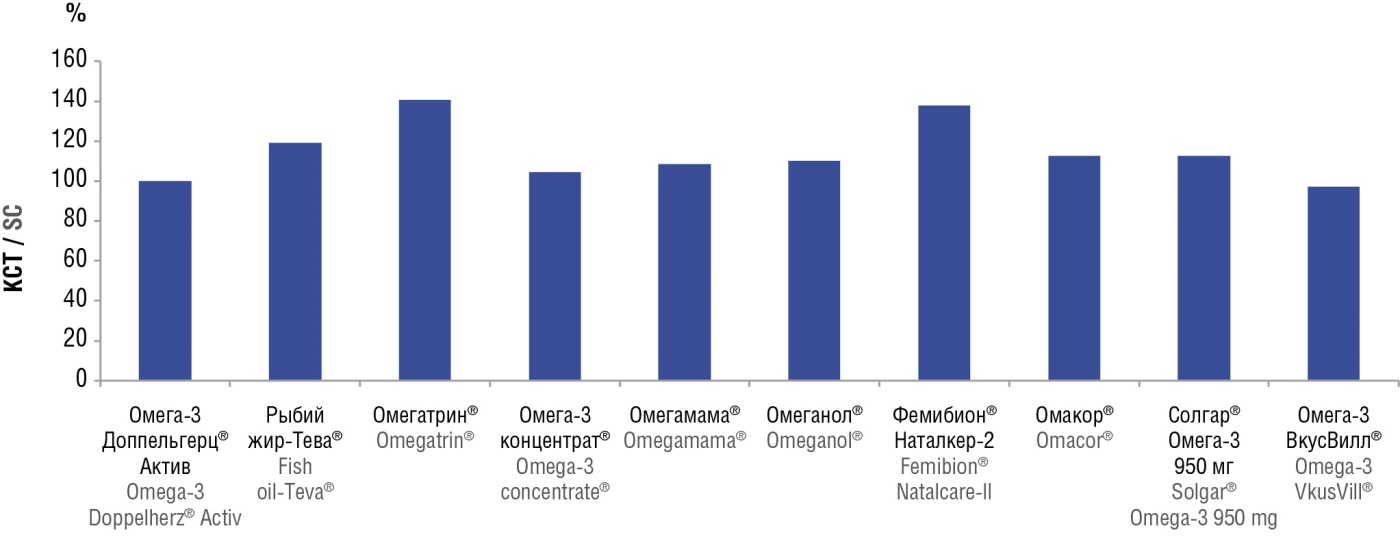
Рисунок 6. Значения коэффициента стандартизации жирнокислотного состава препаратов омега-3 полиненасыщенных жирных кислот.
Примечание: КСТ – коэффициент стандартизации (отличие состава от заявляемого).
Figure 6. Magnitude of the standardization coefficient for the fatty acid composition in omega-3 polyunsaturated fatty acids preparations.
Note: SС – standardization coefficient (difference between determined vs. declared composition).
Обсуждая полученные результаты, следует отметить, что, к сожалению, среди врачей все еще встречается терминологическая путаница, при которой все препараты ω3-ПНЖК называются с использованием такого термина 300–500-летней давности, как «рыбий жир» [7]. Данный термин весьма условен и не соответствует реалиям современной фармакологии ω3-ПНЖК.
Во-первых, препараты, содержащие ω3-ПНЖК, могут изготовляться вообще без использования экстрактов жира рыб (с использованием, например, экстрактов жира морских млекопитающих, экстрактов водорослей, синтетических форм ω3-ПНЖК и др.).
Во-вторых, само использование термина «жир» не совсем грамотно биохимически, так как жирами называются сложные эфиры жирных кислот с глицерином. При реальном приготовлении препаратов ω3-ПНЖК из экстрактов жира рыб зачастую проводится частичное омыление жиров исходного экстракта с удалением глицерина и с последующей этерификацией полученной смеси жирных кислот метиловым, этиловым и другими короткоцепочеными одноатомными спиртами. Полученная таким образом смесь никоим образом не является «жиром» в научном значении этого слова.
В-третьих, и самое главное, препараты ω3-ПНЖК, из какой бы природной субстанции они ни приготовлялись, могут проходить существенную стандартизацию по составу (например, Омакор, Фемибион Наталкер-2 и другие препараты из кластера 1 на рисунке 4).
Полученные нами критерии качества препаратов ω3-ПНЖК позволяют количественно уточнить такие неадекватные термины как «рыбий жир» и проводить своего рода «скрининговую» оценку качества стандартизации таких препаратов.
Заключение / Conclusion
Эффективность препаратов ω3-ПНЖК для беременных в существенной мере зависит от стандартизации содержания экстрактов ω3-ПНЖК по ЭПК, ДГК и по другим видам жирных кислот. В настоящей работе мы провели комплексное исследование состава 10 препаратов ω3-ПНЖК с хроматографическим определением 55 метаболитов жирных кислот и других соединений. Предложены эффективные критерии оценки качества жирнокислотного состава препаратов ω3-ПНЖК.
Выявлены препараты с высокой степенью стандартизации по ω3-ПНЖК (Омакор, Фемибион Наталкер-2 и др.). Однако препарат Омакор фактически не рекомендуется для беременных (см. инструкцию: «Назначать Омакор беременным следует с осторожностью, только после тщательной оценки соотношения риска и пользы… Препарат не должен применяться в период грудного вскармливания»). Такого ограничения не имеется в случае Фемибион Наталкер-2, который предназначен для употребления беременными и в период лактации. Поддержка беременных посредством стандартизированных препаратов ω3-ПНЖК способствует нормальной продолжительности беременности, профилактирует послеродовую депрессию и улучшает развитие зрения, мозга плода, снижает риск аллергических заболеваний новорожденого.
Список литературы
1. Громова О.А., Торшин И.Ю., Гришина Т.Р., Малявская С.И. Омега-3-полиненасыщенные жирные кислоты в поддержке беременности и развития плода: вопросы дозирования. Гинекология. 2020;22(5):61–9. https://doi.org/10.26442/20795696.2020.5.200423.
2. Торшин И.Ю., Громова О.А., Гаранин А.А. Анализ жирнокислотных профилей микронутриентных и фармацевтических препаратов на основе экстрактов омега-3 полиненасыщенных жирных кислот из природных источников. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2025;18(2):199–218. https://doi.org/10.17749/2070-4909/farmakoekonomika.2025.312.
3. Xiong Y., Li X., Liu J. et al. Omega-3 PUFAs slow organ aging through promoting energy metabolism. Pharmacol Res. 2024;208:107384. https://doi.org/10.1016/j.phrs.2024.107384
4. Khan S.U., Lone A.N., Khan M.S. et al. Effect of omega-3 fatty acids on cardiovascular outcomes: A systematic review and meta-analysis. EClinicalMedicine. 2021;38:100997. https://doi.org/10.1016/j.eclinm.2021.100997.
5. Denis I., Potier B., Heberden C., Vancassel S. Omega-3 polyunsaturated fatty acids and brain aging. Curr Opin Clin Nutr Metab Care. 2015;18(2):139–46. https://doi.org/10.1097/MCO.0000000000000141.
6. Thomsen B.J., Chow E.Y., Sapijaszko M.J. The potential uses of omega-3 fatty acids in dermatology: a review. J Cutan Med Surg. 2020;24(5):481–94. https://doi.org/10.1177/1203475420929925.
7. Мареев В.Ю. Отчет о работе Совета экспертов «Актуальность применения этиловых эфиров омега-3 полиненасыщенных жирных кислот (ω-3 ПНЖК, 90 %, 1 г) у постинфарктных пациентов с сопутствующей кардиологической патологией». Сердце: журнал для практикующих врачей. 2016;15(4):301–4. https://doi.org/10.18087/rhj.2016.4.2260
8. Торшин И.Ю., Громова О.А., Кобалава Ж.Д. О репрессиях ω-3 полиненасыщенных жирных кислот адептами доказательной медицины. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2019;12(2):91–114. https://doi.org/10.17749/2070-4909.2019.12.2.91-114.
9. Bjørklund G., Shanaida M., Lysiuk R. et al. Natural compounds and products from an anti-aging perspective. Molecules. 2022;27(20):7084. https://doi.org/10.3390/molecules27207084.
10. Tokumaru K., Imafuku T., Satoh T. et al. Omega 3 fatty acids attenuate the acute kidney injury to CKD transition and renal fibrosis: identification of antifibrotic metabolites. Kidney360. 2024;5(10):1422–34. https://doi.org/10.34067/KID.0000000574.
11. Гаранин А.А., Богачева Т.Е., Громова О.А. Ферроптоз и старение. Фармакокинетика и Фармакодинамика. 2025;(1):17–26. https://doi.org/10.37489/2587-7836-2025-1-17-26.
12. Szucs K.F., Vigh D., Mirdamadi S. et al. Omega-3 fatty acid consumption alters uterine contraction: a comparative study on different breeds of rats. Int J Mol Sci. 2025;26(11):5221. https://doi.org/10.3390/ijms26115221.
13. Li W.J., Lu J.W., Zhang C.Y. et al. PGE2 vs PGF2α in human parturition. Placenta. 2021;104:208–19. https://doi.org/10.1016/j.placenta.2020.12.012.
14. Hashimoto M., Makino N., Inazumi T. et al. Effects of an ω3 fatty acid-biased diet on luteolysis, parturition, and uterine prostanoid synthesis in pregnant mice. Biochem Biophys Res Commun. 2022;589:139–46. https://doi.org/10.1016/j.bbrc.2021.12.029.
15. Arntzen K.J., Brekke O.L., Vatten L., Austgulen R. Reduced production of PGE2 and PGF2 alpha from decidual cell cultures supplemented with N-3 polyunsaturated fatty acids. Prostaglandins Other Lipid Mediat. 1998;56(2–3):183–95. https://doi.org/10.1016/s0090-6980(98)00048-3.
16. Торшин И.Ю., Громова О.А., Зайчик Б.Ц., Ружицкий А.О. Комплексное исследование состава экстрактов жира рыб и количественные критерии для различения стандартизированных экстрактов омега-3 полиненасыщенных жирных кислот. Кардиология. 2020;60(5):47–56.
17. Cholewski M., Tomczykowa M., Tomczyk M. A comprehensive review of chemistry, sources and bioavailability of omega-3 fatty acids. Nutrients. 2018;10(11):1662. https://doi.org/10.3390/nu10111662.
18. Sciotto C., Mjøs S.A. Trans isomers of EPA and DHA in omega-3 products on the European market. Lipids. 2012;47(7):659–67. https://doi.org/10.1007/s11745-012-3672-3.
19. Громова О.А., Торшин И.Ю., Кобалава Ж.Д. и др. Дефицит магния и гиперкоагуляционные состояния: метрический анализ данных выборки пациентов 18-50 лет лечебно-профилактических учреждений России. Кардиология. 2018;58(4):22–35. https://doi.org/10.18087/cardio.2018.4.10106.
20. Торшин И.Ю., Громова О.А., Тетруашвили Н.К. и др. Метрический анализ соотношений коморбидности между невынашиванием, эндометриозом, нарушениями менструального цикла и микронутриентной обеспеченностью в скрининге женщин репродуктивного возраста. Акушерство и гинекология. 2019;(5):156–68. https://doi.org/10.18565/aig.2019.5.156-16819.
21. Торшин И.Ю., Громова О.А., Стаховская Л.В. Анализ 19,9 млн публикаций базы данных PubMed/MEDLINE методами искусственного интеллекта: подходы к обобщению накопленных данных и феномен “fake news”. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2020;13(2):146–63. https://doi.org/10.17749/2070-4909/farmakoekonomika.2020.021.
22. Ghebremeskel K., Min Y., Crawford M.A et al. Blood fatty acid composition of pregnant and nonpregnant Korean women: red cells may act as a reservoir of arachidonic acid and docosahexaenoic acid for utilization by the developing fetus. Lipids. 2000;35(5):567–74. https://doi.org/10.1007/s11745-000-557-3.
Об авторах
О. А. ГромоваРоссия
Громова Ольга Алексеевна - д.м.н., проф. Scopus Author ID: 7003589812.
119333 Москва, ул. Вавилова, д. 44, корп. 2
И. Ю. Торшин
Россия
Торшин Иван Юрьевич - к.ф.-м.н., к.х.н. Scopus Author ID: 7003300274. WoS ResearcherID: C-7683-2018.
119333 Москва, ул. Вавилова, д. 44, корп. 2
И. А. Иловайская
Россия
Иловайская Ирена Адольфовна - д.м.н., проф. Scopus Author ID: 6506067338. WoS ResearcherID: I-1159-2014.
129110 Москва, ул. Щепкина, д. 61/2
А. Н. Громов
Россия
Громов Андрей Николаевич - Scopus Author ID: 7102053964. WoS ResearcherID: C-7476-2018
119333 Москва, ул. Вавилова, д. 44, корп. 2
Что уже известно об этой теме?
► Длинноцепочечные омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК) абсолютно незаменимы для нормального функционирования репродукции, физиологического течения беременности, тормозят старение и фиброзирование тканей почек и печени, миокарда, зрения и мозга, кожи.
► Эйкозапентаеновая кислота (ЭПК) и докозагексаеновая кислота (ДГК) – ключевые формы ω3-ПНЖК, важные для физиологического окончания воспаления и для нейропротекции.
► ДГК способствуют синтезу антифибротических метаболитов, защищающих ткань почек при токсикозе беременных, препятствуя развитию послеродовой депрессии. ω3-ПНЖК являются тонкой модуляцией биосинтеза простагландинов (PG) и, в частности, простагландинов PGE2 и PGF2α. Избыточная активность простагандинов PGE2 и PGF2α, стимулируя приток нейтрофилов и продукцию цитокинов, экспрессию циклооксигеназы-2 (тем самым усиливая свою собственную продукцию), отрицательно сказывается на продолжительности вынашивания.
Что нового дает статья?
► Впервые проведено высокоточное хроматографическое определение жирнокислотного состава 10 препаратов, оценены 55 химических соединений – 55 метаболитов жирных кислот,
► Определено общее содержание ω3, ω6, ω7, ω9, ω11-ПНЖК, ЭПК, ДГК, ЭПК+ДГК.
Как это может повлиять на клиническую практику в обозримом будущем?
► Выявлены препараты с высокой степенью стандартизации по ω3-ПНЖК (Омакор, Фемибион Наталкер-2 и др.). Однако препарат Омакор фактически не рекомендуется для беременных; назначать Омакор беременным следует с осторожностью, только после тщательной оценки соотношения риска и пользы.
► Врачи не должны быть подвержены терминологической путанице, при которой все препараты ω3-ПНЖК называются «рыбий жир»: ω3-ПНЖК могут изготовляться вообще без использования экстрактов жира рыб, с использованием, например, экстрактов жира морских млекопитающих, экстрактов водорослей, льняного масла, синтетических форм ω3-ПНЖК.
► Поддержка беременных посредством стандартизированных препаратов ω3-ПНЖК способствует нормальной продолжительности беременности, профилактирует послеродовую депрессию и улучшает развитие зрения, мозга плода, снижает риск аллергических заболеваний новорожденого.
Рецензия
Для цитирования:
Громова О.А., Торшин И.Ю., Иловайская И.А., Громов А.Н. Комплексный биохимический анализ состава препаратов и биологически активных добавок омега-3 полиненасыщенных жирных кислот для нутрициальной поддержки беременности. Акушерство, Гинекология и Репродукция. 2025;19(5):675-689. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.669
For citation:
Gromova O.A., Torshin I.Yu., Ilovaiskaia I.A., Gromov A.N. Comprehensive biochemical analysis of the omega-3 polyunsaturated fatty acid-based drug and biologically active additive composition for nutritional support of pregnancy. Obstetrics, Gynecology and Reproduction. 2025;19(5):675-689. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2025.669

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.











































