Перейти к:
Как снизить риск венозной тромбоэмболии при приеме комбинированных оральных контрацептивов
https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.422
Аннотация
В обзоре представлены данные по эволюции комбинированных оральных контрацептивов (КОК), их наиболее частым и серьезным нежелательным явлениям, включая венозные тромбоэмболии (ВТЭ). Освещена проблема ВТЭ при приеме КОК и определены риски данного осложнения у пациенток, получающих гормональную контрацепцию. Рассмотрены вопросы основных потребностей женщин при выборе КОК, а также современные возможности удовлетворения этих запросов с помощью новых групп препаратов с высоким профилем эффективности и безопасности. Разобраны частные случаи оптимального выбора КОК у пациенток с определенными сопутствующими патологиями, такими как ожирение, гирсутизм, себорея, алопеция, акне, синдром поликистозных яичников (СПКЯ), фиброзно-кистозная мастопатия, эндометриоз, а также в ситуациях гинекологических оперативных вмешательств. Предложены варианты контрацептивной терапии с учетом индивидуальных желаний женщин (отсутствие набора веса, снижения либидо и т. д.).
Ключевые слова
Для цитирования:
Бицадзе В.О., Хизроева Д.Х., Солопова А.Г., Кварацхелия М.В., Заболотная Д.Ю., Сяося Ч., Третьякова М.В., Цибизова В.И., Гашимова Н.Р., Григорьева К.Н., Гилева М.А., Шкода А.С., Гри Ж., Макацария А.Д. Как снизить риск венозной тромбоэмболии при приеме комбинированных оральных контрацептивов. Акушерство, Гинекология и Репродукция. 2023;17(3):332-342. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.422
For citation:
Bitsadze V.O., Khizroeva J.Kh., Solopova A.G., Kvaratskheliia M.V., Zabolotnaya D.Yu., Xiaoxia Z., Tretyakova M.V., Tsibizova V.I., Gashimova N.R., Grigoreva K.N., Gileva M.A., Shkoda A.S., Gris J., Makatsariya A.D. How to reduce a risk of venous thromboembolism while taking combined oral contraceptives. Obstetrics, Gynecology and Reproduction. 2023;17(3):332-342. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.422
Введение / Introduction
В настоящее время комбинированные оральные контрацептивы (КОК) используются не только в качестве надежного средства защиты от нежелательной беременности, а назначаются и в случаях многих гинекологических заболеваний, связанных с дисбалансом половых гормонов. В связи с ростом потребностей женщин в приеме КОК появилась необходимость создания эффективного препарата, обладающего необходимыми терапевтическими свойствами с минимальными побочными эффектами. Женщины, использующие КОК, отмечают, что наиболее значимыми и негативными для них нежелательными явлениями (НЯ) являются набор массы тела, снижение либидо, выраженные головные боли, венозные тромбоэмболии (ВТЭ). С целью удовлетворения данных потребностей была разработана группа препаратов ПланиЖенс (Фармасинтез-Тюмень, Россия), в которой каждый вариант комбинации гормонов отвечает как конкретному состоянию женской репродуктивной системы и организма в целом, так и определенному «набору» предпочтений потенциальной пациентки.
Эволюция контрацепции / The evolution of contraception
Контрацепция стала радикальным социальным прорывом XX века и изменила жизнь всего общества [1]. Со временем КОК модифицировались в направлении снижения риска сердечно-сосудистых заболеваний и побочных эффектов при одновременном потенциальном усилении желаемых «неконтрацептивных» эффектов [2][3]. Так, эволюция гормональных контрацептивов проходила повышение селективности гестагенов (второе поколение: левоноргестрел; третье поколение: дезогестрел, гестоден; четвертое поколение: дроспиренон); снижение дозы эстрогенов/использование натуральных эстрогенов (15–35 мкг этинилэстрадиола, эстрадиола валерат, 17β-эстрадиол). изменение режима применения (расширенный – 24/4 и 26/2; пролонгированный – 84/7) и пути введения (пероральный – КОК, чрескожный, влагалищный).
Современной тенденцией является своевременная оценка рисков и правильное консультирование женщины при выборе методов контрацепции, что дает возможность адаптировать назначение противозачаточных средств под конкретные индивидуальные потребности женщины с точки зрения эффективности и защиты репродуктивного здоровья [4]. Персонализация гормональной контрацепции подразумевает применение дифференциальных эффектов эстрогенов/гестагенов и расширение индивидуальных возможностей для различных профилей пациентов. Основной задачей производителя становится предупреждение побочных эффектов КОК, что улучшает переносимость и повышает приемлемость контрацепции в сочетании с сохранением неконтрацептивных положительных эффектов для терапевтического применения.
Большое разнообразие средств КОК позволяет каждой женщине сделать свой выбор в пользу того препарата, который будет максимально отвечать ее потребностям и ожиданиям [5]. T. Fait с соавт. провели исследование определенных потребностей и предпочтений женщин в отношении различных составов КОК [6]. По результатам интервьюирования жительниц стран Центральной и Восточной Европы – Россия (n = 300), Польша (n = 100), Чехия (n = 76), Румыния (n = 71), Словакия (n = 68) – была получена достаточно низкая приверженность использованию КОК: средняя продолжительность непрерывного использования препаратов составила 56,2 мес в Словакии, 36,9 мес в Чехии, 23,6 мес в Польше, 21,5 мес в Румынии и 11,4 мес в России. Респонденты сообщили, что наиболее важными (базовыми) характеристиками КОК для них являлись эффективность противозачаточного эффекта (85 %), безопасность (отсутствие влияния на массу тела – 34 %, отсутствие других НЯ – 31 %), обратимость действия (46 %), решение расстройств менструального цикла (46 %). При этом наибольшую озабоченность у респондентов вызывали следующие НЯ: прорывные кровотечения (88 %), прибавка массы тела (65 %, а отдельно в российской популяции – 80 %), гормонально-зависимые новообразования (52 %), ВТЭ (52 %), потеря либидо (49 %), повышение артериального давления и головная боль (45 %), акне (35 %), отеки и масталгия (35 %), перепады настроения (35 %). Наиболее грозным НЯ приема КОК выступает ВТЭ. Многие женщины высказывают свои опасения на консультации у специалиста по поводу риска ВТЭ при назначении длительного режима гормональной контрацепции [6][7].
Венозные тромбоэмболические явления на фоне приема КОК / Venous thromboembolic events paralleled with COCs administration
По данным систематического обзора E.F. van Vlijmen с соат., прием КОК ассоциирован с повышенным риском ВТЭ вследствие изменения коагуляции, антикоагуляции и фибринолиза в протромботическом направлении [7]. Это формирует высокую вероятность ВТЭ у женщин с наследственными нарушениями системы гемостаза (дефицит антитромбина, протеинов С и S, мутации фактора V (FV) Лейден и протромбина G20210A). Основываясь на объединенных результатах 14 исследований, авторы пришли к выводу, что наличие легкой тромбофилии повышало риск ВТЭ у принимающих КОК пациенток почти в 6 раз, при Лейденовской мутации – более чем в 6 раз, при мутации протромбина G20210A – более чем в 5 раз. Тяжелая тромбофилия (в соответствии с объединенными данными трех исследований) повышала вероятность ВТЭ у принимающих КОК более чем в 7 раз. Частота ВТЭ у женщин с легкой тромбофилией (мутация Лейдена и протромбина G20210A), получающих гормональные препараты, составила от 0,49 (95 % доверительный интервал (ДИ) = 0,18–1,07) до 2,0 (95 % ДИ = 0,3–7,2) против диапазона от 0,19 (95 % ДИ = 0,07–0,41) до 0,0 (95 % ДИ = 0,0–5,5) у женщин без данных мутаций на 100 лет приема КОК. Частота ВТЭ у пациенток с двойной гетерозиготностью или гомозиготностью по мутации Лейдена или протромбина G20210A, принимающих КОК, составила 0,86 (95 % ДИ = 0,10–3,11) по сравнению с 0,19 (95 % ДИ = 0,07–0,41) у женщин без мутаций факторов гемостаза на 100 таблеток контрацептивов в год. В случае же наличия дефицита антитромбина, протеина С или S, частота ВТЭ у получающих КОК составила от 4,3 (95 % ДИ = 1,4–9,7) до 4,62 (95 % ДИ = 2,5–7,9) в сравнении с диапазоном от 0,48 (95 % ДИ = 0,1–1,4) до 0,7 (95 % ДИ = 0,0–3,7) на 100 таблеток в год у лиц, принимающих КОК без дефицита антитромбина и протеинов С и S. Исследователи сделали заключение, что наличие легкой и тяжелой тромбофилии увеличивает риск ВТЭ у принимающих КОК в 6 и 7 раз, соответственно [7].
Однако оценки абсолютного риска тромботических событий показывают, что вклад тяжелых наследственных нарушений гемостаза в риск ВТЭ у принимающих КОК значительно выше (частота ВТЭ составляет 4,3–4,6 на 100 таблеток в год), чем дополнительный риск при легкой тромбофилии (0,49–2,0 на 100 таблеток в год), но с оговоркой, что это оценивалось у пациентов с отягощенным семейным анамнезом. Наличие генетической предрасположенности к семейной тромбофилии увеличивает вероятность ВТЭ в 2–3 раза [5–7].
Morimont с соавт. в своем обзоре рассмотрели многочисленные стратегии, которые применялись для снижения тромботического риска, связанного с использованием КОК [8]. Основной причиной ВТЭ считается доза входящего в КОК этинилэстрадиола. Для уравновешивания эффектов эстрогена синтезировали новые прогестины (например, дезогестрел или гестоден), но желаемого эффекта достичь не получилось ввиду их низкой андрогенной активности в отличие от левоноргестрела. В соответствии с мировой литературой, эстрогены в составе КОК способствуют развитию резистентности к активированному протеину С. Впоследствии Европейское агентство по лекарственным средствам (англ. European Medicines Agency, ЕМА) обновило свои рекомендации по клиническим исследованиям стероидных контрацептивов, в которых рекомендовало оценивать этот биологический маркер. В 2009 г. стали доступны КОК с эстрадиола валератом, который, как считается, оказывает меньшее влияние на синтез антикоагулянтных протеинов в печени в сравнении с этинилэстрадиолом. В 2021 г. появился новый комбинированный гормональный препарат на основе нативного эстрогена (эстетрола) в сочетании с дроспиреноном. Этот новый КОК продемонстрировал незначительное влияние на протеины С и S в сравнении с КОК на основе комбинации дроспиренона с другими эстрогенами.
Специалисты мирового медицинского общества продолжают искать наиболее рациональную и доступную стратегию снижения риска ВТЭ у пациенток, которым рекомендуется назначение КОК. Изначально рассматривалась тактика дополнительных диагностических манипуляций исключительно в случае семейного анамнеза тромбофилий, однако эта стратегия обладала невысокой прогностической значимостью. Одним из вариантов был предложен базовый скрининг протромботического состояния перед выбором методов контрацепции, однако этот способ был сочтен слишком дорогостоящим из-за необходимого количества лабораторных исследований. Интересной альтернативой представляется диагностика резистентности фактора V к протеину С, что требует дальнейших исследований [1–8].
Современные решения: препараты из группы ПланиЖенс / Contemporary options: drugs from the PlaniJens group
Инновационная группа гормональных препаратов ПланиЖенс предлагает большой выбор КОК с учетом индивидуальных потребностей каждой конкретной женщины и минимальным риском НЯ, включая ВТЭ. Их механизм действия аналогичен большинству КОК: эстрогеновые и гестагенные компоненты подавляют овуляцию, повышают вязкость секрета шейки матки, препятствуя тем самым попаданию сперматозоидов в полость матки.
Помимо контрацептивного эффекта, представители семейства ПланиЖенс при регулярном приеме оказывают терапевтическое воздействие в случае расстройств менструального цикла. Благодаря восполнению уровня эндогенных гормонов уменьшается болевой синдром и интенсивность менструальноподобных кровотечений, что снижает вероятность возникновения железодефицитных состояний. Препараты с антиандрогенной активностью способствуют бьюти-эффекту, используются для контроля андрогензависимых акне, гирсутизма, себореи, ожирения, повышенного либидо [5][9].
Выбор КОК при нежелании женщины прибавки массы тела / Choice of COCs for woman not wanting to gain body weight
Частым НЯ, с которым боятся столкнуться женщины при назначении КОК, является прибавка массы тела. В открытом многоцентровом рандомизированном клиническом исследовании с участием 768 здоровых женщин, нуждающихся в контрацепции, изучалось влияние гормональных противозачаточных препаратов на массу тела [10]. Сравнивались КОК, содержащие 0,03 мг этинилэстрадиола с дроспиреноном (ЭЭ/дро), с комбинацией 0,03 мг этинилэстрадиола с дезогестрелом (ЭЭ/дезо). На первом визите субъекты были рандомизированы в группу ЭЭ/дро (n = 573) и ЭЭ/дезо (n = 195) в соотношении 3:1. Каждый участник использовал КОК в течение 13 циклов. Последующие визиты проводились на 4-м, 7-м, 10-м и 13-м циклах. При каждом посещении оценивали массу тела, рост и индекс массы тела (ИМТ). Опросник менструального стресса (англ. Menstrual Distress Questionnaire, MDQ) применяли на исходной точке, при 3-м (7-й цикл) и 5-м посещении специалиста (13-й цикл).
Индекс Перля (неэффективность метода) для ЭЭ/дро составил 0,208 на 100 женщин-лет, что ниже, чем у ЭЭ/дезо (0,601 на 100 женщин-лет). Не было никаких существенных различий между группами в отношении характера менструального кровотечения. Согласно подшкале MDQ, уменьшение задержки жидкости в интерстиции и аппетита в межменструальный период, а также отечности и общего недомогания в течение менструального периода наблюдались достоверно больше в группе ЭЭ/дро (–0,297, –0,057, 0,033 и 0,150 соответственно) по сравнению с группой ЭЭ/дезо (–0,108, 0,023, 0,231 и –0,023 соответственно). Другие показатели, которые улучшились в обеих группах, в частности, состояние кожи, уменьшение боли и чувствительности груди были более выражены в группе ЭЭ/дро, чем в группе ЭЭ/дезо. Средняя масса тела увеличилась в группе ЭЭ/дезо (0,57 кг), тогда как в группе ЭЭ/дро наблюдалось снижение средней массы тела (–0,28 кг; p < 0,01). И ЭЭ/дро и ЭЭ/дезо обладают хорошей контрацептивной эффективностью, при этом комбинация ЭЭ/дро оказывала более благоприятное влияние на массу тела и предменструальные симптомы, чем ЭЭ/дезо.
Однако прямое влияние КОК на массу тела не доказано. Предположительно, набор массы тела связан с увеличением аппетита и, соответственно, с употреблением бóльшего количества калорийной пищи, а также с отеками [10]. К тому же известно, что дрос- пиренон за счет антиминералокортикоидного и антиандрогенного эффекта способствует перераспределению жира по женскому типу. Однако дроспиренон является антагонистом минералокортикоидного рецептора, опосредующего дифференцировку висцеральных адипоцитов, и таким образом ингибирует жировую конверсию первичных преадипоцитов человека. Это сильное антиадипогенное свойство позволяет рассматривать дроспиренон в качестве перспективной терапевтической опции чрезмерного отложения жировой ткани и метаболического синдрома [11]. Комбинация дроспиренона (3 мг) с этинилэстрадиолом (0,02 мг) входит в состав микродозированного препарата ПланиЖенс дроспи 20 и обладает антиандрогенным и антиминералокортикоидным действием. В связи с этим ПланиЖенс дроспи 20 больше всего подходит женщинам до 25 лет и после 35 лет; не имевшим ранее опыта приема КОК; с лишней массой тела и отеками. Низкодозированный ПланиЖенс дроспи 30 имеет аналогичный состав, только с чуть большей дозой этинилэстрадиола (0,03 мг) и подходит также женщинам, сталкивающимся с межменструальными кровянистыми выделениями на фоне приема других КОК и не желающим изменений массы тела.
Выбор КОК при страхе потери либидо / Choice of COCs fearing of libido loss
Прием КОК ассоциируется в 15–17 % случаев с нарушением сексуальной функции, в частности, с нарушением возникновения желания и возбуждения [12]. Нарушения сексуальной функции приводят к моральным и физическим проблемам в паре, дисгармоничным бракам и повышению риска развода; в результате женщины могут прекратить прием КОК [13–15]. Влияние гормональных контрацептивов на сексуальную функцию недостаточно изучено и является спорным, также остаются неясными патофизиологические механизмы, приводящие к снижению желания и вульвовагинальной атрофии. В ситуации, когда женщине крайне важно отсутствие влияния на либидо, может быть назначен микродозированный ПланиЖенс гесто 20 (гестоден 0,075 мг и этинилэстрадиол 0,02 мг), а если при этом появляются межменструальные кровотечения или в анамнезе есть вторичная дисменорея, воспалительные заболевания органов малого таза, то рассматриваются низкодозированные КОК, к которым относится ПланиЖенс гесто 30.
Выбор КОК при фиброзно-кистозной мастопатии / Choice of COCs in fibrocystic breast disease
Дезогестрел имеет ряд позитивных эффектов на ткань молочной железы: не влияет на активность ферментов синтеза эстрогенов в молочной железе; угнетает эстроген-индуцированную пролиферативную активность клеток рака молочной железы (линия MCF-7); снижает активность альфа-эстрогеновых рецепторов [16][17]. Применение неандрогенных КОК снижает риск развития фиброзно-кистозной болезни молочных желез (ФКБ), сопровождающейся масталгией.
Основной причиной сопровождающейся масталгией ФКБ выступает персистирующая эстрогенная стимуляция: пролонгированное воздействие эстрадиола, низкое протективное действие прогестерона. КОК ПланиЖенс дезо содержит в составе дезогестрел (0,15 мг) и этинилэстрадиол (0,02 мг – микродозированный; 0,03 мг – низкодозированный). Этот препарат подходит женщинам фертильного возраста (микродозированный в возрасте до 25 и более 35 лет, низкодозированный в 25–35 лет); не имевшим ранее опыта приема КОК. Также в период лактации для улучшения секреции молочных желез или при наличии противопоказаний к использованию эстрогенов пациентке может быть назначен ПланиЖенс лакто с дезогестрелом (0,075 мг) (рис. 1).
Выбор КОК при андрогензависимом акне / Choice of COCs for androgen-dependent acne
У взрослых женщин с акне и подтвержденной гиперандрогенией рекомендуется добавлять КОК к местному или системному лечению акне; использовать любые КОК второго и третьего поколения вне зависимости от дозы эстрогена и прогестинового компонента; добавлять спиронолактон к КОК у женщин с умеренной или тяжелой гиперандрогенной формой акне, не поддающейся обычному лечению. Хотя все КОК теоретически эффективны при угревой болезни, следует отдавать предпочтение менее андрогенным прогестинам и дозам эстрогена более 0,02 мг.
Эффект КОК при акне обусловлен снижением экспрессии рецепторов тестостерона (антиандрогены); уменьшением синтеза андрогенов яичниками (подавление продукции лютеинизирующего гормона гипофизом); уменьшением периферического синтеза андрогенов (ингибирование 5-альфа-редуктазы в волосяных фолликулах и коже); снижением уровня свободного тестостерона за счет повышения гормон-связывающего полового глобулина эстрогенами; уменьшением синтеза андрогенов надпочечниками (глюкокортикоиды – снижение уровня адренокортикотропного гормона) [19]. Антиандрогенный эффект позволяет повысить приверженность к КОК у пациенток с андрогенозависимыми симптомами: акне, себореей, гирсутизмом, андрогенной алопецией [20].
Большое разнообразие вариантов КОК из семейства ПланиЖенс отечественной разработки с учетом индивидуальных потребностей и сниженным риском побочных явлений ведет к повышению долгосрочной приверженности терапии [5][9][14][21]. Оптимальным выбором для женщин с акне легкой степени является ПланиЖенс номе. В ПланиЖенс номе входят номегэстрол (2,5 мг) и эстрадиол (1,5 мг). Данный препарат наиболее близок к естественным гормонам и имеет выраженный антиандрогенный эффект. При акне средней и тяжелой степени используются КОК с более выраженным антиандрогенным действием: в этом случае оправдано рекомендовать ПланиЖенс ципро (ципротерона ацетат 2 мг/ЭЭ 0,035 мг), так как ципротерона ацетат обладает наиболее сильным антиандрогенным эффектом (рис. 2).

Рис. 1. Выбор комбинированных оральных контрацептивов для женщин с масталгией (адаптировано из [9][17][18]).
Fig. 1. Choice of combined oral contraceptives for women with mastalgia (adapted from [9][17][18]).
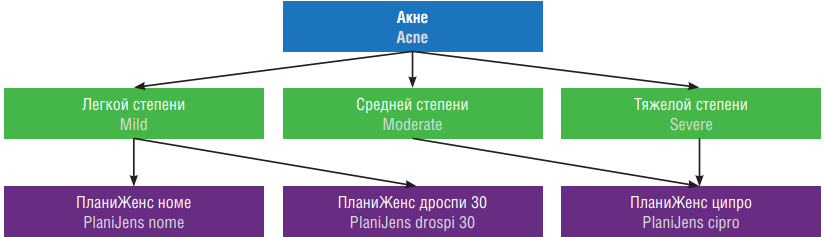
Рис. 2. Выбор комбинированных оральных контрацептивов для женщин с акне (адаптировано из [18]).
Fig. 2. Choice of combined oral contraceptives for women with acne (adapted from [18]).
Выбор КОК при гинекологических оперативных вмешательствах / Choice of COCs in gynecological surgery
Антиандрогенное действие, а также доказанная эффективность при ремиссии эндометриоза наблюдается у диеногеста, который может быть назначен в составе низкодозированного ПланиЖенс дие (диеногест 2 мг и этинилэстрадиол 0,03 мг) женщинам, прошедшим терапию или оперативное вмешательство по поводу эндометриоза. ПланиЖенс лево содержит левоноргестрел (0,15 мг) и этинилэстрадиол (0,03 мг). Левоноргестрел – наиболее изученный прогестаген с хорошим профилем безопасности и переносимости. Для него зафиксированы наименьшие рис- ки развития тромбоэмболических осложнений, что позволяет использовать препарат у женщин после аборта или обширных гинекологических операций вне зависимости от возраста [18].
Выбор КОК при синдроме поликистозных яичников / Choice of COCs for polycystic ovary syndrome
Гиперандрогения при СПКЯ проявляется андрогензависимой дермопатией, ожирением, метаболическими нарушениями, ановуляторными циклами, гирсутизмом, что и становится основной мишенью терапии КОК. Для худых женщин без метаболических нарушений с СПКЯ и дермопатией предлагаются антиандрогенные эстроген-гестагенные препараты (ципротерона ацетат/ЭЭ) и/или антиандрогены (спиронолактон, флутамид, финастерид) [22]. По данным M. Amiri с соавт., более эффективно в снижении гирсутизма длительное (в течение 12 мес) применение КОК с ацетатом ципротерона [23]. В этом случае пациенткам может быть рекомендован препарат ПланиЖенс ципро, имеющий в составе ципротерона ацетат (2 мг) и ЭЭ (0,035 мг).
Для женщин с ожирением, инсулинорезистентностью или сахарным диабетом 2-го типа рекомендованы сенситайзеры инсулина в сочетании с модификацией образа жизни, а также метаболически нейтральные эстроген-гестагенные препараты, например, ПланиЖенс дроспи 20 (дроспиренон 3 мг/ЭЭ 0,02 мг) или ПланиЖенс дроспи 30 (дроспиренон 3 мг/ЭЭ 0,03 мг). Несмотря на большое разнообразие вариантов терапии СПКЯ, существуют «подводные камни» применения КОК у женщин с данной патологией из-за глюкокортикоидных эффектов прогестинов (ципротерона ацетат, медроксипрогестерона ацетат) [24]. Глюкокортикоидная активность может привести к избыточной активации ренин-ангиотензин-альдостероновой системы, повышению сывороточного уровня глюкозы, глюконеогенеза в печени, торможению утилизации глюкозы в тканях. Также при назначении КОК женщинам с СПКЯ повышен риск ВТЭ [25].
Пациентки в возрасте 18–46 лет, получающие КОК и имеющие СПКЯ (n = 43 506), были сопоставлены с женщинами без СПКЯ из контрольной группы (n = 43 506), принимающими оральные контрацептивы. Частота ВТЭ среди женщин с СПКЯ составила 23,7/10 000 человеко-лет, в то время как в контрольной группе она составила 10,9/10 000 человеко-лет. У женщин с СПКЯ, принимающих КОК, относительный риск (ОР) ВТЭ составил 2,14 (95 % ДИ = 1,41–3,24), в то время как у женщин, не использующих КОК, 1,55 (95 % ДИ = 1,10–2,19). Таким образом, ученые обнаружили практически 2-кратное увеличение риска ВТЭ в когорте женщин с СПКЯ, принимавших КОК, и 1,5-кратное увеличение риска ВТЭ среди женщин с СПКЯ, не принимающих оральные контрацептивы. Стоит отметить, что риск развития ВТЭ не зависит от типа прогестагена в составе КОК и снижается после 6 мес приема по данным исследования EURAS [26][27]. Эстрогенный компонент является основным фактором риска ВТЭ на основании отсутствия связи для чисто прогестиновых контрацептивов и повышенного риска для КОК, содержащих более 35 мкг ЭЭ.
Снижение риска ВТЭ при использовании KOK / Reduced VTE risk during COCs use
Открытие основных форм тромбофилии позволило приблизиться к пониманию причин, почему у использующих КОК женщин ВТЭ имела место чаще, чем в общей популяции. В начале 90-х годов XX века помимо дефицита антитромбина III и протеина C стали известны мутации фактора VIII, фактора V Лейден, полиморфизма 4G/5G в гене ингибитора активатора плазминогена и т. п. С ними стали связывать частоту тромбозов в клинической практике. Следует упомянуть и убедительно доказанную роль воспаления и нарушения гемостаза в патогенезе COVID-19, что со своей стороны повышает риск тромбоэмболических нарушений у инфицированных этим крайне распространенным в наши дни заболеванием: ведь ни для одной использующей КОК женщины нельзя исключить вероятность заболеть COVID-19. Поэтому не вызывает сомнений потребность в оценке семейного анамнеза, соответствующих лабораторных исследований на предмет наследственной тромбофилии и своевременной оценке риска повышенного тромбообразования, если женщина планирует начать использовать КОК.
Имеющиеся данные свидетельствуют о том, что КОК, содержащие левоноргестрел или норгестимат, связаны с более низким риском ВТЭ по сравнению с КОК, содержащими дезогестрел, гестоден или дроспиренон. Рекомендуется отдавать предпочтение применению КОК с прогестагенами более низкого риска, чтобы снизить риск ВТЭ.
Более высокие дозы эстрогена (> 50 мкг этинилэстрадиола) связаны с повышенным риском ВТЭ по сравнению с более низкими дозами. Поэтому при выборе средств контрацепции следует отдавать предпочтение КОК с более низкими дозами эстрогена, поскольку они имеют более благоприятный профиль безопасности.
Крайне важно оценить индивидуальные факторы риска развития ВТЭ перед назначением КОК. Следует принимать во внимание возраст, наличие ожирения, курение, персональный или семейный анамнез ВТЭ и другие медицинские состояния. Женщинам с множественными факторами риска могут быть рекомендованы альтернативные варианты контрацепции. Для контроля состояния здоровья пациента и оценки целесообразности постоянного применения КОК рекомендованы регулярные визиты к акушеру-гинекологу.
Заключение / Conclusion
Современная тенденция к персонализированному назначению КОК сформировалась из-за роста потребности женщин в максимально эффективных средствах гормональной контрацепции при снижении рисков побочных явлений. Широкий выбор в группе препаратов ПланиЖенс позволяет реализовать индивидуальные запросы пользователей, что повышает комплаентность и способствует решению ряда гормонально-ассоциированных проблем. Так, для каждой конкретной пациентки может быть подобран определенный КОК с учетом сопутствующей патологии или личного пожелания: комбинации ЭЭ с дроспиреноном для женщин с ожирением или нежеланием набора лишней массы тела; дезогестрел в составе КОК показан при масталгии, являющейся проявлением ФКБ молочных желез; КОК с антиандрогенным эффектом хорошо подходят для лечения андрогензависимых акне, гирсутизма, себореи, алопеции; при ремиссии эндометриоза рекомендуется назначение ЭЭ с диеногестом, а в случае обширных гинекологических операций – ЭЭ с левоноргестрелом, имеющим минимальный риск ВТЭ. Снижение НЯ, включая ВТЭ, и улучшение качества жизни за счет неконтрацептивного действия способствуют увеличению приверженности и длительному использованию КОК, обеспечивая здоровье женщины на долгие годы. КОК из семейства ПланиЖенс продемонстрировали свой высокий профиль безопасности, однако следует учитывать риск ВТЭ при назначении противозачаточных гормональных средств пациенткам с СПКЯ. В этом случае предпочтение следует отдавать чисто прогестиновым препаратам или комбинированным, с содержанием ЭЭ менее 35 мкг. Таким образом, на сегодняшний день благодаря появлению впечатляющего разнообразия КОК с «мультитропным» воздействием, низкой токсичностью и хорошей переносимостью, применение гормональной контрацепции становится доступным все большему количеству женщин.
Снижение риска ВТЭ при использовании КОК требует комплексного подхода, учитывающего их состав, дозировку и индивидуальные особенности пациента. Отдавая предпочтение КОК с прогестагенами более низкого риска, более низким дозам эстрогена и проводя тщательную оценку риска, можно свести к минимуму риск возникновения ВТЭ у применяющих КОК женщин. КОК остаются одним из наиболее эффективных средств контроля рождаемости.
Список литературы
1. Liao P.V., Dollin J. Half a century of the oral contraceptive pill: historical review and view to the future. Can Fam Physician. 2012;58(12):e757–60.
2. Regidor P.A. The clinical relevance of progestogens in hormonal contraception: Present status and future developments. Oncotarget. 2018;9(77):34628–38. https://doi.org/10.18632/oncotarget.26015.
3. Bateson D., Butcher B.E., Donovan C. et al. Risk of venous thromboembolism in women taking the СОСs: A systematic review and meta-analysis. Aust Fam Physician. 2016;45(1):59–64.
4. De Leo V., Musacchio M.C., Cappelli V. et al. Hormonal contraceptives: pharmacology tailored to women's health. Hum Reprod Update. 2016;22(5):634–46. https://doi.org/10.1093/humupd/dmw016.
5. Дикке Г.Б. Просто «таблетка». Шестьдесят лет открытий и достижений, которые изменили мир. Часть I. Гормональная контрацепция: от идеи к совершенству. Фарматека. 2019;27(6):38–45. https://doi.org/10.18565/pharmateca.2020.6.10-17.
6. Fait T., Buryak D., Cirstoiu M.-M. et al. Needs and preferences of women users of oral contraceptives in selected countries in Central and Eastern Europe. Drugs Context. 2018;7:212510. https://doi.org/10.7573/dic.212510.
7. van Vlijmen E.F., Wiewel-Verschueren S., Monster T.B., Meijer K. Combined oral contraceptives, thrombophilia and the risk of venous thromboembolism: a systematic review and meta-analysis. J Thromb Haemost. 2016;14(7):1393–403. https://doi.org/10.1111/jth.13349.
8. Morimont L., Haguet H., Dogné J.M. et al. Combined oral contraceptives and venous thromboembolism: Review and perspective to mitigate the risk. Front Endocrinol (Lausanne). 2021;12:769187. https://doi.org/10.3389/fendo.2021.769187.
9. Михайлова О.И., Мирзабекова Д.Д., Тютюнник В.Л., Кан Н.Е. Выбор метода контрацепции в послеродовом периоде. Зарождение жизни. 2022;(1):40–4. https://doi.org/10.46393/27826384_2022_1_40.
10. Guang-Sheng F., Mei-Lu B., Li-Nan C. et al. Efficacy and safety of the combined oral contraceptive ethinylestradiol/drospirenone (Yasmin) in healthy Chinese women: a randomized, open-label, controlled, multicentre trial. Clin Drug Investig. 2010;30(6):387–96. https://doi.org/10.1007/BF03256908.
11. Caprio M., Antelmi A., Chetrite G. et al. Antiadipogenic effects of the mineralocorticoid receptor antagonist drospirenone: potential implications for the treatment of metabolic syndrome. Endocrinology. 2011;152(1):113–25. https://doi.org/10.1210/en.2010-0674.
12. Wallwiener C.W., Wallwiener L.-M., Seeger H. et al. Prevalence of sexual dysfunction and impact of contraception in female German medical students. J Sex Med. 2010;7(6):2139–48. https://doi.org/10.1111/j.1743-6109.2010.01742.x.
13. Higgins J.A., Hoffman S., Graham S.A., Sanders S.A. Relationships between condoms, hormonal methods, and sexual pleasure and satisfaction: an exploratory analysis from the Women's Well-Being and Sexuality Study. Sex Health. 2008;5(4):321–3. https://doi.org/10.1071/sh08021.
14. Здравомыслов В.И., Анисимова З.Е., Либих С.С. Функциональная женская сексопатология. Пермь: ТОО фирма «Репринт», 1994. 272 с.
15. Sanders S.A., Graham C.A, Bass J.L., Bancroft J. A prospective study of the effects of oral contraceptives on sexuality and well-being and their relationship to discontinuation. Contraception. 2001;64(1):51–8. https://doi.org/10.1016/s0010-7824(01)00218-9.
16. Shamseddin M., De Martino F., Constantin C. et al. Contraceptive progestins with androgenic properties stimulate breast epithelial cell proliferation. EMBO Mol Med. 2021;13(7):e14314. https://doi.org/10.15252/emmm.202114314.
17. Мусина Е.В., Коган И.Ю., Тарасова М.А. Лечебное действие дезогестрела при масталгии у женщин с фиброзно-кистозной болезнью молочных желез. Проблемы репродукции. 2013;(5):42–6.
18. Жуковская И.Г., Хузина Л.Ф. Некоторые аспекты приверженности к комбинированной гормональной контрацепции у молодых женщин. Медицинский совет. 2022;16(16):93–8. https://doi.org/10.21518/2079-701X-2022-16-16-93-98.
19. Ebede T.L., Arch E.L., Berson D. Hormonal treatment of acne in women. J Clin Aesthet Dermatol. 2009;2(12):16–22.
20. Mueck A.O., Sitruk-Ware R. Nomegestrol acetate, a novel progestogen for oral contraception. Steroids. 2011;76(6):531–9. https://doi.org/10.1016/j.steroids.2011.02.002.
21. Nappi R.E., Albani F., Tonani S. et al. Psychosexual well-being in women using oral contraceptives containing drospirenone. Funct Neurol. 2009;24(2):71–5.
22. Ndefo U.A., Eaton A., Green M.R. Polycystic ovary syndrome: a review of treatment options with a focus on pharmacological approaches. P T. 2013;38(6):336–55.
23. Amiri M., Kabir A., Nahidi F. et al. Effects of combined oral contraceptives on the clinical and biochemical parameters of hyperandrogenism in patients with polycystic ovary syndrome: a systematic review and meta-analysis. Eur J Contracept Reprod Health Care. 2018;23(1):64–77. https://doi.org/10.1080/13625187.2018.1435779.
24. Ehrhart-Bornstein M., Lamounier-Zepter V., Schraven A. et al. Human adipocytes secrete mineralcorticoid-releasing factors. Proc Natl Acad Sci USA. 2003;100(24):14211–6. https://doi.org/10.1073/pnas.2336140100.
25. Bird S.T., Hartzema A.G., Brophy J.M et al. Risk of venous thromboembolism in women with polycystic ovary syndrome: a population-based matched cohort analysis. CMAJ. 2013;185(2):E115–20. https://doi.org/10.1503/cmaj.120677.
26. Dinger J.C., Heinemann L.A.J., Kühl-Habich D. The safety of a drosperinone-containing oral contraceptive: final results from the European Active Surveillance study on oral contraceptives based on 142,475 women-years of observation. Contraception. 2007;75(5):344–54. https://doi.org/10.1016/j.contraception.2006.12.019.
27. Bateson D., Butcher B.E., Donovan C. et al. Risk of venous thromboembolism in women taking the СОСs: A systematic review and meta-analysis. Aust Fam Physician. 2016;45(1):59–64.
Об авторах
В. О. БицадзеРоссия
Бицадзе Виктория Омаровна – д.м.н., профессор РАН, профессор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
Scopus Author ID: 6506003478. Researcher ID: F-8409-2017.
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
Д. Х. Хизроева
Россия
Хизроева Джамиля Хизриевна – д.м.н., профессор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
Scopus Author ID: 57194547147. Researcher ID: F-8384-2017.
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
А. Г. Солопова
Россия
Солопова Антонина Григорьевна – д.м.н., профессор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
Scopus Author ID: 6505479504. Researcher ID: Q-1385-2015.
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
М. В. Кварацхелия
Россия
Кварацхелия Маргарита Варламовна – клинический ординатор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
Д. Ю. Заболотная
Россия
Заболотная Диана Юрьевна – клинический ординатор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
Ч. Сяося
Россия
Сяося Чжоу – клинический ординатор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
М. В. Третьякова
Россия
Третьякова Мария Владимировна – к.м.н., врач акушер-гинеколог, ассистент кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
В. И. Цибизова
Россия
Цибизова Валентина Ивановна – к.м.н., врач акушер-гинеколог НИЛ оперативной гинекологии Института перинатологии и педиатрии, врач отделения функциональной ультразвуковой диагностики
197341 Санкт-Петербург, ул. Аккуратова, д. 2
Н. Р. Гашимова
Россия
Гашимова Нилуфар Рамиль кызы – аспирант кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
К. Н. Григорьева
Россия
Григорьева Кристина Николаевна – ассистент кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
М. А. Гилева
Россия
Гилева Мария Алексеевна – клинический ординатор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
А. С. Шкода
Россия
Шкода Андрей Сергеевич – д.м.н., профессор, главный врач
123423 Москва, ул. Саляма Адиля, д. 2/44
Ж.-К. Гри
Франция
Гри Жан-Кристоф – д.м.н., профессор кафедры акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова; профессор гематологии, зав. лабораторией гематологии факультета биологических и фармацевтических наук Университета Монпелье и Университетской больницы Нима, Франция; иностранный член РАН, Москва, Россия.
Scopus Author ID: 7005114260. Researcher ID: AAA-2923-2019.
Россия, 119991 Москва, ул. Большая Пироговская, д. 2, стр. 4;
Франция, 34090 Монпелье, ул. Огюста Бруссоне, д. 163.
А. Д. Макацария
Россия
Макацария Александр Давидович – д.м.н., профессор, академик РАН, зав. кафедрой акушерства, гинекологии и перинатальной медицины Клинического института детского здоровья имени Н.Ф. Филатова; вице-президент Российского общества акушеров-гинекологов (РОАГ); Заслуженный врач Российской Федерации; Почетный профессор Венского Университета
Scopus Author ID: 57222220144. Researcher ID: M-5660-2016.
119991 Москва, ул. Большая Пироговская, д. 2, стр. 4
Рецензия
Для цитирования:
Бицадзе В.О., Хизроева Д.Х., Солопова А.Г., Кварацхелия М.В., Заболотная Д.Ю., Сяося Ч., Третьякова М.В., Цибизова В.И., Гашимова Н.Р., Григорьева К.Н., Гилева М.А., Шкода А.С., Гри Ж., Макацария А.Д. Как снизить риск венозной тромбоэмболии при приеме комбинированных оральных контрацептивов. Акушерство, Гинекология и Репродукция. 2023;17(3):332-342. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.422
For citation:
Bitsadze V.O., Khizroeva J.Kh., Solopova A.G., Kvaratskheliia M.V., Zabolotnaya D.Yu., Xiaoxia Z., Tretyakova M.V., Tsibizova V.I., Gashimova N.R., Grigoreva K.N., Gileva M.A., Shkoda A.S., Gris J., Makatsariya A.D. How to reduce a risk of venous thromboembolism while taking combined oral contraceptives. Obstetrics, Gynecology and Reproduction. 2023;17(3):332-342. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.422

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.











































