Перейти к:
Оценка влияния эмболизации маточных артерий на репродуктивную функцию
https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.410
Аннотация
Введение. Эмболизация маточных артерий (ЭМА) является эффективной малоинвазивной манипуляцией, которая нашла широкое применение в акушерско-гинекологической практике. До сих пор остается спорной целесообразность использования данного метода хирургического лечения у пациенток, имеющих репродуктивные планы. Основными опасениями со стороны клиницистов являются риск развития локальной ишемии эндометрия, что может приводить к привычному невынашиванию, преждевременным родам и патологической плацентации, снижению овариального резерва в результате нарушения адекватного кровоснабжения яичников.
Цель: проанализировать литературные данные о влиянии ЭМА на репродуктивную функцию.
Материалы и методы. Поиск литературы проводили в поисковых базах Web of Science, eLibrary, Scopus, PubMed/MEDLINE. Отбирали статьи за период 1995–2023 гг., посвященные оценке влияния ЭМА на репродуктивную функцию. Поиск статей проводился по ключевым словам и словосочетаниям: «эмболизация», «маточные артерии», «репродуктивная функция»,
«прогноз», «оценка», "embolization", "uterine arteries", "reproductive function", "prognosis", "assessment". Для исключения пропуска подходящих статей методологический фильтр не применялся. Отбирались полнотекстовые источники и литературные обзоры по изучаемой тематике на русском и английском языке. Из обзора были исключены статьи, не имеющие прямого отношения к тематике ЭМА. Чтобы избежать включения дублирующихся публикаций, в случае обнаружения двух и более исследований одних и тех же авторов был изучен период исследования в каждой статье, и если даты совпадали, выбирали самую последнюю по дате публикацию.
Результаты. Имеются ограничения в отношении частоты и исходов беременности у когорты пациенток, которые перенесли ЭМА. Многие вошедшие в обзор статьи с результатами оригинальных исследований и клинические случаи имеют переменные факторы, которые затрудняют прямой анализ или сравнение, такие как возраст, предыдущие самопроизвольные аборты, предшествующие операции на матке, различная техника и профессиональная подготовленность рентген-эндоваскулярных хирургов, неопределенность женщины относительно дальнейших репродуктивных планов и другие формы бесплодия, которые также могут искажать результаты исследований. Кроме того, контролируемые исследования часто имеют небольшие размеры выборки пациентов, что затрудняет получение из них значимой клинической информации.
Заключение. Наступление беременности возможно у женщин после ЭМА, и многие из этих беременностей протекают без осложнений и приводят к успешным родам. Фактический коэффициент фертильности после ЭМА остается неопределенным, но приближается к 38,3 % на основе доступных опубликованных результатов
Для цитирования:
Калинина Н.А., Сулима А.Н., Румянцева З.С., Баскаков П.Н., Калинин В.Д. Оценка влияния эмболизации маточных артерий на репродуктивную функцию. Акушерство, Гинекология и Репродукция. 2023;17(4):476-484. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.410
For citation:
Kalinina N.A., Sulima A.N., Rumyantseva Z.S., Baskakov P.N., Kalinin V.D. Impact assessment of uterine artery embolization on reproductive. Obstetrics, Gynecology and Reproduction. 2023;17(4):476-484. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.410
Введение / Introduction
Эмболизация маточных артерий (ЭМА) является эффективной малоинвазивной манипуляцией, которая активно используется в акушерско-гинекологической практике. Данная манипуляция нашла свое применение в таких клинических ситуациях, как миома [1], послеродовое кровотечение [2], в качестве профилактической процедуры перед акушерской операцией с высоким риском массивного кровотечения [3], аденомиоз [4] и мальформация сосудов матки [5]. Однако в настоящее время использование ЭМА у пациенток, имеющих репродуктивные планы, остается спорным из-за предположительно высокой частоты выкидышей, патологии плацентации и послеродовых кровотечений [6][7]. Также существуют опасения относительно влияния ЭМА на овариальный резерв.
В ряде публикаций была показана возможность нормального течения беременности и послеродового периода у пациенток с ЭМА в анамнезе. O. Serres-Cousine с соавт. представили результаты, в которых 148 беременностей закончились живорождением в 109 случаях у пациенток, перенесших ЭМА [8]. А. Torre с соавт. опубликовали проспективное исследование, в котором была проведена оценка овариального резерва и вероятности наступления беременности после ЭМА с обнадеживающими результатами, но в исследование было включено небольшое число пациенток [9].
Репродуктивный потенциал после ЭМА вызывает множество споров среди ученых. Сложность систематизации данных заключается в том, что случаи беременности и родов после ЭМА представлены недостаточными когортами пациентов, что затрудняет формирование вывода. Особая актуальность данной проблемы заключается в росте обнаружения миомы матки у пациенток репродуктивного возраста [10]. ЭМА является альтернативным минимально инвазивным методом лечения в сравнении с хирургическим и медикаментозным методами коррекции.
Цель: проанализировать литературные данные о влиянии ЭМА на репродуктивную функцию.
Материалы и методы / Materials and Methods
Поиск литературы проводили в поисковых базах Web of Science, eLibrary, Scopus, PubMed/MEDLINE. Отбирали статьи за период 1995–2023 гг., посвященные оценке влияния ЭМА на репродуктивную функцию с использованием алгоритма PRISMA. Поиск статей проводился по ключевым словам на русском и английском языках: «эмболизация», «маточные артерии», «репродуктивная функция», «прогноз», «оценка», "embolization", "uterine arteries", "reproductive function", "prognosis", "assessment". Для исключения пропуска подходящих статей методологический фильтр не применялся. В исследование были включены полнотекстовые источники и литературные обзоры по изучаемой тематике. Из обзора были исключены статьи, не имеющие прямого отношения к тематике ЭМА. Из анализа исключали исследования, которые были представлены 20 и менее пациентами, что обусловлено необходимостью отбора для анализа возможно более репрезентативных данных. Также не включали в обзор работы с недостаточными данными о влиянии ЭМА на репродуктивную функцию. Чтобы избежать включения в литературный обзор дублирующихся публикаций, в случае обнаружения двух исследований одних и тех же авторов был изучен период исследования каждого автора, и если даты совпадали, выбирали самую последнюю по дате публикацию (рис. 1). Отбор работ осуществляли независимо друг от друга 2 исследователя. В случае возникновения разногласий привлекали третьего исследователя.
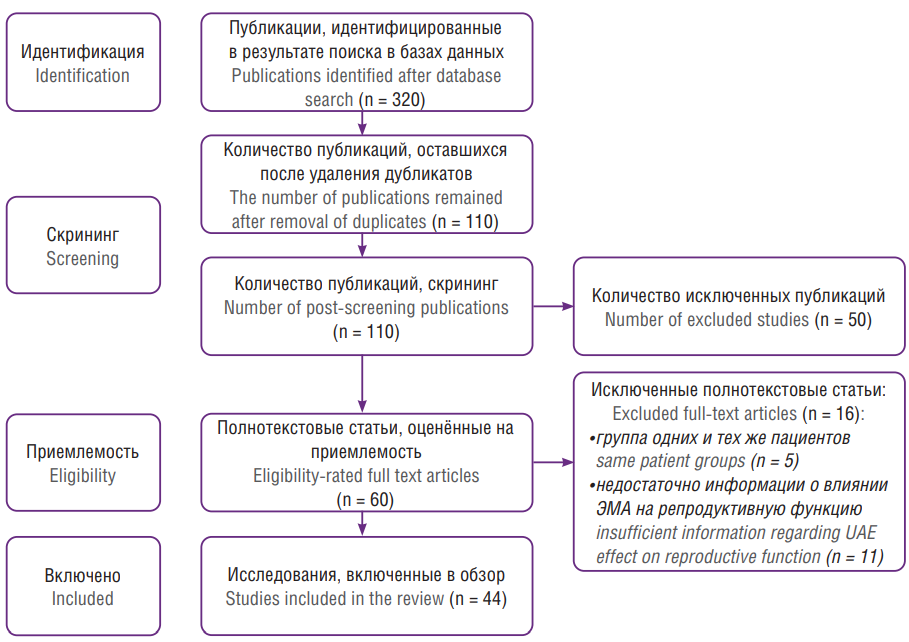
Рисунок 1. Схема отбора публикаций.
Примечание: ЭМА – эмболизация маточных артерий.
Figure 1. Publication selection scheme.
Note: UAE – uterine artery embolization.
Результаты и обсуждение / Results and Discussion
J.H. Ravina c соавт. сообщили о первой ЭМА во Франции в 1995 г. [11], за которой последовали ранние сообщения J.P. Pelage c соавт., показывающие низкую частоту осложнений и эффективность манипуляции [12][13].
ЭМА изначально проводилась с целью предотвращения массивного кровотечения перед миомэктомией или при послеродовом кровотечении. Позже данный метод был признан эффективным в отношении лечения миом матки, как правило, сопровождающихся аномальными маточными кровотечениями (АМК) [14][15]. Ежегодно в мире выполняется порядка 25 тыс. ЭМА [16].
Показания к ЭМА, начиная с первой эмболизации в 1955 г., значительно расширились: сейчас к ним относятся «симптомные миомы», приводящие к АМК, выраженному болевому синдрому, учащенному мочеиспусканию, диспареунии, а также растущие бессимптомные миомы вне зависимости от количества узлов и их расположения [17].
ЭМА выполняется в условиях операционной, оснащенной рентгенодиагностической аппаратурой, с помощью пункции бедренной артерии; кроме того, в ряде случаев может применяться трансрадиальный доступ [18], который имеет ряд преимуществ: отсутствие показаний к строгому постельному режиму в течение 24 ч после манипуляции, уменьшение времени оборота койки, снижение частоты осложнений в месте доступа и уменьшение времени лучевой нагрузки [19][20]. В ходе эмболизации просвет маточных артерий обтурируют частицами поливинилового спирта или трисакрил-желатиновыми микросферами. Дополнительно могут быть использованы металлические спирали [21–23].
Согласно действующим клиническим рекомендациям Министерства здравоохранения Российской Федерации (2020), ЭМА рекомендуется выполнять как альтернативный метод лечения миомы матки у пациенток, не планирующих беременность [10]. Однако в ряде публикаций была показана возможность нормального течения беременности после выполнения ЭМА. Данные работы касались небольшой выборки пациентов и короткого периода наблюдения [8][24][25]. Приблизительные показатели фертильности после миомэктомии оцениваются в 53,6–55,9 % [26], но показатели фертильности после ЭМА до сих пор не были эффективно определены количественно.
Влияние на вероятность зачатия, самопроизвольного аборта, преждевременных родов и кесарева сечения / Influence on likelihood of conception, spontaneous abortion, premature birth and caesarean section
Мировое сообщество не пришло к единому мнению относительно влияния ЭМА на наступление беременности и вынашивание. Основным опасением со стороны клиницистов является риск развития локальной ишемии эндометрия, что может приводить к привычному невынашиванию, преждевременным родам и патологической плацентации, снижению овариального резерва в результате нарушения адекватного кровоснабжения яичников.
В рандомизированном клиническом исследовании, опубликованном в журнале Cardiovascular and Interventional Radiology, были представлены данные, что открытая миомэктомия ассоциирована с лучшими репродуктивными результатами в первые 2 года после оперативного лечения. В исследовании сравнивались репродуктивные результаты пациенток, пытающимися забеременеть после ЭМА (n = 26), с женщинами, желающими забеременеть после лапароскопической или открытой миомэктомии (n = 40). Более высокие показатели беременности и родов при заметно более низком уровне абортов регистрировали у женщин после миомэктомии [27].
Однако стоит принять во внимание, что миомы матки способны самостоятельно приводить к выше- описанным осложнениям в результате деформации полости матки, местного изменения сократимости миометрия и локального нарушения кровоснабжения [28]. Так, систематический обзор, проведенный Н. Homer и Е. Saridogan, показал, что у беременностей после ЭМА и у беременностей, протекавших на фоне миомы матки, наблюдались сходные показатели преждевременных родов, синдрома задержки развития плода и неправильного предлежания плода; в то же время у беременностей после ЭМА был повышенный риск выкидыша, кесарева сечения (КС) и послеродового кровотечения [6]. В другом ретроспективном многоцентровом исследовании А. Hirst с соавт. обнаружили, что показатели фертильности и выкидышей были одинаковыми у женщин соответствующего возраста, которые имели в анамнезе ЭМА, и теми, кто предпочел не получать никакого лечения [29].
Авторы сообщали, что ЭМА может вызывать ишемию и некроз эндометрия, потенциально сопровождающиеся аномальной плацентацией, с последующим нарушением маточно-плацентарного обмена и возможным ограничением внутриутробного роста [30], приращением плаценты (placenta accreta) [31], врастанием плаценты (placenta increta) [32] и предлежанием плаценты [33]. Ведущим фактором в данных исследованиях выступало повреждение эндомиомет- рия. Однако ни в одном из исследований не проводилась макро- или микроскопическая оценка после ЭМА для подтверждения причинно-следственной связи данных осложнений.
Так, в исследовании, проведенном Г.П. Титовой с соавт., показано, что после ЭМА наиболее выраженные участки ишемии были выявлены непосредственно в узлах миомы, что проявлялось некротическими изменениями очагового характера, для которых не было характерно демаркационное воспаление. Асептическое воспаление затрагивало миометрий только в случаях крупномасштабного некроза миомы. Также авторы отмечают отсутствие тромбов в просвете артерий при использовании спиралей в протоколах ЭМА [34].
В 2021 г. в American Journal of Obstetrics and Gynecology вышла работа, в которой были получены следующие данные: в исследовании приняли участие 363 пациентки, 158 из которых имели репродуктивные планы. После выполнения ЭМА у 102 пациенток из 158 (65 %) наступила хотя бы одна беременность. Показатель самопроизвольного прерывания беременности составил 17,57 % [8], он аналогичен результату исследования G. Pron с соавт. [25]. Данный показатель самопроизвольного прерывания беременности после ЭМА намного ниже, чем в других исследованиях [27][29]. Частота КС после ЭМА была высокой – 46,8 %, в то время как частота встречаемости КС в популяции составляет 21,0 % [35][36]. Рекомендуемым сроком между выполнением ЭМА и наступлением беременности является 6 мес [37].
По данным Ю.Э. Доброхотовой с соавт., в группе пациенток с ЭМА в анамнезе частота выполнения операции КС в плановом и экстренном порядке сопоставима с общепопуляционными показателями, что подтверждает возможность физиологичного течения беременности после ЭМА [38].
В Онтарио было проведено проспективное многоцентровое исследование, в котором приняли участие 555 пациенток в возрасте 21 до 41 лет, имевших в анамнезе ЭМА. Результаты исследования также продемонстрировали благоприятные репродуктивные исходы: в 50 % случаях – физиологические роды и нормальный рост плода; тем не менее в 4 наблюдениях произошел самопроизвольный аборт, также отмечались 3 случая массивного послеродового кровотечения из-за патологии плаценты, 4 случая преждевременных родов. Стоит учесть, что средний возраст пациенток при родах составлял 36 лет. В группе исследования 31 % пациенток были моложе 40 лет, а 16 % участниц были потеряны для наблюдения через 2 года. Ограничения исследования включали неопределенность желаемой беременности и использования контрацепции [39].
К. Karlsen с соавт. провели анализ 17 исследований, которые включали 989 пациенток. Авторы пришли к выводу, что у пациенток, которым была выполнена ЭМА, частота наступления беременности была ниже, а частота выкидышей выше по сравнению с женщинами после консервативной миомэктомии [40].
Другое ретроспективное исследование, сравнивающее 53 беременности после ЭМА с 139 беременностями после миомэктомии (группы исследования не были скорректированы), выявило более высокую частоту преждевременных родов и неправильного предлежания в когорте ЭМА: отношение шансов (ОШ) = 6,2; 95 % доверительный интервал (ДИ) = 1,4–27,7 и ОШ = 4,3; 95 % ДИ = 1,0–20,5 соответственно [41].
В литературе описываются ограничения в отношении частоты и исходов беременности у пациенток репродуктивного возраста, которые перенесли ЭМА. Многие пациентки, включенные в существующие исследования и отчеты о случаях, имеют переменные факторы, которые затрудняют прямой анализ или сравнение, такие как возраст, предыдущие самопроизвольные аборты, предшествующие операции на матке, различная техника и профессиональная подготовленность рентгенэндоваскулярных хирургов, неопределенность женщины относительно дальнейших репродуктивных планов и другие формы бесплодия, которые также могут искажать результаты исследований. Кроме того, наиболее хорошо контролируемые исследования часто имеют небольшие размеры выборки пациентов, что затрудняет получение из них значимой клинической информации.
Влияние на овариальный резерв / Effect on ovarian reserve
При выполнении ЭМА важным моментом является адекватная оценка анатомических особенностей кровоснабжения органов малого таза. Особый интерес представляет наличие маточно-яичниковых анастомозов. Так, по данным В.Г. Бреусенко с соавт., подобные анастомозы ангиографически визуализируются только в 25 % случаев. Авторы пришли к заключению, что «…только при наличии двусторонних анастомозов, которые имеют коллатерали с фундальной артерией, наблюдается контралатеральный сброс эмболов, препятствующий полной эмболизации перифиброидного сплетения» [42]. Наличие двусторонних маточно-яичниковых анастомозов может влиять на функцию яичника посредством нарушения кровотока в яичниковой артерии. В течение 3–6 мес после оперативного лечения кровоток в яичнике восстанавливается, что может быть связано с редукцией узла и уменьшении им компрессии яичниковой ветви маточной артерии [43].
Гормональный профиль также претерпевает изменения после выполнения ЭМА. М.М. Высоцкий с соавт. провели исследование, включавшее 23 пациентки, у которых в течение первого месяца после выполнения ЭМА наблюдалось значительное снижение содержания стероидных гормонов: синтез Е2 снизился на 60,5 %, антимюллерова гормона – на 65,8 %. При этом синтез гонадотропных гормонов увеличился: фолликулостимулирующего гормона (ФСГ) – на 58,4 %, лютеинизирующего гормона (ЛГ) – на 55,5 %, показатель соотношения ЛГ/ФСГ оставался прежним. Восстановление показателей до дооперационных значений происходит только через 10 мес после оперативного лечения [44].
Заключение / Conclusion
На основании проведенного обзора отечественных и зарубежных литературных источников последних лет можно сделать вывод о том, что ЭМА является эффективной малоинвазивной органосохраняющей манипуляцией, которая активно используется в акушерско- гинекологической практике. Данная операция нашла свое применение в различных клинических ситуациях.
Вопрос о целесообразности использования ЭМА в группе пациенток репродуктивного возраста с нереа- лизованной репродуктивной функцией остается открытым. В литературе описаны ограничения в отношении частоты и исходов беременности у этой когорты пациенток, которые перенесли ЭМА. Однако ясно, что наступление беременности возможно у женщин после ЭМА, и многие из этих беременностей протекают без осложнений и приводят к успешным родам. Фактический коэффициент фертильности после ЭМА остается неопределенным, но приближается к 38,3 % на основе доступных опубликованных результатов.
Таким образом, анализ современной научной литературы, посвященной проблеме применения ЭМА у молодых пациенток с нереализованной репродуктивной функцией, свидетельствует о высокой медицинской и социально-экономической значимости данной проблемы, диктует необходимость дальнейшего изучения механизмов сохранения овариального резерва и фертильности после ЭМА и обусловливает приоритетность поиска дополнительных патогенетически обоснованных лечебных и профилактических мероприятий.
Список литературы
1. Masciocchi C., Arrigoni F., Ferrari F. et al. Uterine fibroid therapy using interventional radiology mini-invasive treatments: current perspective. Med Oncol. 2017;34(4):52. https://doi.org/10.1007/s12032-017-0906-5.
2. Jitsumori M., Matsuzaki S., Endo M. et al. Obstetric outcomes of pregnancy after uterine artery embolization. Int J Womens Health. 2020;12:151–8. https://doi.org/10.2147/IJWH.S236443.
3. Ko H.K., Shin J.H., Ko G.Y. et al. Efficacy of prophylactic uterine artery embolization before obstetrical procedures with high risk for massive bleeding. Korean J Radiol. 2017;18(2):355–60. https://doi.org/10.3348/kjr.2017.18.2.355.
4. Dessouky R., Gamil S.A., Nada M.D. et al. Management of uterine adenomyosis: current trends and uterine artery embolization as a potential alternative to hysterectomy. Insights Imaging. 2019;10(1):48. https://doi.org/10.1186/s13244-019-0732-8.
5. El Shamy T., Amer S.A.K., Mohamed A.A. et al. The impact of uterine artery embolization on ovarian reserve: a systematic review and metaanalysis. Acta Obstet Gynecol Scand. 2020;99(1):16–23. https://doi.org/10.1111/aogs.13698.
6. Homer H., Saridogan E. Uterine artery embolization for fibroids is associated with an increased risk of miscarriage. Fertil Steril. 2010;94(1):324–30. https://doi.org/10.1016/j.fertnstert.2009.02.069.
7. Jegaden M., Bleas C., Debras E. et al. Asherman syndrome after uterine artery embolization: A cohort study about surgery management and fertility outcomes. JMIG. February 20, 2023. https://doi.org/10.1016/jmig2023.02.012.
8. Serres-Cousine O., Kuijper F.M., Curis E., Atashroo D. Clinical investigation of fertility after uterine artery embolization. Am J Obstet Gynecol. 2021;225(4):403.e1–403.e22. https://doi.org/10.1016/j.ajog.2021.05.033.
9. Torre A., Fauconnier A., Kahn V. et al. Fertility after uterine artery embolization for symptomatic multiple fibroids with no other infertility factors. Eur Radiol. 2017;27(7):2850–9. https://doi.org/10.1007/s00330-016-4681-z.
10. Клинические рекомендации. Миома матки. М.: Министерство здравоохранения Российской Федерации, 2020. 32 с. Режим доступа: https://minzdrav.samregion.ru/wp-content/uploads/sites/28/2021/02/mioma-matki.pdf. [Дата обращения: 20.03.2023].
11. Ravina J.H., Herbreteau D., Ciraru-Vigneron N. et al. Arterial embolisation to treat uterine myomata. Lancet. 1995;346(8976):671–2. https://doi.org/10.1016/s0140-6736(95)92282-2.
12. Pelage J.P., Le Dref O., Mateo J. et al. Life-threatening primary postpartum hemorrhage: treatment with emergency selective arterial embolization. Radiology. 1998;208(2):359–62. https://doi.org/10.1148/radiology.208.2.9680559.
13. Pelage J.P., Soyer P., Repiquet D. et al. Secondary postpartum hemorrhage: treatment with selective arterial embolization. Radiology. 1999;212(2):385–9. https://doi.org/10.1148/radiology.212.2.r99jl05385.
14. Hutchins F.L., Worthington-Kirsch R. Embolotherapy for myoma-induced menorrhagia. Obstet Gynecol Clin North Am. 2000;27(2):397–405, viii. https://doi.org/10.1016/s0889-8545(00)80030-3.
15. McLucas B., Adler L., Perrella R. Uterine fibroid embolization: nonsurgical treatment for symptomatic fibroids. J Am Coll Surg. 2001;192(1):95–105. https://doi.org/10.1016/s1072-7515(00)00738-9.
16. Dariushnia S.R., Nikolic B., Stokes L.S., Spies J.B. Quality improvement guidelines for uterine artery embolization for symptomatic leiomyomata. J Vasc Interv Radiol. 2014;25(11):1737–47. https://doi.org/10.1016/j.jvir.2014.08.029.
17. Goodwin S.C., McLucas B., Lee M. et al. Uterine artery embolization for the treatment of uterine leiomyomata midterm results. J Vasc Interv Radiol. 1999;10(9):1159–65. https://doi.org/10.1016/s1051-0443(99)70213-7.
18. Nakhaei M., Mojtahedi A., Faintuch S. et al. Transradial and transfemoral uterine fibroid embolization comparative study: technical and clinical outcomes. J Vasc Interv Radiol. 2020;31(1):123–9. https://doi.org/10.1016/j.jvir.2019.08.016.
19. Антропова Е.Ю., Шарафутдинов Б.М., Рыжкин С.А., Мазитова М.И. Успехи и нерешенные вопросы эмболизации маточных артерий при миоме матки. Российский медико-биологический вестник имени академика И.П. Павлова. 2021;29(4):545–56. https://doi.org/10.17816/PAVLOVJ71390.
20. Гаязов Д.Р., Терегулов А.Ю., Терегулова Л.Е. Сравнительный анализ трансрадиального и трансфеморального сосудистых доступов при проведении эмболизации маточных артерий. Практическая медицина. 2017;(2):119–23.
21. Калмыков Е.Л., Рахимов Ф.Р., Умарзода С.Г., Баратов А.К. Эмболизация маточных артерий при лейомиоме матки: состояние проблемы. Акушерство и гинекология. 2020;(9):18–26. https://doi.org/10.18565/aig.2020.9.18-26.
22. Das R., Wale A., Renani S.A. et al. Randomised controlled trial of particles used in uterine fibroid embolisation (PURE): non-spherical polyvinyl alcohol versus calibrated microspheres. Cardiovasc Intervent Radiol. 2022;45(2):207–15. https://doi.org/10.1007/s00270-021-02977-0.
23. Zhang Y., Xu Y., Zhang X. et al. 8Spheres conformal microspheres as embolic agents for symptomatic uterine leiomyoma therapy in uterine artery embolization (UAE): A prospective clinical trial. Medicine (Baltimore). 2023;102(9):e33099. https://doi.org/10.1097/MD.0000000000033099.
24. Ghanaati H., Firouznia K., Moradi B. et al. Fertility outcomes after uterine artery embolization for symptomatic uterine arteriovenous malformations: a single-center retrospective study in 33 women. Cardiovasc Intervent Radiol. 2022;45(7):983–91. https://doi.org/10.1007/s00270-022-03105-2.
25. Pron G., Cohen M., Soucie J. et al. Ontario uterine fibroid embolization collaboration group. The Ontario uterine fibroid embolization trial. Part 1. Baseline patient characteristics, fibroid burden, and impact on life. Fertil Steril. 2003;79(1):112–9. https://doi.org/10.1016/s0015-0282(02)04539-9.
26. Seracchioli R., Rossi S., Govoni F. et al. Fertility and obstetric outcome after laparoscopic myomectomy of large myomata: a randomized comparison with abdominal myomectomy. Hum Reprod. 2000;15(12):2663–8. https://doi.org/10.1093/humrep/15.12.2663.
27. Mara M., Maskova J., Fucikova Z. et al. Midterm clinical and first reproductive results of a randomized controlled trial comparing uterine fibroid embolization and myomectomy. Cardiovasc Intervent Radiol. 2008;31(1):73–85. https://doi.org/10.1007/s00270-007-9195-2.
28. Коробова П.Г., Сулима А.Н., Мкртчян А.А. и др. Актуальные вопросы эффективности и безопасности эмболизации маточных артерий у пациенток с лейомиомой матки. Журнал акушерства и женских болезней. 2020;69(2):15–22. https://doi.org/10.17816/JOWD69215-22.
29. Hirst A., Dutton S., Wu O. et al. A multi-centre retrospective cohort study comparing the efficacy, safety and cost-effectiveness of hysterectomy and uterine artery embolisation for the treatment of symptomatic uterine fibroids. The HOPEFUL study. Health Technol Assess. 2008;12(5):1–248, iii. https://doi.org/10.3310/hta12050.
30. Soro M.P., Denys A., de Rham M., Baud D. Short & long term adverse outcomes after arterial embolisation for the treatment of postpartum haemorrhage: a systematic review. Eur Radiol. 2017;27(2):749–62. https://doi.org/10.1007/s00330-016-4395-2.
31. Kanter G., Packard L., Sit A. S. Placenta accreta in a patient with a history of uterine artery embolization for postpartum hemorrhage. J Perinatol. 2013;33(6):482–3. https://doi.org/10.1038/jp.2012.99.
32. Kitao K., Makihara N, Morita H. et al. The development of placenta increta following pelvic transcatheter artery embolization for postpartum hemorrhage. Clin Exp Obstet Gynecol. 2009;36(1):53–4.
33. Igarashi S., Izuchi S., Ogawa Y. et al. N-butyl cyanoacrylate is very effective for massive haemorrhage during the perinatal period. PLoS One. 2013;8(10):e77494. https://doi.org/10.1371/journal.pone.0077494.
34. Титова Г.П., Коков Л.С., Дамиров М.М. и др. Морфологические изменения тканей матки после эмболизации маточных артерий у больных с лейомиомой. Журнал имени Н.В. Склифосовского «Неотложная медицинская помощь». 2017;6(4):331–5. https://doi.org/10.23934/2223-9022-2017-6-4-331-335.
35. Mailli L., Patel S., Das R. et al. Uterine artery embolisation: fertility, adenomyosis and size – what is the evidence? CVIR Endovasc. 2023;6(1):8. https://doi.org/10.1186/s42155-023-00353-2.
36. Goldberg J., Pereira L., Berghella V. et al. Pregnancy outcomes after treatment for fibromyomata: uterine artery embolization versus laparoscopic myomectomy. Am J Obstet Gynecol. 2004;191(1):18–21. https://doi.org/10.1016/j.ajog.2004.01.046.
37. Kröncke T., David M. Uterine artery embolization (UAE) for fibroid treatment – results of the 7th Radiological Gynecological Expert Meeting. Geburtshilfe Frauenheilkd. 2019;79(7):688–92. https://doi.org/10.1055/a-0893-4807.
38. Доброхотова Ю.Э., Кнышева И.Г., Джобава Э.М. и др. Эмболизация маточных артерий и беременность: дискуссионные вопросы. Акушерство и гинекология. 2013;(5):42–7.
39. Pron G., Mocarski E., Bennett J. et al. Pregnancy after uterine artery embolization for leiomyomata: the Ontario multicenter trial. Obstet Gynecol. 2005;105(1):67–76. https://doi.org/10.1097/01.AOG.0000149156.07061.1f.
40. Karlsen K., Hrobjartsson A., Korsholm M. et al. Fertility after uterine artery embolization of fibroids: a systematic review. Arch Gynecol Obstet. 2018;297(1):13–25. https://doi.org/10.1007/s00404-017-4566-7.
41. Pabón I.P., Magret J.P., Unzurrunzaga E.A. et al. Pregnancy after uterine fibroid embolization: follow-up of 100 patients embolized using tris-acryl gelatin microspheres. Fertil Steril. 2008;90(6):2356–60. https://doi.org/10.1016/j.fertnstert.2007.10.074.
42. Бреусенко В.Г., Краснова И.А., Капранов С.А. и др. Спорные вопросы эмболизации маточных артерий при миоме матки. Вопросы гинекологии, акушерства и перинатологии. 2005;4(4):44–8.
43. Антропова Е.Ю., Коробов В.В., Сафиуллина Л.Р. Оценка влияния анастомозов между маточными и яичниковыми артериями на клинический результат эмболизации маточных артерий, на основании изучения маточного и яичникового кровотока. Журнал акушерства и женских болезней. 2010;59(6):22–6.
44. Высоцкий М.М., Куранов И.И., Невзоров О.Б. Влияние различных методов хирургического лечения миомы матки на показатели овариального резерва. Акушерство и гинекология. 2020;(5):132–8. https://doi.org/10.18565/aig.2020.5.132-138.
Об авторах
Н. А. КалининаРоссия
Калинина Наталья Алексеевна – клинический ординатор кафедры акушерства, гинекологии и перинатологии № 1
295051 Симферополь, бульвар Ленина, д. 5/7
А. Н. Сулима
Россия
Сулима Анна Николаевна – д.м.н., профессор, профессор кафедры акушерства, гинекологии и перинатологии № 1
295051 Симферополь, бульвар Ленина, д. 5/7
З. С. Румянцева
Россия
Румянцева Зоя Сергеевна – к.м.н., доцент, и.о. зав. кафедрой акушерства, гинекологии и перинатологии № 1
295051 Симферополь, бульвар Ленина, д. 5/7
П. Н. Баскаков
Россия
Баскаков Петр Николаевич – д.м.н., профессор, профессор кафедры акушерства, гинекологии и перинатологии № 1
295051 Симферополь, бульвар Ленина, д. 5/7
В. Д. Калинин
Россия
Калинин Виктор Дмитриевич – врач, сердечно-сосудистый хирург отделения кардиохирургии
299011 Севастополь, ул. Адмирала Октябрьского, д. 19
Рецензия
Для цитирования:
Калинина Н.А., Сулима А.Н., Румянцева З.С., Баскаков П.Н., Калинин В.Д. Оценка влияния эмболизации маточных артерий на репродуктивную функцию. Акушерство, Гинекология и Репродукция. 2023;17(4):476-484. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.410
For citation:
Kalinina N.A., Sulima A.N., Rumyantseva Z.S., Baskakov P.N., Kalinin V.D. Impact assessment of uterine artery embolization on reproductive. Obstetrics, Gynecology and Reproduction. 2023;17(4):476-484. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.410

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.











































