Перейти к:
Дефицит железа в практике врача-гинеколога: эффективность терапии
https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.402
Аннотация
Введение. Наиболее частым и довольно серьезным внегинекологическим осложнением аденомиоза является дефицит железа (ДЖ) различной степени за счет мено/метроррагий различной степени выраженности, вплоть до аномальных маточных кровотечений, требующих хирургического гемостаза. Принимая во внимание хронический характер заболевания, сложность радикальной терапии, а также влияние ДЖ на состояние всего организма и репродуктивной системы в частности, проблема достаточной и своевременной коррекции данного дефицита у пациенток с аденомиозом не теряет своей актуальности.
Цель: изучение эффективности терапии ДЖ у пациенток с аденомиозом при помощи препарата, содержащего фумарат железа и фолиевую кислоту.
Материалы и методы. Проведено наблюдательное исследование, в которое вошли 90 пациенток с изолированным аденомиозом различной степени выраженности: 30 пациенток с аденомиозом 1-й степени (группа 1), 30 пациенток с аденомиозом 2-й степени (группа 2), 30 женщин с аденомиозом 3–4-й степени (группа 3). Все пациентки получали фумарат железа в сочетании с фолиевой кислотой в течение 30 дней. Для выявления варианта ДЖ оценивали содержание сывороточного ферритина, сывороточного железа и трансферрина, общую железосвязывающую способность сыворотки крови (ОЖСС), параметры клинического анализа крови – уровень гемоглобина, число эритроцитов, показатель гематокрита, средний объем эритроцита (MCV), среднюю концентрацию гемоглобина в эритроците (MCHC).
Результаты. Выявлено статистически значимое увеличение феррокинетических показателей во всех группах пациенток после лечения. Наиболее достоверная и клинически значимая динамика отмечена по показателям сывороточного железа и ОЖСС. Так, после проведенной терапии уровень сывороточного железа вырос в группе 1 с 11,0 ± 0,6 мкмоль/л до 15,0 ±1,1 мкмоль/л, в группе 2 – с 9,0 ± 1,6 мкмоль/л до 14,0 ± 0,8 мкмоль/л, в группе 3 – с 7,0 ± 1,3 мкмоль/л до 12,0 ±1,3 мкмоль/л (p < 0,05). Также в группе 3 установлено снижение ОЖСС с 68,0 ± 1,8 мкмоль/л до 58,0 ± 1,7 мкмоль/л (p <0,05); в группах 2 и 3 также наблюдалась тенденция к снижению ОЖСС.
Заключение. Применение препарата, содержащего фумарат железа в сочетании с фолиевой кислотой, позволяет эффективно скорректировать имеющийся ДЖ различной степени выраженности у пациенток с аденомиозом при различной степени заболевания. Для более выраженного клинического эффекта рекомендовано более раннее и более длительное назначение препаратов железа среди пациенток с аденомиозом под контролем клинико-лабораторных показателей.
Для цитирования:
Джобава Э.М., Кнышева И.Г., Артизанова Д.П. Дефицит железа в практике врача-гинеколога: эффективность терапии. Акушерство, Гинекология и Репродукция. 2023;17(2):202-209. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.402
For citation:
Dzhobava E.M., Knysheva I.G., Artizanova D.P. Iron deficiency in the practice of a gynecologist: therapeutic efficacy. Obstetrics, Gynecology and Reproduction. 2023;17(2):202-209. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.402
Введение / Introduction
Дефицит железа (ДЖ) при гинекологической патологии – ситуация довольно частая, что требует определенных знаний и навыков от врача акушера-гинеколога. Глобально причинами ДЖ могут быть недостаток поступления, недостаток всасывания, нарушения обмена железа, повышенный расход, патологическая потеря железа [1].
Железо в организме человека содержится в количестве 4–5 г в форме геминовых и негеминовых соединений. Белки ферритин и гемосидерин являются главным депо железа в организме, при этом ферритин является также воспалительным белком. Транспортная функция железа осуществляется трансферрином. Сывороточное железо плазмы крови – это наиболее лабильный показатель, отвечающий за суточную потребность в железе и зависящий от множества факторов [2].
Бóльшая часть железа, а именно, 65 % используется для выработки эритроцитов (эритропоэза), для нормальной функции которого значимы несколько факторов: уровень эритропоэтина, уровень белка крови, а также насыщенность организма минералами и витаминами – кофакторами эритропоэза [3][4].
Причинами ДЖ в акушерско-гинекологической практике являются аномальные маточные кровотечения различной этиологии, нарушение гемостаза по типу коагулопатии (в частности, приобретенной, печеночного генеза или коагулопатии потребления), миома матки (особенно определенных типов узлов и их расположения), эндометриоз, аденомиоз, аборты (особенно осложненные), опухоли и т. д. [5].
Интересно, что аденомиоз может способствовать развитию ДЖ по нескольким механизмам. Первый – это потери железа при менометроррагиях при аденомиозе. Второй вариант относится не к истинному ДЖ, а к развитию анемии хронических заболеваний или анемии хронического воспаления.
Менометроррагии могут вызывать потерю железа до 250 мг [6][7]. Своевременная диагностика и адекватная эффективная терапия железодефицитных состояний в гинекологической практике является важнейшей задачей врача-гинеколога для сохранения женского здоровья, качества жизни и репродуктивного потенциала [8][9].
В настоящее время по выраженности ДЖ выделяют:
– предлатентный ДЖ, который характеризуется невыраженным снижением запасов железа в депо, но расход на продукцию эритроцитов не снижается. У данной формы ДЖ нет достоверных клинических и лабораторных критериев диагностики, кроме единственного теста абсорбции 59 Fe3+, который показывает повышение абсорбции до 50–60 % при норме 10–15 %;
– латентный ДЖ, который характеризуется выраженным снижением запасов железа в депо, но при этом нет клинико-лабораторных признаков анемии. В этом случае имеется снижение уровня ферритина при нормальных показателях клинического анализа крови и пограничных значениях других показателей обмена железа;
– манифестный ДЖ, это выявление железодефицитной анемии по данным клинико-лабораторного обследования, а именно, в первую очередь снижение гемоглобина [3].
Во всех случаях развития ДЖ в гинекологической практике, независимо от его причины, требуется длительная терапия препаратами железа с высокой степенью усвоения, хорошей переносимостью и высокой клинической эффективностью [10][11].
Цель: изучение эффективности терапии ДЖ у пациенток с аденомиозом при помощи препарата, содержащего фумарат железа и фолиевую кислоту.
Материалы и методы / Materials and Methods
Дизайн исследования / Study design
Проведено наблюдательное исследование, в которое вошли 90 пациенток в возрасте от 25 до 45 лет, обратившихся в ООО Клиника «Креде Эксперто» (Москва, Россия) с жалобами на аномальные маточные кровотечения и которым после дообследования был поставлен диагноз «аденомиоз» согласно существующим клиническим рекомендациям [9]. У всех пациенток был выявлен ДЖ различной степени выраженности.
Критерии включения и исключения / Inclusion and exclusion criteria
Критерии включения: аденомиоз; репродуктивный период; подписанное добровольное информированное согласие.
Критерии исключения: гиперплазия и полипы эндометрия; миома матки; наружный эндометриоз; анемия хронических заболеваний; отказ от участия в исследовании.
Группы обследованных / Patient groups
Все пациентки были разделены на 3 группы по степени выраженности аденомиоза на основании результатов двукратного ультразвукового исследования (УЗИ) матки по фазам цикла (в 1-ю и 2-ю фазы цикла) и магнитно-резонансной томографии (МРТ) во 2-ю фазу цикла: 30 пациенток с аденомиозом 1-й степени (группа 1), 30 пациенток с аденомиозом 2-й степени (группа 2), 30 женщин с аденомиозом 3–4-й степени.
Методы исследования / Study methods
Для выявления варианта ДЖ оценивали уровень сывороточного ферритина, сывороточного железа, трансферрина, общую железосвязывающую способность сыворотки крови (ОЖСС), измеренные на биохимическом анализаторе Labio-200 (Mindray, Китай), и параметры клинического анализа крови – уровень гемоглобина, число эритроцитов, показатель гематокрита, средний объем эритроцита (MCV), среднее количество гемоглобина в эритроците (MCHC), определенные на гематологическом анализаторе Medonic М20 (Boule Medical AB, Швеция).
Лечение / Therapy
После выявления ДЖ и верификации его варианта проводили коррекцию наиболее активной, биодоступной пероральной формой железа – железа фумарат (эквивалентно 50 мг элементарного железа) в комбинации с фолиевой кислотой в дозировке 500 мкг (препарат Ферретаб® комп.) 1 капсула в сутки. Прием препарата назначали после 16 ч до приема пищи (на голодный желудок), запивая водой с лимоном. Эффективность терапии оценивали по лабораторным показателям. Мы провели сравнительный анализ гематологических и феррокинетических показателей у пациенток всех трех групп в динамике – до начала лечения и через 30 дней лечения.
Этические аспекты / Ethical aspects
Все участницы исследования подписали форму добровольного информированного согласия и получили исчерпывающую информацию о характере исследования. Исследование проведено в соответствии с этическими требованиями Хельсинской декларации Всемирной медицинской ассоциации.
Статистический анализ / Statistical analysis
Статистический анализ выполняли согласно правилам медицинской статистики с использованием программ для статистической обработки данных Statistica 6.0 (StatSoft Inc., США). Показатели описывали с помощью среднего арифметического (M) и ошибки среднего (m). Сравнение групп выполняли с помощью t-критерия Стьюдента. Для всех тестов и критериев критический уровень значимости принимали равным 0,05, т. е. различия признавали статистически значимыми при р < 0,05.
Результаты и обсуждение / Results and Discussion
Клинико-анамнестическая характеристика обследованных / Clinical and anamnestic characteristics of the patients examined
Средний возраст пациенток составил 38,3 ± 3,9 лет: в группе 1 – 36,7 ± 3,5 лет, в группе 2 – 37,4 ± 3,3 лет, в группе 3 – 38,7 ± 3,4 лет. Отмечена тенденция к более старшему возрасту в группе 3 с более выраженной тяжестью протекания аденомиоза, что, вероятно, связано с длительностью заболевания и прогрессированием аденомиоза с течением времени, однако значимых различий между группами пациенток по возрасту выявлено не было. По анамнезу и экстрагенитальной патологии группы также были сопоставимы между собой. Структура соматической патологии в группах отражена в таблице 1.
При анализе сопутствующей патологии обращает на себя внимание существенно более высокая частота (p < 0,05) патологии желудочно-кишечного тракта, что, вероятно, связано с одним из патогенетических механизмов прогрессирования аденомиоза. Также отмечена тенденция к более высокой частоте инфекционных заболеваний ЛОР-органов в анамнезе, однако достоверных различий выявлено не было. Это связано с тем, что критерием исключения в группах являлось наличие анемии хронических заболеваний, куда также относят хронические персистирующие инфекции ЛОР-органов. Однако наши наблюдения сопоставимы с данными литературы о аутоимунных нарушениях, «пусковым» критерием которых может быть длительный инфекционный процесс как причина развития аденомиоза [11].
Интересные данные получены при анализе паритета беременности и родов среди всех пациенток (табл. 2).
Статистически значимых различий при сравнении анамнестических данных по паритету беременностей и родов между группами пациенток выявлено не было. Более того, как видно из таблицы 2, среди пациенток всех трех групп были женщины с отсутствием беременности в анамнезе. Хочется отметить, что среди пациенток, исключенных из исследования, была одна пациентка с распространенным инфильтративным эндометриозом с последующей резекцией кишечника и длительной гормональной терапией, дебют заболевания (сразу 4-я стадия) у которой был диагностирован в возрасте 17 лет. Это свидетельствует о мультифакторной природе возникновения и прогрессирования эндометриоза и аденомиоза, что соответствует последним данным мировой литературы [11].
Таблица 1. Сопутствующая соматическая патология.
Table 1. Somatic comorbidities.
|
Характер патологии Pathology affecting |
Группа 1 / Group 1 n = 30 |
Группа 2 / Group 2 n = 30 |
Группа 3 / Group 3 n = 30 |
|
Патология органов зрения Visual organs |
7 |
13 |
9 |
|
Патология ЛОР-органов (ремиссия) ENT (remission) |
17 |
15 |
18 |
|
Патология органов дыхания Air way tract |
5 |
8 |
6 |
|
Патология сердечно-сосудистой системы Cardiovascular system |
7 |
11 |
9 |
|
Патология эндокринной системы Endocrine system |
9 |
13 |
11 |
|
Патология желудочно-кишечного тракта Gastrointestinal tract |
25* |
28* |
30* |
|
Патология мочевыводящих путей Urinary tract |
8 |
5 |
9 |
Примечание: *р < 0,05 – различия статистически значимы внутри группы по сравнению с частотой другой патологии.
Note: *p < 0.05 – significant in-group differences compared with incidence of other pathology.
Таблица 2. Паритет беременности и родов.
Table 2. Parity of pregnancy and delivery.
|
Исходы беременностей Pregnancy outcome |
Группа 1 / Group 1 n = 30 n (%) |
Группа 2 / Group 2 n = 30 n (%) |
Группа 3 / Group 3 n = 30 n (%) |
|
Всего беременностей Total pregnancies |
26 (86,7) |
25 (83,3) |
27 (90,0) |
|
Роды Delivery |
20 (66,7) |
15 (50,0) |
25 (83,3) |
|
Самопроизвольное прерывание беременности в сроке до 12 нед Spontaneous abortion at gestational age before 12 weeks |
2 (6,7) |
3 (10,0) |
1 (3,3) |
|
Неразвивающаяся беременность Non-developing pregnancy |
1 (3,3) |
1 (3,3) |
0 (0) |
|
Артифициальный аборт Artificial abortion |
3 (10,0) |
6 (20,0) |
1 (3,3) |
Результаты лечения / Therapeutic results
Исходя из показателей исходных нарушений обмена железа, можно утверждать, что манифестный ДЖ (рис. 1) значимо чаще (p < 0,05) выявлялся в группах 2 (в 56,7 %) и 3 (в 70,0 %) по сравнению с группой 1 (в 33,3 %). Предлатентный ДЖ ожидаемо чаще встречался среди пациенток группы 1 (56,7 %). Латентный ДЖ был определен у 10,0 % пациенток группы 1, у 23,3 % пациенток группы 2 и у 13,0 % женщин группы 3.
Проведя анализ данных обследования после проведения железо-заместительной терапии, установлено статистически значимое (p < 0,05) увеличение показателей среди пациенток всех трех групп по сравнению с показателями до начала лечения. Наиболее выраженный прирост показателей, характеризующих обмен железа, был выявлен среди пациенток группы 1, что, вероятно, связано с величиной кровопотери, в отличие от ДЖ при других патологиях репродуктивной системы, где зачастую ведущими факторами, влияющим на эффективность терапии, являются кофакторы усвоения железа, состояние желудочно-кишечного тракта и т. д. Также хочется подчеркнуть, что хорошие результаты восполнения ДЖ были достигнуты всего через 1 мес лечения без радикальной терапии аденомиоза, что косвенно свидетельствует о хорошей усвояемости препарата и его высокой биодоступности.
Динамика гематологических и феррокинетических показателей обмена железа у пациенток всех трех групп на фоне терапии отражена в таблице 3. Наиболее показательным был рост содержания гемоглобина и сывороточного железа.
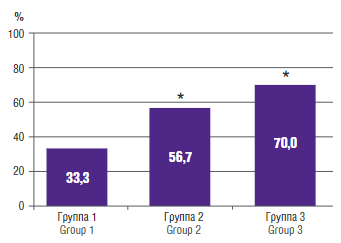
Рисунок 1. Манифестный дефицит железа в группах обследованных.
Примечание: *p < 0,05 – различия статистически значимы по сравнению с группой 1.
Figure 1. Manifested iron deficiency in the examined groups.
Note: *p < 0.05 – significant differences compared to group 1.
Таблица 3. Динамика показателей обмена железа на фоне терапии (М ± m).
Table 3. Therapy-related dynamics of iron metabolism parameters (M ± m).
|
Показатель Parameter |
Группа 1 / Group 1 n = 30 |
Группа 2 / Group 2 n = 30 |
Группа 3 / Group 3 n = 30 |
|||
|
До лечения Before treatment |
После лечения After treatment |
До лечения Before treatment |
После лечения After treatment |
До лечения Before treatment |
После лечения After treatment |
|
|
Гемоглобин, г/л Hemoglobin, g/L |
120,0 ± 1,8 |
125,0 ± 2,1 |
110,0 ± 3,2 |
115,0 ± 3,6* |
103,0 ± 3,7 |
110,0 ± 2,4* |
|
Сывороточное железо, мкмоль/л Serum iron, µmol/l |
11,0 ± 0,6 |
15,0 ± 1,1* |
9,0 ± 1,6 |
14,0 ± 0,8* |
7,0 ± 1,3 |
12,0 ± 1,3* |
|
Сывороточный ферритин, мкг/л Serum ferritin, µg/l |
19,0 ± 1,3 |
22,0 ± 1,2 |
15,0 ± 2,6 |
20,0 ± 1,7 |
13,0 ± 2,6 |
18,0 ± 1,9 |
|
Общая железосвязывающая способность сыворотки крови, мкмоль/л Total iron-binding capacity of blood serum, µmol/l |
59,0 ± 1,2 |
55,0 ± 1,3 |
63,0 ± 1,4 |
57,0 ± 1,3 |
68,0 ± 1,8 |
58,0 ± 1,7* |
|
Эритроциты, ×1012/л Erythrocytes, ×1012/L |
4,1 ± 0,9 |
4,3 ± 1,3 |
4,0 ± 0,8 |
4,2 ± 1,2 |
3,9 ± 1,5 |
4,1 ± 1,4 |
|
Гематокрит, % Hematocrit, % |
35,3 ± 1,1 |
37,1 ± 1,2 |
33,3 ± 1,7 |
35,2 ± 1,5 |
31,8 ± 1,6 |
36,3 ± 1,2* |
|
Cредний объем эритроцита (MCV), фл Mean corpuscular volume, fl |
88,0 ± 1,5 |
91,0 ± 1,2 |
84,0 ± 1,3 |
89,0 ± 1,5 |
82,0 ± 1,9 |
87,0 ± 1,1 |
|
Cреднее количество гемоглобина в эритроците (MCHC), г/дл Mean corpuscular hemoglobin concentration, g/dl |
33,5 ± 1,3 |
35,5 ± 0,8 |
31,6 ± 1,5 |
33,8 ± 1,7 |
27,1 ± 1,8 |
32,1 ± 1,5 |
Примечание: *р < 0,05 – различия статистически значимы по сравнению с показателями до лечения внутри группы.
Note: *p < 0.05 – significant differences compared to pre-treatment in-group magnitude.
Анализ результатов лечения / Data analysis
При анализе данных клинико-лабораторного обследования у пациенток с ДЖ при аденомиозе и расчетом дозы и длительности железо-заместительной терапии мы считаем необходимым акцентировать важность рассмотрения объема и частоты кровопотери у каждой отдельной пациентки, так как, по нашим данным, это существенно влияет на эффективность терапии и состояние пациенток. Необходимо оценивать сопутствующее факторы, влияющие на усвоение железа – наличие хронических заболеваний, дефицит кофакторов и т. д.
Также следует помнить о гипоксическом поражении органов при анемии различной степени выраженности и влиянии уровня железа на функционирование всех систем и органов, в связи с чем мы рекомендуем начинать коррекцию ДЖ у пациенток с аденомиозом, начиная с предлатентной стадии, с динамическим наблюдением и контролем на предмет ДЖ параллельно с лечением основного заболевания (принимая во внимание чаще всего неуклонное прогрессирование процесса в отсутствие радикальной терапии). По нашим данным, это позволяет значительно улучшить субъективное самочувствие пациенток и объективное состояние организма даже при прогрессировании аденомиоза и увеличении менструальных и межменструальных кровопотерь в дальнейшем.
Заключение / Conclusion
По результатам проведенного краткосрочного исследования у пациенток с аденомиозом и различным уровнем ДЖ, можно утверждать, что препарат, содер- жащий железа фумарат (эквивалентно 50 мг элементарного железа) в комбинации с фолиевой кислотой в дозировке 500 мкг (препарат Ферретаб® комп.), эффективен при лечении ДЖ и железодефицитной анемии и может быть использован как для стартовой, так и для длительной поддерживающей терапии у пациенток с хронической кровопотерей на фоне аденомиоза. Более ранняя дотация железа (в том числе профилактическая) на стадии предлатентной и латентной формы ДЖ позволяет значительно улучшить состояние пациенток даже при выраженной стадии аденомиоза и сочетается с основным лечением.
Список литературы
1. Коноводова Е.Н., Докуева Р.С-Э., Якунина Н.А. Железодефицитные состояния в акушерско-гинекологической практике. РМЖ. Мать и дитя. 2011;19(20):1228–31.
2. Pasricha S.-R.S., Flecknoe-Brown S.C., Allen K.J. et al. Diagnosis and management of iron deficiency anaemia: a clinical update. Med J Aust. 2010;193(9):525–32. https://doi.org/10.5694/j.1326-5377.2010.tb04038.x.
3. Серов В.Н., Дубровина Н.В., Балушкина А.А. Железодефицитная анемия в гинекологической практике: основные принципы лечения. РМЖ. Мать и дитя. 2011;19(1):1–4.
4. Городецкий В.В., Годулян О.В. Железодефицитные состояния и железодефицитная анемия: диагностика и лечение. Методические рекомендации. М.: Медпрактика-М, 2005. T. 3. 28 c.
5. Козловская Л.В. Гипохромные анемии: дифференциальный диагноз и лечение. Новый медицинский журнал. 1996;56:8–12.
6. UNICEF/UNU/WHO. Iron Deficiency Anemia: Assessment, Prevention, and Control. A Guide for Programme Managers. Geneva: WHO/NHD, 2001. 132 p. Режим доступа: http://s2.medicina.uady.mx/observatorio/docs/an/li/AN2001_Li_WHO.pdf. [Дата доступа: 10.02.2023].
7. Лебедев В.А., Пашков В.М. Принципы терапии железодефицитной анемии у гинекологических больных. Трудный пациент. 2013;(11):3–7.
8. Дворецкий Л.И., Заспа Е.А. Железодефицитные анемии в практике акушера-гинеколога. РМЖ. 2008;16(29):1898–905.
9. Клинические рекомендации. Эндометриоз. М.: Министерство здравоохранения Российской Федерации, 2020. 60 с. Режим доступа: https://minzdrav.samregion.ru/wp-content/uploads/sites/28/2020/12/endometrioz.pdf. [Дата доступа: 10.02.2023].
10. Fernаndez-Gaxiola A.C., De-Regil L.M. Intermittent iron supplementation for reducing anaemia and its associated impairments in menstruating women. Cochrane Database Syst Rev. 2019;1(1):CD009218. https://doi.org/10.1002/14651858.CD009218.pub3.
11. Верткин А.Л., Годулян О.В., Городецкий В.В., Скотников А.С. Железодефицитная анемия и выбор препарата для ее коррекции. РМЖ. Медицинское обозрение. 2010;(5):260.
Об авторах
Э. М. ДжобаваРоссия
Джобава Элисо Мурмановна – д.м.н., профессор, медицинский директор
109004 Москва, Товарищеский переулок, д. 10, стр. 1
И. Г. Кнышева
Россия
Кнышева Инесса Геннадьевна – к.м.н., врач гинеколог-эндокринолог, генеральный директор
109004 Москва, Товарищеский переулок, д. 10, стр. 1
Д. П. Артизанова
Россия
Артизанова Дарья Павловна – врач акушер-гинеколог
109004 Москва, Товарищеский переулок, д. 10, стр. 1
Рецензия
Для цитирования:
Джобава Э.М., Кнышева И.Г., Артизанова Д.П. Дефицит железа в практике врача-гинеколога: эффективность терапии. Акушерство, Гинекология и Репродукция. 2023;17(2):202-209. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.402
For citation:
Dzhobava E.M., Knysheva I.G., Artizanova D.P. Iron deficiency in the practice of a gynecologist: therapeutic efficacy. Obstetrics, Gynecology and Reproduction. 2023;17(2):202-209. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.402

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.











































