Перейти к:
Оценка эффективности и безопасности применения железа (III) гидроксида олигоизомальтозата у женщин репродуктивного возраста с железодефицитной анемией
https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.378
Аннотация
Цель: продемонстрировать эффективность и безопасность применения железа (III) гидроксида олигоизомальтозата для восполнения дефицита железа у пациенток с железодефицитной анемией (ЖДА).
Материалы и методы. Проведено наблюдательное когортное исследование, обследована 31 пациентка (10 родильниц, 13 беременных, 8 гинекологических пациенток), страдающих ЖДА 1–3-й степени тяжести. После исследования уровней ферритина, железа, латентной железосвязывающей способности, общего кальция, неорганического фосфора, трансферрина, С-реактивного белка была проведена терапия препаратом Монофер (железа (III) гидроксид олигоизомальтозат). Через 4 нед после последнего приёма препарата проводили контроль эффективности и удовлетворенности терапией.
Результаты. При обследовании после лечения получены статистически значимые изменения следующих показателей: повышение уровня эритроцитов в 1,3 раза, показателя гемоглобина – на 26,5 г/л, значений гематокрита – на 0,58 % (р = 0,00). Результаты биохимического анализа крови также имели положительную динамику: уровень ферритина повысился на 216,21 нг/мл, железа – на 6,87 мкмоль/л, латентная железосвязывающая способность крови снизилась на 30,73 мкмоль/л, концентрация трансферрина уменьшилась на 1,17 г/л, незначительно повысилось содержание общего кальция (на 0,14 ммоль/л) и неорганического фосфора (на 0,1 ммоль/л). Опрос пациенток согласно шкале Лайкерта показал высокую степень удовлетворенности лечением. Нежелательные явления (НЯ) и серьезные нежелательные явления (СНЯ) при проведении исследования не возникали.
Заключение. Достигнуто значимое повышение показателей качественного и количественного состава форменных элементов и биохимических показателей крови. Посттрансфузионную гипофосфатемию и гипокальциемию у обследованных пациенток не наблюдали. Отмечена высокая удовлетворенность лечением и безопасность применения препарата.
Ключевые слова
Для цитирования:
Андреева М.Д., Ахиджак А.Н., Белая А.Д., Карахалис Л.Ю., Кононенко Т.С. Оценка эффективности и безопасности применения железа (III) гидроксида олигоизомальтозата у женщин репродуктивного возраста с железодефицитной анемией. Акушерство, Гинекология и Репродукция. 2023;17(1):45-52. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.378
For citation:
Andreeva M.D., Akhidzhak A.N., Belaya A.D., Karakhalis L.Yu., Kononenko T.S. Assessing efficacy and safety of iron (III) hydroxide oligoisomaltosate in reproductive-age women with iron deficiency anemia. Obstetrics, Gynecology and Reproduction. 2023;17(1):45-52. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.378
ВВЕДЕНИЕ / INTRODUCTION
Железодефицитная анемия (ЖДА) является одним из самых распространенных заболеваний на планете, а последствия дефицита железа в организме, связанные с ней, определяют актуальность изучения данной проблемы. По данным Всемирной организации здравоохранения (ВОЗ), ЖДА выявляется у 1,8 млрд человек нашей планеты, а дефицит железа разной степени тяжести имеется у каждого 3-го жителя Земли – это 3,6 млрд человек (30 % населения). Основываясь на результатах исследований отечественных и зарубежных ученых последних лет, удалось ответить на многие вопросы этиологии, патогенеза, диагностики, лечения, а также профилактики дефицита железа [1][2].
При железодефицитных состояниях развиваются такие морфофункциональные нарушения, как дистрофия внутренних органов с функциональными и органическими изменениями, вторичная недостаточность иммунитета, осложненное течение беременности и родов, задержка развития детей, данное заболевание сопровождают изменения интеллекта и психомоторных реакций [3]. Группу риска по развитию ЖДА прежде всего составляют женщины репродуктивного возраста, беременные, послеродовые и лактирующие, женщины с аномальными маточными кровотечениями (АМК) [4][5]. В последние годы появились современные препараты железа для внутривенного введения, которые позволяют быстро купировать ЖДА. Несмотря на высокую эффективность препаратов железа (карбоксимальтозат и изомальтоза железа) для внутривенного введения, сообщается о таких побочных эффектах, как гипофосфатемия и, как следствие, развитие каскада патологических процессов, ведущих к гипокальциемии. Клинические проявления гипофосфатемии разнообразны (боли в костях, мышцах, остеомаляция с переломами) и коррелируют с длительностью проводимой терапии, степенью дефицита фосфатов, сопутствующими заболеваниями почек и дефектами генов, регулирующих фосфатный гомеостаз. В группу риска по развитию внутривенной гипофосфатемии входят прежде всего пациенты с тяжелыми и хроническими формами ЖДА, а также пациенты, длительно находящиеся на терапии внутривенными формами препаратов железа [6][7].
Таким образом, высокая распространенность железодефицитных состояний среди женщин репродуктивного возраста, недостаточная эффективность лечения, проявления побочного действия препаратов железа, увеличение частоты функциональной и органической патологии, значимое снижение качества жизни делают проблему изучения дефицита железа и её эффективной терапии весьма актуальной [8][9].
Цель: продемонстрировать эффективность и безопасность применения железа (III) гидроксида олигоизомальтозата для восполнения дефицита железа у пациенток с ЖДА.
МАТЕРИАЛЫ И МЕТОДЫ / MATERIALS AND METHODS
Дизайн исследования / Study design
На базе Перинатального центра ГБУЗ ККБ № 2 Минздрава Краснодарского края проведено наблюдательное когортное исследование. Обследована 31 женщина репродуктивного возраста (от 18 до 46 лет), страдающая ЖДА различной степени тяжести. Диагноз анемии был выставлен на основании критериев ЖДА согласно Федеральным клиническим рекомендациям «Диагностика, профилактика и лечение железодефицитных состояний у беременных и родильниц» Минздрава России [10]. Все участницы исследования были пролечены препаратом Монофер (железа (III) гидроксид олигоизомальтозат).
Критерии включения и исключения / Inclusion and exclusion criteria
Критерии включения: возраст от 18 до 55 лет на момент скрининга; железодефицитные состояния, связанные с АМК различного генеза (функциональные или органические); беременность (срок не менее 22 нед); послеродовой период; подписанное информированное добровольное согласие.
Критерии исключения: повышенная чувствительность к компонентам препарата Монофер; признаки перегрузки железом (гемосидероз, гемохроматоз); анемия, не связанная с дефицитом железа; нарушение выведения железа; I триместр беременности; острые инфекционные заболевания; отказ от участия в исследовании.
Методы обследования / Study methods
Всем пациенткам было выполнено комплексное обследование. Физикальный осмотр включал измерение артериального давления, температуры тела, подсчет частоты сердечных сокращений (ЧСС), частоты дыхательных движений (ЧДД), визуальную оценку состояния кожных покровов и слизистых оболочек. Проведено анкетирование, в котором отображались данные как соматического, так и гинекологического анамнеза. Рассчитывали индекс массы тела (ИМТ).
Лабораторная диагностика / Laboratory diagnostics
Общий анализ крови (ОАК) до и после терапии выполняли на автоматических гематологических анализаторах Sysmex XN-450 (Sysmex, Япония) и Sysmex XN-1000-2 (Sysmex, Япония) соответственно. Биохимический анализ крови (БхАК) включал исследование латентной железосвязывающей способности крови, уровней общего кальция, неорганического фосфора и С-реактивного белка на автоматическом анализаторе Architect c8000 (Abbott Laboratories, США); содержание ферритина, трансферрина и железа определяли на автоматическом анализаторе Сobas 8000 (Roche Diagnostics GmbH, Германия).
Группы обследованных / Study groups
Когорта обследованных представлена в виде трех групп: группа I (n = 8; 25,8 %) – гинекологические пациентки с АМК; группа II (n = 13; 41,9 %) – беременные с 22-й недели беременности и ЖДА; группа III (n = 10; 32,3 %) – родильницы.
Лечение / Therapy
После обследования (ОАК, БхАК) была проведена терапия препаратом Монофер в соответствии с инструкцией и по следующим схемам: 1) для находящихся в отделениях от 7 до 10 дней гинекологических и беременных пациенток – 500 мг железа (III) гидроксида олигоизомальтозата + 500 мл 0,9 % раствора NaCl внутривенно капельно медленно трижды через день; 2) для родильниц по короткой схеме – 1000 мг железа (III) гидроксида олигоизомальтозата + 500 мл 0,9 % раствора NaCl внутривенно капельно медленно однократно.
Через 4 нед после последнего приёма препарата пациентки сдавали контрольные анализы крови (ОАК, БхАК), а также проводилась оценка удовлетворенности лечением по шкале Лайкерта, которая основывается на оценке пациенткой степени своего согласия или несогласия с утверждениями от «полностью не согласен», «не согласен», «затрудняюсь ответить», «согласен» до «полностью согласен» при ответе на вопросы: получаемое мной лечение эффективно; я чувствую улучшение своего состояния после начала лечения; в целом, я довольна проводимым лечением.
Этические аспекты / Ethical aspects
Исследование проведено в соответствии с этическими стандартами Хельсинской декларации Всемирной медицинской ассоциации 1964 г. и ее последующими изменениями. Исследование было одобрено независимым этическим комитетом ФГБОУ ВО КубГМУ Минздрава России, протокол № 104 от 22.10.2021. Все пациентки подписали добровольное информированное согласие на участие в исследовании и отбор биоматериала для анализа.
Методы статистического анализа / Statistical analysis
Полученные данные были обработаны с помощью программ Microsoft Excel 2010 (Microsoft, США), Statistica 13.3 (Tibco, США). Статистическая обработка включала статистическое описание исследуемых объектов, оценку значимости выявленных различий, а также поиск связей между признаками: оценка среднего путем подсчета среднего арифметического (М), стандартной ошибки средней арифметической (m), медианы (Ме), моды (Мо). Применяли методику кросстабуляции, непараметрические методы сравнения по тестам Вальда–Вольфовица и Манна–Уитни. Корреляционные связи оценивали с помощью коэффициента корреляции Спирмена, коэффициента сопряженности, F-критерия Фишера, коэффициента Крамера. После проведенной математической обработки статистически значимыми считали полученные данные при уровне р < 0,05 [11].
РЕЗУЛЬТАТЫ / RESULTS
Клинико-анамнестические данные / Clinical and anamnestic data
Средний возраст всех пациенток составил 32,61 ± 6,65 года (Ме = 31,0 год), средний ИМТ – 22,88 ± 2,45 кг/м2 (Ме = 22,60 кг/м2). Средний возраст составил в группе I (n = 8) – 36,75 лет, в группе II (n = 13) – 30,08 лет, в группе III (n = 10) – 31,3 год. По данным анкетирования, возраст наступления менархе составил 12,77 ± 1,38 год (Ме = 13,0 лет), возраст начала половой жизни – 18,81 ± 3,29 года (Ме = 18,0 лет). У 28 (90,3 %) пациенток в анамнезе менструации были регулярными, и только 3 пациентки (9,7 %) отмечали нарушения менструального цикла. Длительность менструального цикла у всех пациенток составила 31,97 ± 17,42 лет (Ме = 28,0 дней); длительность менструальных кровотечений – 5,55 ± 1,12 дней (Ме = 5,0 дней). Умеренные менструальные выделения отмечали 26 (83,9 %) пациенток, обильные – 5 (16,1 %). Дисменорея была у 11 (35,5 %) пациенток, у 20 (60,5 %) не отмечалось болезненных менструаций. Гинекологическую патологию в анамнезе имели 16 (51,6 %) женщин.
По результатам анкетирования, субъективная оценка состояния здоровья по 5-ти балльной шкале непосредственно перед проведением исследования в среднем составила 3,29 ± 0,59 балла (Ме = 3,0 балла). За 1 год до исследования субъективная оценка состояния здоровья по той же системе оценивания составляла 3,42 ± 0,67 балла (Ме = 3,0 балла).
Из сопутствующей соматической патологии чаще всего встречались заболевания желудочно-кишечного тракта – у 5 (16,1 %) пациенток, эндокринные нарушения – у 4 (12,9 %), заболевания сердечно-сосудистой системы – у 3 (9,7 %), дыхательной, мочевыделительной систем – у 2 (6,5 %), заболевание крови (ранее диагностируемая анемия) и опорно-двигательного аппарата – у 1 (3,2 %) пациентки.
Данные лабораторных исследований / Laboratory data
Результаты исследования ОАК пациенток до и после лечения препаратом железа (III) гидроксид олигоизомальтозат представлены в таблице 1.
Результаты исследования БхАК пациенток до и после лечения препаратом железа (III) гидроксид олигоизомальтозат представлены в таблице 2.
Результаты исследования фосфорно-кальциевого обмена пациенток до и после лечения препаратом железа (III) гидроксид олигоизомальтозат представлены в таблице 3.
Таблица 1. Параметры общего анализа крови обследованных пациенток до и после проведенного лечения.
Table 1. Parameters of general blood test in patients examined before and after treatment.
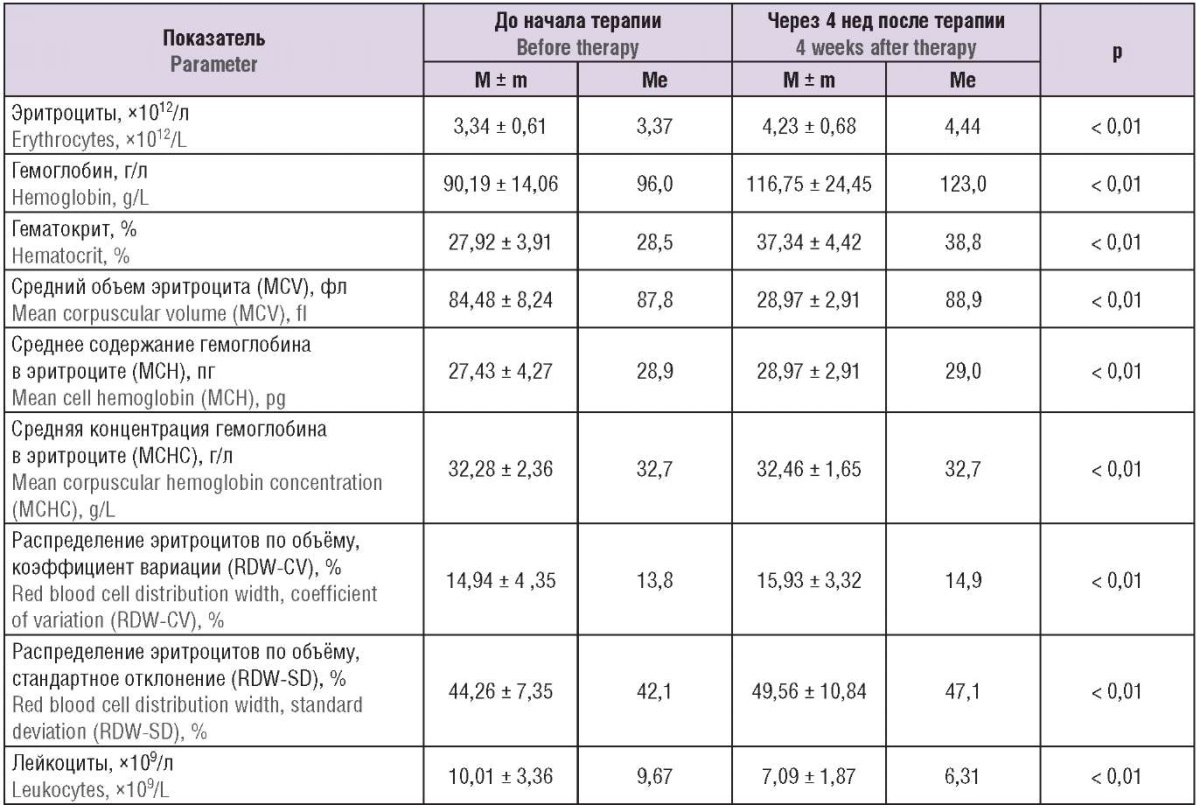
Таблица 2. Параметры биохимического анализа крови обследованных пациенток до и после проведенного лечения.
Table 2. Parameters of blood test in patients examined before and after treatment.
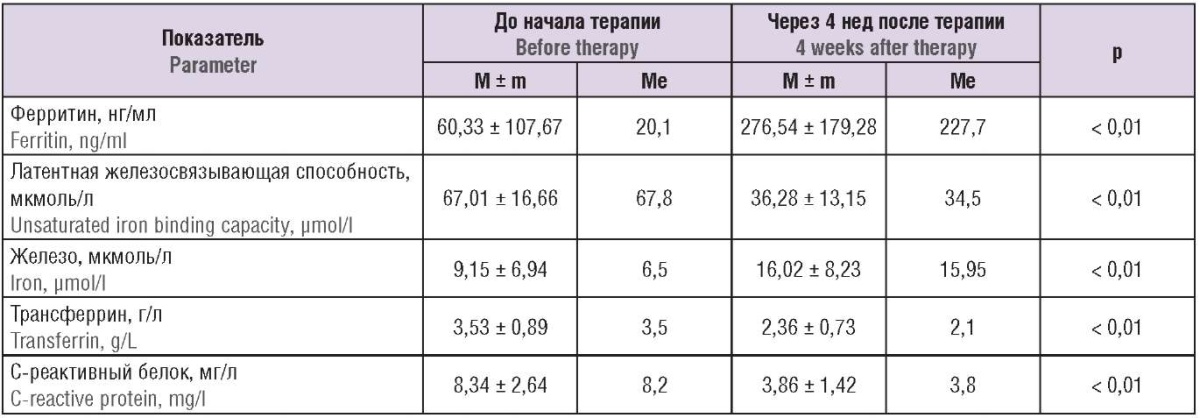
Таблица 3. Содержание общего кальция и неорганического фосфора крови обследованных пациенток до и после проведенного лечения.
Table 3. Blood total calcium and inorganic phosphorus in patients examined before and after treatment.
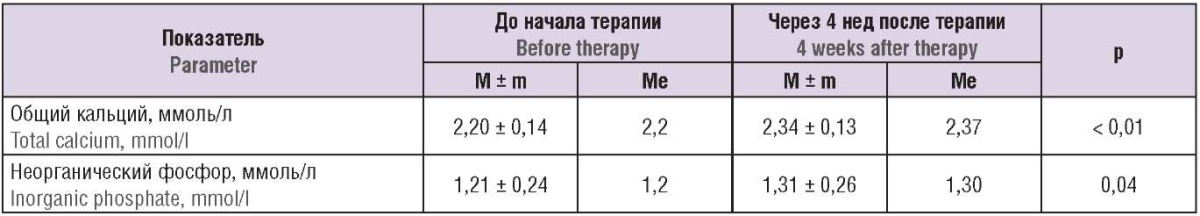
После проведенной терапии пациентки дали оценку удовлетворенности лечением согласно шкале Лайкерта по 5-ти балльной шкале по следующим показателям: эффективность получаемого лечения – 4,73 ± 0,45 балла (Ме = 5,0 баллов); улучшение состояния после начала лечения – 4,50 ± 0,51 балла (Ме = 4,5 балла); удовлетворенность проводимым лечением в целом – 4,69 ± 0,47 балла (Ме = 5,0 баллов).
Нежелательные явления (НЯ) и серьезные нежелательные явления (СНЯ) в процессе лечения и после не наблюдались.
ОБСУЖДЕНИЕ / DISCUSSION
Лечение ЖДА препаратом Монофер (железа (III) гидроксид олигоизомальтозат) короткими курсами показало высокую эффективность, что подтверждают лабораторные показатели ОАК: повышение после терапии количества эритроцитов в 1,3 раза, уровня гемоглобина – на 26,5 г/л, значений гематокрита – на 0,58 %. Результаты БхАК, отражающие запасы железа в организме, также имели хорошую положительную динамику: уровень ферритина повысился на 216,21 нг/мл, латентная железосвязывающяя способность крови снизилась на 30,73 мкмоль/л, концентрация трансферрина уменьшилась на 1,17 г/л, получено значительное повышение уровня железа на 6,87 мкмоль/л.
По данным систематического обзора, проведенного B. Schaefer с соавт., наиболее значимым побочным эффектом применения карбоксимальтозы и изомальтозида железа для внутривенного введения является гипофосфатемия, приводящая при легком течении к боли в мышцах и костях, а в присутствии высоких факторов риска может принимать тяжелое течение с развитием остеомаляции [6][7]. В проведенном нами исследовании не отмечено клинически значимого влияния препарата на фосфорно-кальциевый обмен: содержание общего кальция повысилось на 0,14 ммоль/л, неорганического фосфора – на 0,1 ммоль/л. Посттрансфузионной гипофосфатемии и гипокальциемии у обследованных пациенток не наблюдали, что может быть обусловлено короткими курсами терапии.
Проведена дифференциальная диагностика роста уровня ферритина, связанного с эффективностью терапии и возможным воспалительным процессом у пациенток. Значительное снижение количества лейкоцитов и концентрации С-реактивного белка через 4 нед после окончания лечения исключает воспалительный процесс на момент взятия контрольных анализов крови.
Опрос пациенток согласно шкале Лайкерта показал высокую степень удовлетворенности лечением.
СНЯ и НЯ при проведении исследования не возникали, что подтверждает безопасность применения препарата железа (III) гидроксида олигоизомальтозата.
Учитывая, что легкая и среднетяжелая гипофосфатемия часто протекает малосимптомно, рекомендовано измерение уровня фосфатов и кальция в сыворотке крови у пациенток с повышенной утомляемостью, мышечной слабостью и болью в костях.
ЗАКЛЮЧЕНИЕ / CONCLUSION
После терапии железа (III) гидроксида олигоизомальтозатом наблюдалось значимое повышение показателей качественного и количественного состава форменных элементов и биохимических показателей крови.
В посттрансфузионном периоде не отмечено клинически значимого влияния железа (III) гидроксида олигоизомальтозата на фосфорно-кальциевый обмен.
Терапия препаратом Монофер показала высокую удовлетворенность лечением и безопасность применения у пациенток с АМК, беременных (с 22-й недели беременности) и в послеродовом периоде.
Список литературы
1. Богданов А.Н., Мазуров В.И. Железодефицитные анемии в XXI веке. Вестник Северо-Западного государственного медицинского университета имени И.И. Мечникова. 2016;8(4):106–12.
2. Серов В.Н., Ди Ренцо Ж.К., Андреева М.Д. и др. Резолюция Cовета экспертов по профилактике и лечению железодефицитной анемии у беременных. Акушерство и гинекология. 2020;(4):230–6. https://doi.org/10.18565/aig.2020.4.230-232.
3. Баранов И.И., Дегтярёва Е.И., Самошкина Е.С., Абрамова С.В. Железодефицитные состояния при беременности. Акушерство и гинекология. Новости. Мнения. Обучение. 2015;4(10):68–76.
4. Ватутин Н.Т., Калинкина Н.В., Смирнова А.С. и др. Роль железа в организме человека. Вестник Харьковского национального университета имени В.Н. Каразина. Серия: Медицина. 2012;(24):74–80.
5. Андреичев Н.А., Балеева Л.В. Железодефицитные состояния и железодефицитная анемия. Вестник современной клинической медицины. 2009;2(3):60–5.
6. Schaefer B., Viveiros A., Tilg H. et al. Hypophosphataemia after treatment of iron deficiency with intravenous ferric carboxymaltose or iron isomaltoside – a systematic review and meta-analysis. Br J Clin Pharmacol. 2020;87(5):2256–73. https://doi.org/10.1111/bcp.14643.
7. Schaefer B., Tobiasch M., Wagner S. et al. Hypophosphatemia after intravenous iron therapy: Comprehensive review of clinical findings and recommendations for management. Bone. 2020;154:116202. https://doi.org/10.1016/j.bone.2021.116202.
8. Карахалис Л.Ю., Андреева М.Д., Ахиджак А.Н., Игнатьева Е.О. Железодефицитная анемия и состояние печени у беременных: корреляционные связи. Акушерство и гинекология. Новости. Мнения. Обучение. 2022;10(1):38–45. https://doi.org/10.33029/2303-9698-2022-10-1-38-45.
9. Курилович Е.О., Волкова О.И., Федорова Т.А. и др. Социально-экономические выгоды адекватной коррекции дефицита железа у беременных. Акушерство и гинекология. 2021;(9):212–20. https://doi.org/10.18565/aig.2021.9.212-220.
10. Клинические рекомендации. Железодефицитная анемия. М., 2021. 43 с. Режим доступа: https://cr.minzdrav.gov.ru/recomend/669_1. [Дата обращения: 10.12.2022].
11. Халафян А.А. STATISTICA 6. Математическая статистика с элементами теории вероятностей. М.: Бином, 2010. 492 c.
Об авторах
М. Д. АндрееваРоссия
Андреева Маргарита Дарчоевна – д.м.н., доцент, профессор кафедры акушерства, гинекологии и перинатологии ФПК и ППС; врач акушер-гинеколог
Scopus Author ID: 57200068605
350063 Краснодар, ул. Митрофана Седина, д. 4
350012 Краснодар, ул. Красных партизан, д. 6, корп. 2
А. Н. Ахиджак
Россия
Ахиджак Ася Нуховна – аспирант кафедры акушерства, гинекологии и перинатологии ФПК и ППС; зав. родильным отделением
350063 Краснодар, ул. Митрофана Седина, д. 4
350012 Краснодар, ул. Красных партизан, д. 6, корп. 2
А. Д. Белая
Россия
Белая Алина Дмитриевна – аспирант кафедры акушерства, гинекологии и перинатологии ФПК и ППС
350063 Краснодар, ул. Митрофана Седина, д. 4
Л. Ю. Карахалис
Россия
Карахалис Людмила Юрьевна – д.м.н., профессор кафедры акушерства, гинекологии и перинатологии ФПК иППС
350063 Краснодар, ул. Митрофана Седина, д. 4
350007 Краснодар, Площадь Победы, д. 1
Т. С. Кононенко
Россия
Кононенко Татьяна Сергеевна – ассистент кафедры акушерства, гинекологии и перинатологии ФПК и ППС
350063 Краснодар, ул. Митрофана Седина, д. 4
Рецензия
Для цитирования:
Андреева М.Д., Ахиджак А.Н., Белая А.Д., Карахалис Л.Ю., Кононенко Т.С. Оценка эффективности и безопасности применения железа (III) гидроксида олигоизомальтозата у женщин репродуктивного возраста с железодефицитной анемией. Акушерство, Гинекология и Репродукция. 2023;17(1):45-52. https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.378
For citation:
Andreeva M.D., Akhidzhak A.N., Belaya A.D., Karakhalis L.Yu., Kononenko T.S. Assessing efficacy and safety of iron (III) hydroxide oligoisomaltosate in reproductive-age women with iron deficiency anemia. Obstetrics, Gynecology and Reproduction. 2023;17(1):45-52. (In Russ.) https://doi.org/10.17749/2313-7347/ob.gyn.rep.2023.378

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.











































